查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





胸腺瘤相关重症肌无力(TAMG)是神经肌肉疾病与肿瘤共存的复杂临床情形,不仅患者发病率增加,其疾病进展和手术风险也显著高于单纯重症肌无力或胸腺瘤病例。重症肌无力(MG)是一种自身免疫性疾病,乙酰胆碱受体抗体(AChR-Ab)在发病机制中起核心作用,导致骨骼肌无力甚至危及生命的肌无力危象(MC)或术后肌无力危象(POMC)。胸腺瘤患者发生MG的概率约为30%-50%,且病情常严重并伴随高风险的术后呼吸并发症。
现有文献和临床研究表明,TAMG患者因肿瘤与自身免疫共同影响,术后POMC发生率高,导致术后恢复困难,住院周期延长,甚至危及生命。然而,围手术期TAMG患者的最佳免疫调控策略一直缺乏统一标准,传统免疫抑制治疗如糖皮质激素、硫唑嘌呤、他克莫司、静脉注射免疫球蛋白(IVIg)或血浆置换(PLEX)虽有效,但存在起效慢、依赖血制品或副作用大等限制,尤其在急性病程、快速行胸腺切除需求时,如何实现MG症状稳定与手术安全兼顾成为亟须解决的问题。随着生物靶向药物的发展,生儿Fc受体(FcRn)抑制剂艾加莫德因其独特机制和快速起效优势,已被批准用于gMG,但其在TAMG手术期应用的可行性与优势尚不明确。最近发表在《Journal of Thoracic Oncology》上的一项前瞻性、多中心、II期临床试验,对艾加莫德在TAMG患者胸腺瘤切除术围手术期的安全性和有效性进行了评估,为这类特殊患者群体提供了新的治疗选择和治疗策略。
本临床研究即基于上述临床问题,针对AChR-Ab阳性的TAMG患者,系统评价了艾加莫德于胸腺切除围手术期的安全性与疗效。研究共纳入中国多家三级医院的40例经胸部CT及抗体检测确诊的TAMG患者,全部为一般状况良好(ASA 1或2级)、器官功能正常、无严重合并症或近期使用生物制剂史的18-75岁成年人。所有患者均按照既定免疫治疗稳定方案(糖皮质激素剂量<50mg/d)维持,排除了既往行胸骨正中切口、近期剧烈体重下降、孕哺期、严重感染及免疫低下者。艾加莫德方案采用10mg/kg静脉注射,1、8、15、22天各1次,术前2次、术后2次(即2+2方案),手术当天为第9天;手术方式包括微创及传统胸骨正中切口,具体按肿瘤分期和生长范围决定。疗效随访包括围手术期每周及术后1、2月,分别评估MG-ADL、QMG、MGC等量表变化,监测免疫球蛋白与AChR-Ab水平,分析手术出血、引流、住院天数、POMC及其他不良事件。
结果显示,入组患者中女性占57.5%,年龄中位数46岁,病程中位为3个月,MGFA分级以IIa(32.5%)、Ⅲa(30%)为主。术式以T2b微创胸腺切除为主(52.5%)。手术相关出血量平均96.8±153.9ml,术后住院天数7.1±5.0天。围手术期TEAE发生率62.5%,多为轻度(如感染30%主要为轻度肺炎和胸腔积液),未观察到致死或导致停药的不良反应。POMC发生率10%(4/40),均发生于术野广、合并膈肌或膈神经切除的高危病例。
疗效方面,所有患者在MG-ADL、QMG、MGC量表均表现为“响应者”,手术后1周即有明显症状缓解,MG-ADL平均下降4.6分,QMG下降6.5分,MGC下降6.6分。2个月时,82.5%达到缓解(包括完全稳定、药物缓解及最小表现状态);75%达到显著临床改善(CMI定义为MG-ADL≥2分减少)、57.5%达最小症状表达(MSE,MG-ADL=0或1)。
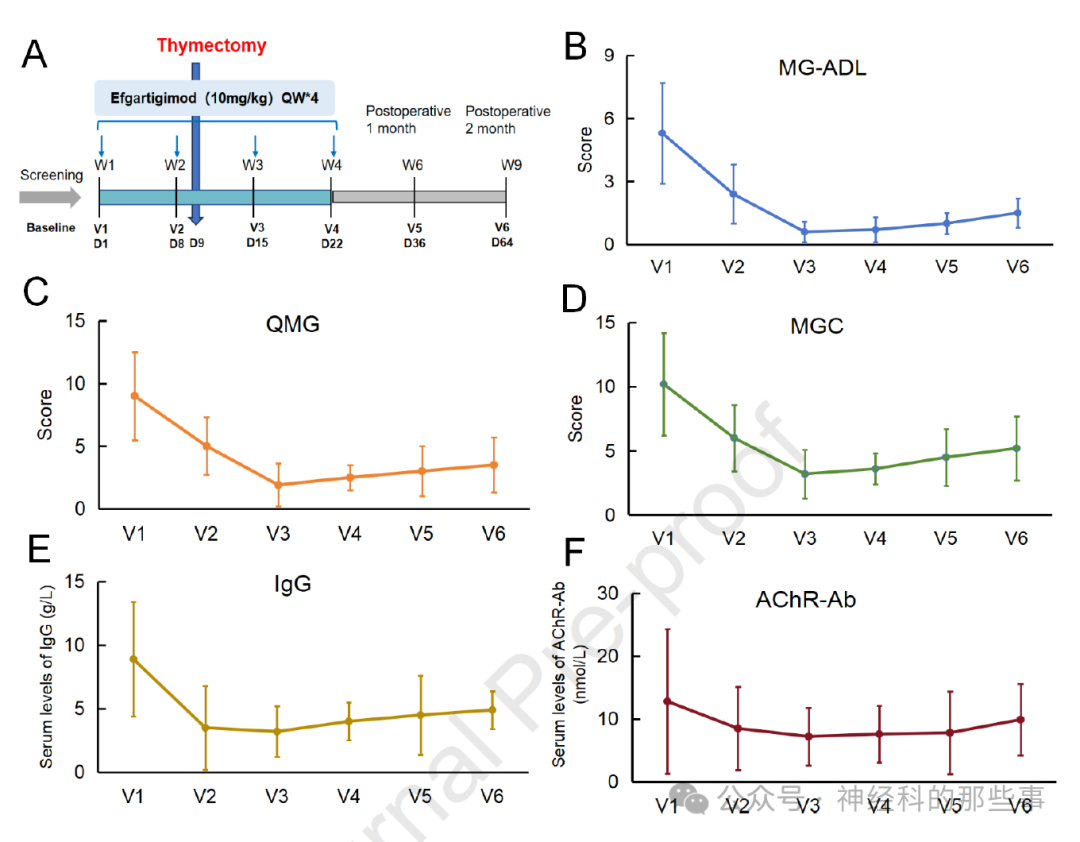
图:艾加莫德用于胸腺瘤相关重症肌无力的2期研究示意图(A)。MG-ADL(B)、QMG(C)和MGC(D)评分的变化,以及IgG(E)和AChR-Ab(F)从基线(访视1)在整个研究过程中的变化。
对不同肌群分析显示,延髓肌群改善最显著(70.5%)、肢体(65.1%)、呼吸肌(62.3%)、眼肌次之(60.7%)。实验室指标方面,IgG及AChR-Ab水平均于术后快速下降,最大降幅分别为64.0%、43.8%,2月后稳态仍优于基线;而IgA、IgM、IgE及总补体无显著变化,显示艾加莫德选择性靶向IgG,未损害其他体液免疫。
在与传统免疫治疗及其他生物靶向药的对比中,艾加莫德最大优势表现为起效速度快、疗效显著、机制特异性强,且无需干预既有药物,不增加疫苗失效及广泛免疫抑制的风险。传统免疫抑制剂需要1-2月症状改善,且药物调整和副作用频发,而IVIg/PLEX虽启动快,但技术要求高、依赖血制品且成本巨大。其他生物制剂如B细胞耗竭及补体抑制剂(如利妥昔单抗、eculizumab)常伴随更强免疫抑制及疫苗相关风险,不适合围手术期广泛应用。艾加莫德对IgG亚型有特异性清除,减少病理性AChR抗体水平,同时保留IgA、IgM等对抗感染关键免疫,不增加感染风险;本研究中感染以轻型为主,未发生播散性感染及脓毒症。尤其在高危人群或需快速准备手术的MG患者,2+2方案能于较短时间内实现神经肌肉症状缓解,降低术后POMC风险(既往公开研究报告POMC发生率常见区间为15%至40%),提高围手术期安全性,这一点为TAMG围手术期管理带来创新思路与高价值补充。
本研究直接的临床启示是,艾加莫德可优先推荐用于病情急进、需快速手术、肿瘤负担大或既有免疫抑制方案效果不佳的TAMG患者,尤其适用于:(1)晚期/需广泛切除的胸腺瘤患者;(2)合并延髓肌、呼吸肌损害的高危重症MG病例;(3)对传统药物耐受不良或需快速稳定症状者;(4)需缩短术前准备、提高手术窗口期者。在保护患者免疫功能的基础上减少POMC发生率、缩短住院时间和降低ICU需求,对重症肌无力合并胸腺瘤的外科治疗安全开展意义重大。此外,数据还支持外科和神经内科可联合制订基于风险分层的围手术期免疫方案,形成更加个体化和精细化的TAMG管理流程,为后续国际指南的优化提供坚实证据。
研究局限性包括:样本量较小且随访时间有限,限制了长期疗效与安全性评估;入患者病种异质性较高,包括TNM I-IVa不同分期及多种术式,结果外推需谨慎;未纳入MGFA I类和纯粹眼肌型TAMG患者,未能探讨其在轻型病例的效果;纳入对象均为中国人群,种族差异等影响有待多中心确认。此外,2个月的短期内疗效数据虽已展现早期益处,随后炎性免疫重构及长期复发率、对肿瘤本身的控制效果,尚需持续观察与后续研究。成本效益亦需在更大型健康经济研究中结合保险政策分析。未来方向建议扩大样本,延长随访,并尝试与其他靶向治疗头对头比较,以及探索基于风险分层的免疫调控个体化策略。
总之,这项前瞻性多中心II期试验证实艾加莫德在TAMG围手术期具有快速、显著且安全的神经肌肉症状缓解作用,显著降低POMC风险,简化围手术期管理,为高风险TAMG患者的个体化治疗提供了新的靶点与策略。后续需以更大样本和长期随访验证其安全性和最佳适应证,推动国际共识和指南更新,进一步帮助TAMG患者群体。
Perioperative Safety and Efficacy of Efgartigimod for Thymoma associated Myasthenia Gravis: A Prospective, Multicenter, Phase II Clinical Trial. J Thorac Oncol. 2025 May 2:S1556-0864(25)00703-8.
来源:神经科的那些事
查看更多