查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过






患者男性,49岁,2021年7月1日因“肝癌切除术后3年余,全身黄染10天”为主诉入院。
现病史 患者3年前在外院行腹腔镜肝肿瘤切除术,术后病理提示“肝细胞癌(HCC)”,术后半年内行肝动脉化疗栓塞术(TACE)预防,术后半年余发现复发,应用索拉非尼治疗,定期复查病情仍有进展;8个月前换为瑞戈非尼治疗,因副反应无法耐受停用,后应用阿帕替尼+卡瑞利珠单抗治疗。半年前(2021.01.07)PET-CT发现“胰头部可疑淋巴结转移”,外院行伽马刀放疗。10天前出现全身皮肤巩膜黄染,为进一步治 疗来院就诊。
既往史 十二指肠溃疡病史,无肝炎病史,无高血压、糖尿病、冠心病史。
个人史 无饮酒和吸烟史。
家族史 否认家族性遗传病史。
体格检查 口唇结膜无苍白,全身皮肤黏膜黄染。腹部可见陈旧性手术疤痕,上腹部轻压痛,肝区轻叩击痛。PS评分0 分,Child-Pugh分级B级。
实验室检查 血红蛋白105g/L,血小板243x109/L,总胆红素108.8μmol/L,直接胆红素97.7μmol/L,白蛋白36.7g/L,甲胎蛋白(AFP)32.97ng/ml。凝血功能基本正常。
辅助检查 PET-CT(2021.04.12):原发性肝癌术后近3 年、介入治疗后、靶向及免疫治疗中+胰头可疑转移灶伽马刀治疗后。与上次(2021.01.07)PET-CT 图像相比:原右残肝前缘病灶较前有所扩大,中央区仍无明显氟代脱氧葡萄糖(FDG)代谢活性,但新见其周边组织高度摄取FDG,考虑活性肿瘤组织可能性大;原胰头部可疑转移灶部位FDG水平较前减低;原胰周可疑淋巴结转移灶大小及FDG摄取水平较前变化不明显。
上腹增强CT(2021.07.01):肝右叶术后所见,术区下方略低密度灶,胰头略低密度灶并胆总管末端截断、胆系扩张,建议强化扫描或MRI进一步检查;胆囊炎;腹腔多发小淋巴结可见;所示胃窦壁、十二指肠壁较厚,建议结合胃镜。
初步诊断 1.肝细胞癌术后复发;2.梗阻性黄疸;3.胰周转移瘤、腹腔淋巴结转移;4.十二指肠溃疡。
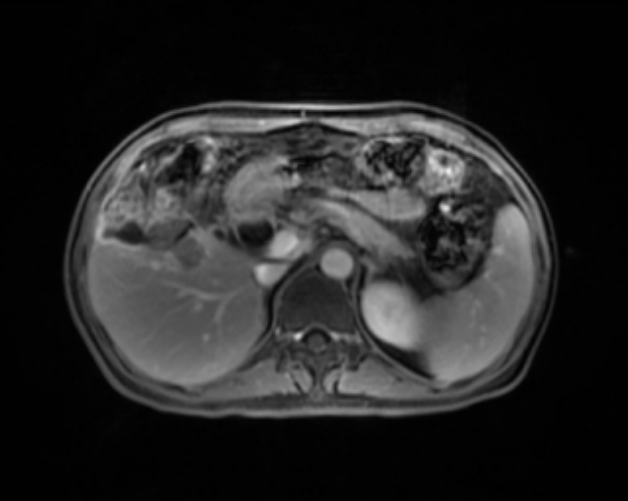
图1 肝脏强化 MRI (2021.07.03)
第一次多学科诊疗(MDT):1.2021.07.06行内镜下金属覆膜胆道支架植入术(胆总管狭窄,ERCP+EST+EMBE,十二指肠溃疡伴球部狭窄,慢性非萎缩性胃炎);2.贝伐珠单抗+阿替利珠单抗治疗;3. TACE治疗。
疗效评价:2021.11.22 复查 PET-CT,与上次(2021.04.12)PET-CT图像相比,原右残肝前缘病灶较前有所扩大,FDG代谢水平增高,考虑疾病进展可能性大;原胰头部可疑灶部位未见异常FDG代谢;原胰周可疑淋巴结转移灶大小及FDG摄取水平较前变化不明显。
患者出现明显上腹部痉挛痛,无法耐受,2022.02.23给予内镜下胆管支架取出+鼻胆管引流术,拔除支架后上腹痛较前明显缓解。
2022.03.18患者出现大便带血,血红蛋白降至71g/L,患者进食困难。行胃肠镜检查:胃镜见十二指肠球部狭窄,胃镜无法通过;结肠镜发现肝癌侵犯结肠肝区导致活动性出血。
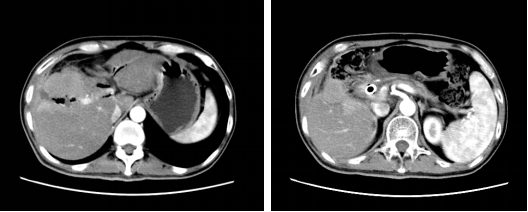
图 2 放入支架后腹部CT
第二次MDT:考虑结肠肝曲病理示肝细胞癌转移,于2022.03.28行开腹探查,肝肿瘤侵犯结肠部分切除+胃空肠吻合+肝肿瘤微波消融术。
2022.04.09患者清晨出现呕大量鲜血,介入科紧急行腹腔动脉造影及胃十二指肠动脉栓塞术,术中肝固有动脉栓塞。
第三次MDT:患者转移瘤行基因检测;给予仑伐替尼+阿替利珠单抗+淫羊藿素软胶囊。
疗效评价:2022.08.04影像结果示肿瘤稳定,未再继续增大,较前略有减小(图3)。
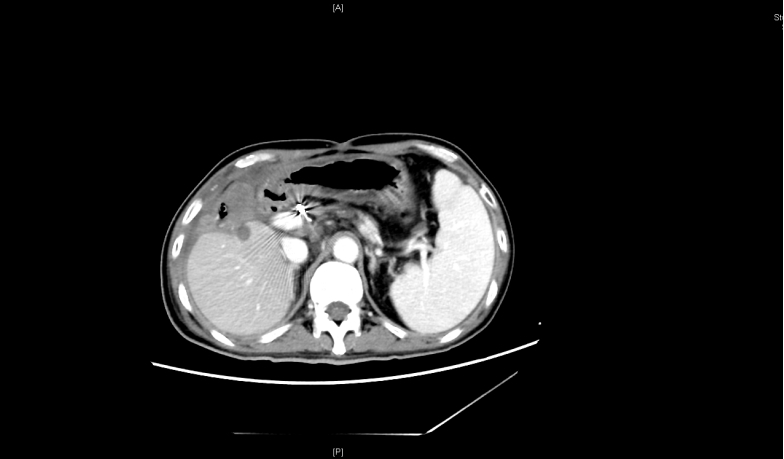
图3 腹部CT(2022.08.04)
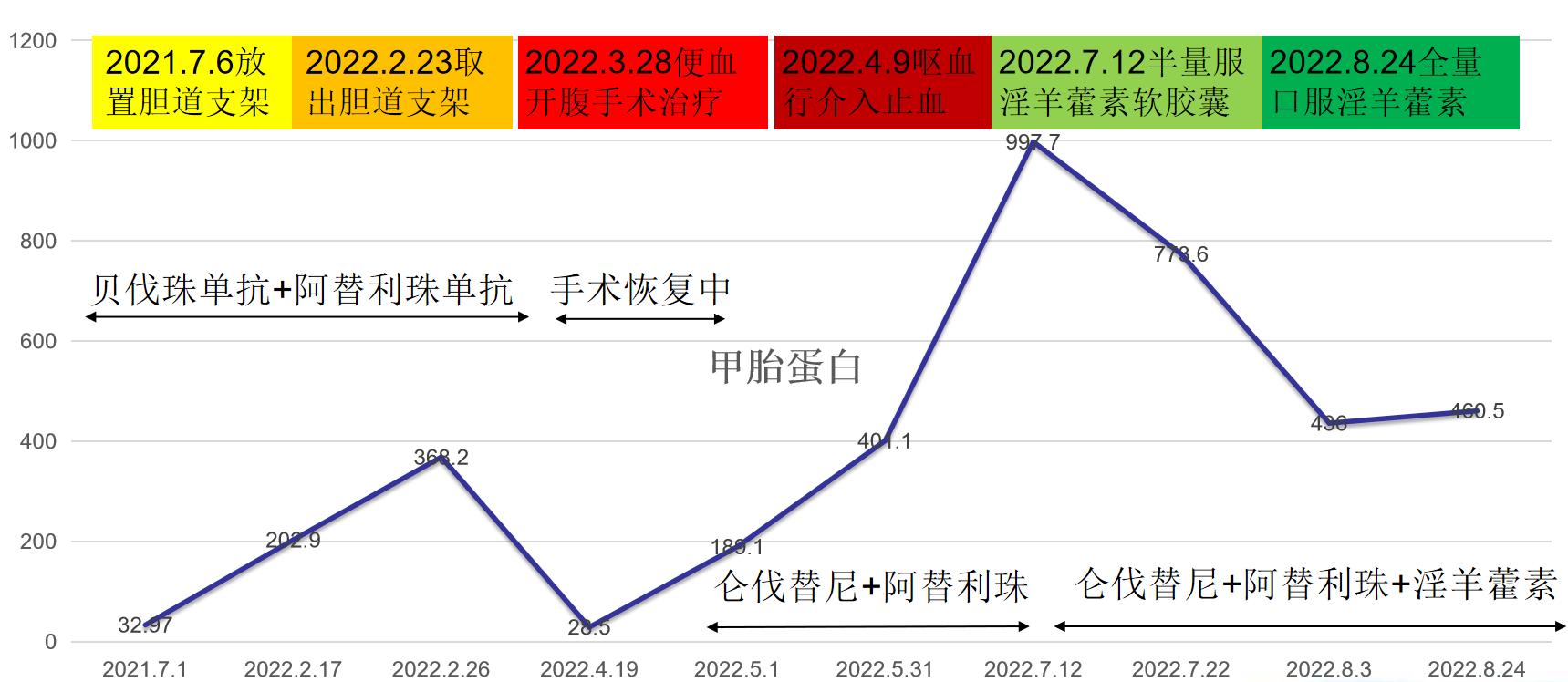
图4 治疗期间AFP(单位:ng/ml)水平
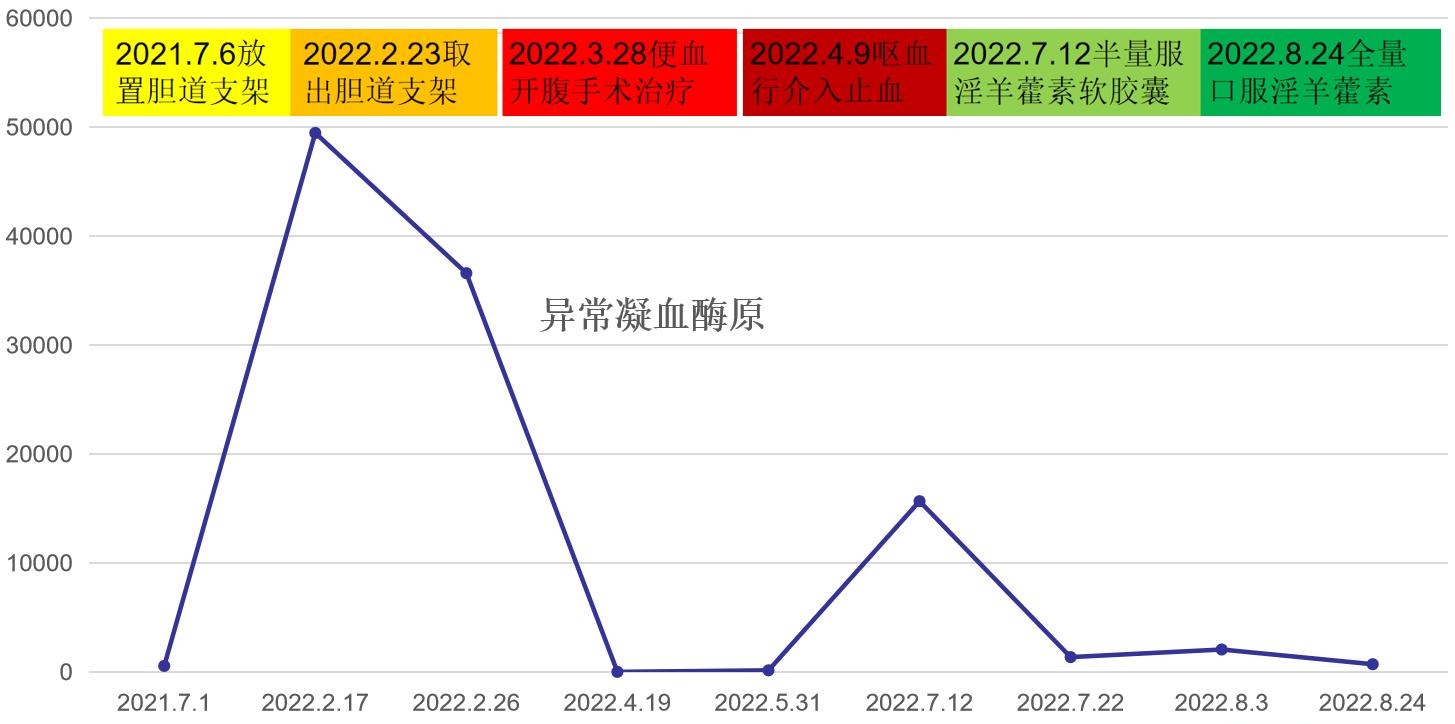
图5 治疗期间异常凝血酶原(PIVKA-Ⅱ单位:mAU/ml)水平
山东大学第二医院 靳斌

本病例患者为HCC术后复发,同时伴有梗阻性黄疸及胰周转移瘤、腹腔淋巴结转移。行TACE后给予贝伐珠单抗+阿替利珠单抗治疗;评估疾病进展后调整治疗方案为仑伐替尼+阿替利珠单抗+淫羊藿素软胶囊药物联合治疗,影像结果示肿瘤稳定,较前略有减小,AFP及PIVKA-Ⅱ均显著下降。
抗程序性死亡蛋白-配体1(PD-L1)抗体+抗血管内皮生长因子抗体为代表的联合治疗在不可切除的HCC中观察到优秀的临床疗效。然而,在应用阿替利珠单抗+贝伐珠单抗治疗中可能会产生耐药1。淫羊藿素软胶囊与细胞毒类抗肿瘤药物、靶向抗肿瘤药物及免疫检查点抑制剂不同,可以通过联合多重机制和靶点进行相互作用。研究显示,淫羊藿素软胶囊可以抑制IL-6/STAT3通路并阻断肿瘤坏死因子-α(TNF-α)介导的IKK/P65通路,发挥抗肿瘤作用,并且可以抑制PD-L1表达,与免疫治疗协同增效2。本病例中,患者在应用贝伐珠单抗+阿替利珠单抗治疗期间AFP及 PIVKA-Ⅱ呈持续上升趋势,PET-CT提示考虑疾病出现进展,经评估后调整治疗方案为仑伐替尼+阿替利珠单抗+淫羊藿素软胶囊药物联合治疗,PIVKA-Ⅱ及AFP呈明显下降趋势,且肿瘤病灶明显缩小。
AFP和PIVKA-Ⅱ是HCC常见的预后生物标志物,两者联合检测可提高HCC阳性检出率。PIVKA-Ⅱ与多种不良临床病理特征及预后密切相关,可作为评估中晚期HCC患者预后的潜在生物标志物3。此外,术后连续监测PIVKA-Ⅱ有助于监测肿瘤的复发,PIVKA-Ⅱ水平降低并维持低水平者HCC复发风险显著降低4。研究显示,AFP或PIVKA-Ⅱ降低>50%的HCC患者的无进展生存时间显著高于降低<50%的患者(P<0.05)5。 本病例患者在给予淫羊藿素软胶囊联合治疗后,PIVKA-Ⅱ及AFP在1个月内迅速下降50%以上,这为患者带来了新的希望。此外,淫羊藿素软胶囊的安全性极好,≥3级治疗相关不良事件发生率约为12%,停药率仅为0.7%6。
淫羊藿素软胶囊可以通过多种机制发挥抗肿瘤作用,调节免疫微环境,降低术后复发或转移风险,且安全性良好。期待未来淫羊藿素软胶囊联合局部治疗或免疫与靶向治疗可以进一步优化HCC治疗格局,为更多的患者获得最佳生存获益的同时保障生活质量。
1. Liu K, et al. J Clin Med Res. 2016 Apr;8(4):297-302.
1. Lu L, et al. Curr Res Immunol. 2022 Jun 3;3:118-127.
2.Tan HL, et al. Front Pharmacol. 2016 Jun 29;7:191.
3.薄维波,等. 实用医学杂志,2021,37(23).
4.Kim DY, et al. Oncology 2007;72 suppl 1:52-57.
5.Sun et al. BMC Cancer (2021) 21:775.
6.CSCO 2021 Keynote Speech.
查看更多