查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





1.AB是院内感染常见的条件致病菌之一,2024年上半年CHINET数据显示其对碳青霉烯类抗生素耐药率超70%。
2.CRAB耐药由多种机制引起,产生D类β-内酰胺酶为主要机制之一。
前言
鲍曼不动杆菌(AB)为革兰阴性杆菌,是导致医院感染的常见条件致病菌之一1。2024年上半年中国细菌耐药监测网(CHINET) 发布的数据显示,AB耐药形势严峻,碳青霉烯类耐药的鲍曼不动杆菌(CRAB)检出率逐渐增长2,同时亚太地区的耐药数据显示,我国耐药AB菌的检出率位于第3,仅次于韩国和印度3。2024年上半年CHINET数据显示AB对碳青霉烯类药物的耐药率超70%2,对大多数抗菌药耐药率高,仅对少数药物敏感,可选择的治疗药物有限2。
因此,了解AB的耐药机制具有重要的意义,本文将对CRAB的多种耐药机制进行描述,通过了解这些机制,为制定适宜的抗感染治疗方案及防控AB耐药提供指导。
CRAB的耐药机制较为复杂,包括产生β-内酰胺酶以及其他耐药机制(渗透性降低和外排泵、作用靶点改变、生物膜的形成)4。
AB耐药的主要机制之一:
产生β-内酰胺酶4
β-内酰胺酶是一种由细菌产生的酶,能够水解β-内酰胺类抗生素的活性中心环结构,使抗生素失去抗菌活性,是AB耐药的重要原因(图1)4,5。该酶按照Ambler分类方法分为A、B、C、D四类6。
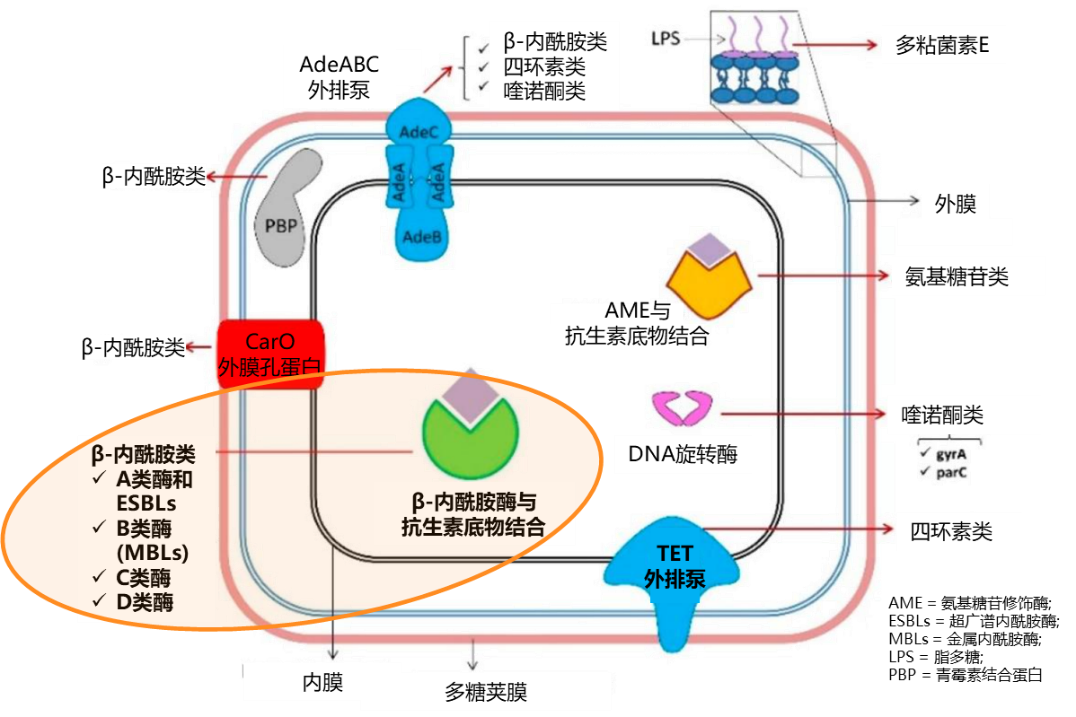
图1 AB的耐药机制7
A类酶:一般为质粒介导,可以水解青霉素和早期头孢菌素,如肺炎克雷伯菌碳青霉烯酶(KPC),在AB菌中较罕见4,6;
B类酶:金属β-内酰胺酶(MBL),需要锌离子才能发挥活性,能够水解青霉素、头孢菌素和碳青霉烯类4。常见的MBL包括NDM、VIM、IMP,通常对除单环内酰胺外的所有β-内酰胺类药物都具有耐药性4。
C类酶:头孢菌素酶(AmpC)β-内酰胺酶在β-内酰胺类抗生素诱导下产生,可能导致细菌在治疗期间耐药性升级4。
D类酶:是AB耐药机制中研究最多的,以丝氨酸苯唑西林酶(OXA酶)(OXA-23,OXA-24,OXA-58)最常见,在CRAB耐药性方面起着关键作用4,6。一项国际多中心前瞻性观察队列研究显示,全球CRAB产酶均以OXA-23最多见,其中我国CRAB产OXA-23最高,达99%8。
当前针对难治性耐药性AB感染常用的β-内酰胺类抗生素包括β-内酰胺/β-内酰胺酶抑制剂联合制剂(如舒巴坦-度洛巴坦)和碳青霉烯类9。其中,度洛巴坦可抑制A、C、D类β-内酰胺酶,主要抑制D类酶 (OXA-23、OXA-24和OXA-58),恢复了舒巴坦对AB的活性,可有效针对AB9-10。
① 膜渗透性降低或外排泵4
渗透性降低:渗透性降低是AB对抗生素耐药的重要机制之一,主要影响亲水性抗生素(如β-内酰胺、氨基糖苷和甘氨酰环素类)的活性,通过改变细菌外膜的通透性阻碍抗生素进入微生物细胞,降低抗生素在细胞内的浓度和有效性,包括膜孔蛋白修饰、脂多糖(LPS)修饰、胶囊产生、生物膜产生等。
外排泵:可排出多种抗生素包括氟喹诺酮类、四环素类和氯霉素,降低细胞内抗生素的浓度,产生耐药。
② 作用靶点改变4
β-内酰胺类抗生素与青霉素结合蛋白(PBP)结合发挥抗菌作用,AB通过针对PBP的基因突变或获得新的PBP基因,降低抗生素与PBP的亲和力产生耐药性。此外,核糖体修饰、脂质A结构改变也将引起不同类别的抗生素耐药。
③ 生物膜形成4
生物膜的形成可使细菌对抗菌药耐受性提高10-1000倍,AB具有很强的形成生物膜的能力,能够在呼吸道、体内植入物等表面形成并长期存活,增强了其对抗生素的耐药性1。
AB对多种抗菌药物(尤其是碳青霉烯类)存在耐药,其耐药机制复杂多样。包括产生β-内酰胺酶、渗透性降低或外排泵、抗生素作用靶点改变和生物膜形成在内的多种复杂机制。其中,D类β-内酰胺酶在CRAB耐药性方面起着关键作用。度洛巴坦可抑制D类β-内酰胺酶,恢复舒巴坦对AB的活性9。
审批号:PP-XAD-CHN-0027 到期日:2027-1-6
仅供医疗卫生专业人士阅读/参考
编辑:天之涯
参考文献:
1.侯小丫, 等. 国际生物制品学杂志, 2022, 45(2): 111-115.
2.CHINET 2024年上半年细菌耐药监测结果.
3.Chen CH, et al. Int J Antimicrob Agents. 2023;61(2):106707.
4.Marino A, et al. Int J Mol Sci. 2024;25(13):6814.
5.Alkekhia D, et al. ACS Appl Mater Interfaces. 2022;14(24):27538-27550.
6.侯盼飞,等.上海交通大学学报(医学版),2010,30(01):98-103.
7.Moubareck CA, et al. Antibiotics (Basel). 2020 Mar; 9(3), 119
8.Wang MG, et al. Clin Infect Dis . 2024 Feb17;78(2):248-258
9.Rafailidis P, et al. Antibiotics (Basel). 2024;13(3):261.
10.Tamma PD, et al. Clin Infect Dis. 2024 Aug 7: ciae403.
查看更多