查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





长期以来,放疗一直是局晚期妇科肿瘤的主要治疗方式,也是实现转移性疾病缓解的重要手段1。随着科技的进步与实践的积累,放疗技术的应用趋于成熟与完善,为妇科肿瘤带来了更精确、更有效的治疗2。但在不同类型妇科肿瘤中,放疗的应用存在着差异。
欧阳翼教授
中山大学附属肿瘤医院放疗科副主任医师
中华医学会放射肿瘤妇瘤学组委员
中国抗癌协会近距离放射治疗专业委员会委员
中国抗癌协会近距离放射治疗专业青委副主委
广东省医学会放射治疗专委会近距离放疗学组副组长
广东省中西医结合学会放疗专委会常委
广东省医学会心身医学分会巴林特联盟学组组员
一、举足轻重:放疗在妇瘤治疗中的重要地位
放疗是妇科肿瘤中重要的治疗手段之一。在不同妇科肿瘤类型中,放疗应用于根治性治疗、辅助治疗以及复发/转移的治疗。
图1. 放疗在不同类型妇科肿瘤中的地位
放疗是宫颈癌、子宫内膜癌、阴道癌、外阴癌的常用治疗方式,尤其在宫颈癌中是主要治疗手段。
宫颈癌 | 主要治疗手段,适用于各期宫颈癌患者,尤其是局部晚期患者3-6 |
子宫内膜癌 | 是术后辅助的重要治疗手段,包括特殊类型子宫内膜癌,也是复发和转移性子宫内膜癌的重要治疗手段7-10 |
阴道癌 | 适用于Ⅰ ~Ⅳ期病例,是大多数阴道癌患者首选的治疗。尤其适用于Ⅱ期及以上中晚期患者及失去手术机会的患者11-13 |
外阴癌 | 主要用于局晚期患者和术后辅助治疗,也可用于姑息性治疗和系统性治疗14-16 |
子宫肉瘤 | 主要用于有肿瘤残留或有亚临床转移区域的补充治疗,以及复发/转移病灶的姑息性治疗,也可用于术后辅助治疗17-19 |
卵巢癌 | 很少使用,应经过多学科会诊讨论决定。可用于不适合手术切除或存在手术禁忌证的局灶性复发,或需姑息放疗的患者20-23 |
表1.放疗在妇科肿瘤中的治疗地位
二、相辅相成:放疗在妇科肿瘤围术期的应用
1. 辅助放疗可改善早期中高危因素宫颈癌的预后
具有中危因素患者,通过Sedlis标准、“四因素”模型可判断辅助放疗获益人群。GOG-092研究,验证了符合Sedlis标准(术后存在中危不良病理因素:脉管受累、子宫颈肿瘤直径>4 cm、浸润子宫颈间质深层)的患者,给予辅助放疗将使患者获益(2年无复发率,辅助放疗 vs. 无进一步治疗,88% vs 79%,P=0.008)24。将Sedlis标准3个中危因素与病理因素联合的“四因素”模型:肿瘤≥3cm,外1/3深间质受侵,淋巴脉管受侵,腺癌或腺鳞癌,进一步表明存在任意两种危险因素均提示预后不良25。GOG 109研究显示,符合入组条件243例早期高危宫颈癌患者的4年PFS和OS率,单纯放疗均低于同步放化疗(63% vs. 80%,P=0.003和71% vs. 81%,P=0.007)26。
图2. GOG 109研究的生存结果
2. 辅助放疗可减少子宫内膜癌局部复发
辅助放疗可减少子宫内膜癌局部复发,但未能提高总生存率。前瞻性PORTEC-1研究显示,相比于未接受进一步治疗,接受辅助外照射治疗(EBRT)有效减少5年局部复发率(4% vs 14%),但5年总生存率相似(81% vs 85%)27。
图3.PORTEC-1研究辅助放疗 vs. 无进一步治疗的局部复发结果
3. 辅助放疗显著提高高危外阴癌患者生存
纳入257例原发性外阴癌患者的多中心回顾性研究显示,切缘阳性或近切缘的外阴癌患者,接受术后辅助放疗,5年OS率从29%提升至67.6%,与切缘阴性患者相似28。前瞻性GOG 37研究显示,6年时,放疗癌症相关死亡的累计发病率29%,而盆腔淋巴结切除术癌症相关死亡为51%(P=0.015)29。
4. 辅助放疗降低子宫肉瘤局部复发风险,但不同亚型中存在差异
纳入224 例Ⅰ-Ⅱ期子宫肉瘤术后患者的前瞻性研究显示,盆腔放疗组局部控制率提高,但子宫平滑肌肉瘤(uLMS) 亚组未显示出任何获益, 局部复发率无改善30。另有研究显示,辅助放疗对改善子宫内膜间质肉瘤OS无意义31,但能提升高级别子宫内膜间质肉瘤(HG-ESS)32、子宫内膜肉瘤(UUS)生存率33。
5. 新辅助放疗可为外阴癌&子宫肉瘤患者创造手术机会
在外阴癌中,术前放疗/术前放化疗即新辅助治疗主要适用于无法耐受手术、拒绝手术或需要扩大手术的局部晚期患者34。在子宫肉瘤中,新辅助放疗可能有助于控制缩小癌灶创造手术机会或缩小肿瘤范围,提高手术切除率35。
三、争先恐后:放疗联合化疗的模式探讨
1. 同步放化疗
局晚期宫颈癌同步放化疗后IGABT可获得长期局部控制及生存。前瞻性EMBRACE-1研究显示,中位随访51个月,同步放化疗后行MRI引导的自适应近距离放疗(IGABT)治疗局晚期宫颈癌,总体5年OS率为74%,总体5年局部控制率为92%36。此外,研究证实,同步放化疗可减少局晚期子宫内膜癌局部复发(GOG-258研究)37,同步放化疗也有效延长局晚期外阴癌患者生存38。
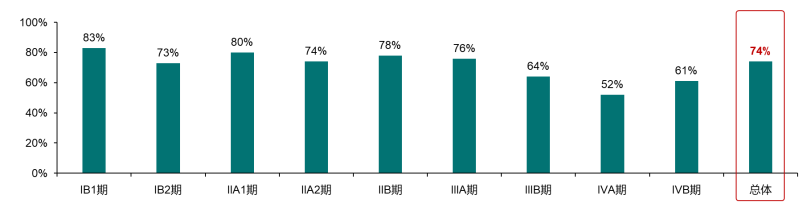
图4.EMBRACE-1研究不同FIGO 2009
分期宫颈癌患者的5年OS率
2. 诱导化疗+同步放化疗
诱导化疗+同步放化疗显著改善局晚期宫颈癌生存。INTERLACE研究是一项III期、随机、对照研究,纳入500例局晚期宫颈癌患者,随机1:1分组分别接受诱导化疗+同步放化与单独同步放化疗,主要终点为PFS及OS。结果显示,诱导化疗+CRT vs. 单独CRT,显著改善PFS(5年PFS率,73% vs. 64%,P=0.013)与OS(5年OS率:80% vs. 72%,P=0.04)39。
3. 同步放化疗+辅助化疗
同步放化疗+辅助化疗未能改善局晚期宫颈癌的生存,但对局晚期子宫内膜癌的生存有改善。III期OUTBACK研究显示,放化疗+辅助化疗 vs. 单独放化疗,两组间5年OS率无显著性差异(72% vs 71%,P=0.81)40。而在III期PORTEC-3研究显示,放化疗 vs. 单独放疗可显著改善5年OS率(81.4% vs. 76.1%,P=0.034)41。
图5. PORTEC-3研究中,放化疗 vs. 单独放疗的OS
4. 放疗+靶向治疗
放疗+靶向治疗可提高局晚期宫颈癌的ORR。2024年ASCO大会报告了两项nimotuzumab联合放疗用于局晚期宫颈癌的研究。一项随机对照III期CC3研究显示,相比于仅接受同步放化疗,nimotuzumab+同步放化疗治疗局晚期宫颈癌ORR更长(83.80% vs. 74.31%,P=0.049),但1年PFS率(96.1% vs. 92.1%,P=0.506)相似42。另一项前瞻性单臂研究显示,nimotuzumab+放疗的1年OS为96.03%、2年OS为90.21%,1年DFS为85.71%、2年DFS为78.31%,ORR为89.92%,DCR为93.28%43。
四、创新引领:免疫与放疗的联合治疗新篇章
1. 免疫治疗+同步放化疗已有探索
不同研究显示,免疫治疗+同步放化疗对于妇科肿瘤的改善存在差异。小样本量研究显示,特瑞普利单抗+同步放化疗的客观缓解率(ORR)达到了100%、完全缓解率(CR)为90%、部分缓解(PR)率为10%44。而在III期CALLA研究显示,度伐利尤单抗+同步放化疗未显著改善高危LACC患者的PFS (HR 0.84,P=0.174)45。
2. KEYNOTE-A18研究:开启妇瘤标准治疗新方式
随机、双盲、III期、对照研究——ENGOT-cx11/GOG-3047/KEYNOTE-A18研究(KN-A18)纳入980例新诊断、未经治疗过的高危LACC患者,随机分组分别接受帕博利珠单抗+标准方案的放化疗+随后的帕博利珠单抗治疗与安慰剂+标准方案的放化疗,主要终点为PFS和OS。
图6. KEYNOTE-A18研究的研究设计
结果显示:帕博利珠单抗治疗组较安慰剂组:显著改善高危LACC患者的PFS:24个月PFS率分别为67.8% vs. 57.3%(HR 0.70,P=0.0020),且在协议预定的各亚组中PFS分析支持帕博利珠单抗联合同步放化疗获益;降低27%的死亡风险:24个月的OS率分别为87.2% vs. 80.8%(HR 0.73);有更高的ORR和DOR。帕博利珠单抗联合同步放化疗的全因AEs、治疗相关AEs的发生率与安慰剂相比没有更高,安全性可控。KEYNOTE-A18研究支持帕博利珠单抗联合同步放化疗作为新诊断、未经治疗过高危LACC新的潜在的标准治疗方案46。
近期,ESMO GYN公布了KEYNOTE-A18研究的东亚人群结果。对于主要终点PFS,帕博利珠单抗治疗组与安慰剂组24个月PFS率分别为77.6% vs. 59.8%(HR 0.55),两组差异进一步加大,帕博利珠单抗在东亚人群表现更优。在安全性方面,帕博利珠单抗组安全可控,与全球人群结果一致47。
图7. KEYNOTE-A18研究PFS和OS的结果
图8. KEYNOTE-A18研究ORR和DOR结果
图9. KEYNOTE-A18研究东亚人群PFS
*帕博利珠单抗NMPA获批实体瘤适应证:微卫星高度不稳定型或错配修复基因缺陷型肿瘤,本适应症基于替代终点获得附条件批准上市,暂未获得临床终点数据,有效性和安全性尚待上市后进一步确证。
3. 免疫联合放疗在妇瘤领域的探索持续进行中
NRG-GY020研究,探讨了帕博利珠单抗+常规放疗治疗早期中高危dMMR子宫内膜样子宫内膜癌的疗效与安全性,主要终点为3年无复发生存率49。期待该该项研究结果的呈现。
4. 免疫联合放疗在2024 ASCO & ESMO GYN依然为妇瘤领域热点内容
2024年ASCO大会已于近日召开,会上报告了多项宫颈癌相关临床研究。其中,免疫联合放疗依然为热点内容:
表2 2024年ASCO & ESMO GYN大会宫颈癌相关研究
五、总结
放疗在妇科肿瘤的治疗中占据重要地位,尤其在宫颈癌与子宫内膜癌中。在围术期治疗中,辅助放疗可为妇科肿瘤患者带来生存获益或局部控制。放疗的多种模式在积极探索中,如同步放化疗、新辅助化疗+同步放化疗、同步放化疗+辅助化疗,并取得了令人鼓舞的结果。免疫治疗联合同步放化疗是妇科肿瘤放疗新型的联合模式,KEYNOTE-A18研究的阳性结果支持这一联合,而更多的研究也在持续进行中。
参考文献:
1. Venkat PS, et al. Curr Opin Obstet Gynecol. 2019.
2. Fabian A, et al. J Clin Med. 2020;10(1):93.
3. NCCN Guidelines. Cervical Cancer . 2024. V2.
4. 中国临床肿瘤学会(CSCO). 宫颈癌诊疗指南 2023.
5. 中华妇科肿瘤学分会. 中国妇科肿瘤临床实践指南第7版 (2023): 子宫颈癌.
6. 中国抗癌协会 (CACA). 中国肿瘤整合诊治指南: 宫颈癌. 2022.
7. NCCN Guidelines. Uterine Neoplasms. 2024.V2.
8. 中国临床肿瘤学会(CSCO). 子宫内膜癌诊疗指南 2023.
9. 中华妇科肿瘤学分会. 中国妇科肿瘤临床实践指南第7版 (2023): 子宫内膜癌.
10. 中国抗癌协会 (CACA). 中国肿瘤整合诊治指南: 子宫内膜癌. 2022.
11. NCCN Guidelines. Vaginal Cancer. 2025.V1.
12. 中华妇科肿瘤学分会. 中国妇科肿瘤临床实践指南第7版 (2023): 阴道癌.
13. 中国抗癌协会 (CACA). 中国肿瘤整合诊治指南: 阴道癌. 2022.
14. NCCN Guidelines. Vulvar Cancer. 2024.V3.
15. 中华妇科肿瘤学分会. 中国妇科肿瘤临床实践指南第7版 (2023): 外阴癌.
16. 中国抗癌协会 (CACA). 中国肿瘤整合诊治指南: 外阴癌. 2022.
17. NCCN Guidelines. Uterine Neoplasms. 2024.V2.
18. 中华妇科肿瘤学分会. 中国妇科肿瘤临床实践指南第7版 (2023): 子宫肉瘤.
19. 中国抗癌协会 (CACA). 中国肿瘤整合诊治指南: 子宫内膜癌. 2022.
20. NCCN GuidelinesOvarian Cancer/Fallopian Tube Cancer/Primary Peritoneal Cancer. 2024. V1.
21. 中国临床肿瘤学会(CSCO). 卵巢癌诊疗指南 2023.
22. 中华妇科肿瘤学分会. 中国妇科肿瘤临床实践指南第7版 (2023): 卵巢癌.
23. 中国抗癌协会 (CACA). 中国肿瘤整合诊治指南: 卵巢癌. 2022.
24. Sedlis A, et al. Gynecol Oncol. 1999; 73(2):177-83.
25. Ryu SY, et al. Br J Cancer. 2014;110(2):278-85.
26. Peters WA 3rd, et al. J Clin Oncol. 2000;18(8):1606-13.
27. Creutzberg CL, et al. Int J Radiat Oncol Biol Phys. 2011;81(4):e631-8.
28. Ignatov T, et al. J Cancer Res Clin Oncol. 2016 Feb;142(2):489-95.
29. Kunos C, et al. Obstet Gynecol. 2009 Sep;114(3):537-546.
30. Reed NS, et al. Eur J Cancer. 2008 Apr;44(6):808-18.
31. Barney B, et al. Int J Gynecol Cancer, 2009, 19(7): 1232-1238.
32. Seagle BL, et al. Gynecol Oncol. 2017, 146(2): 254-262.
33. Malouf GG, et al. Int J Gynaecol Obstet, 2013, 122(1): 57-61.
34. 张宝玉, 等. 国际肿瘤学杂志. 2019; 46(11):699-704.
35. 中华医学会妇科肿瘤学分会. 子宫肉瘤. 2023.
36. de Boer SM, et al. Lancet Oncol. 2019 Sep;20(9):1273-1285.
37. Matei D, et al. N Engl J Med. 2019 Jun 13;380(24):2317-2326.
38. Rao YJ, et al. Gynecol Oncol. 2017 Sep;146(3):572-579.
39. McCormack M, et al. ESMO 2023. Abstract LBA8.
40. Mileshkin LR, et al. Lancet Oncol. 2023 May;24(5):468-482.
41. de Boer SM, et al. Lancet Oncol. 2018 Mar;19(3):295-309.
42. Jun jie Wang, et al. ASCO 2024. abstract#5514.
43. Ang Qu, et al. ASCO 2024. abstract#5527.
44. Ping Jiang, et al. ESMO 2023. 767P;
45. Monk B, et al. Presented at: 2022 International Gynecologic Cancer Society Annual Meeting; September 29-October 1, 2022; New York, NY. Abstract O001.
46. Lorusso D, et al. ESMO 2023. Abstract LBA38.
47. Yang Xiang, et al. ESMO GYN 2024. Abstract 23O.
48. ClinicalTrials.gov: NCT04214067.
49. Mario Arguello, et al. ASCO 2024. abstract#e17527.
50. Prashant Kumar, et al. ASCO 2024. abstract#e17531.
51. Genlai Lin, et al. ASCO 2024. abstract#e17507.
52. Shanshan Ma, et al. ASCO 2024. abstract#e17523.
53. YiMing Ma, et al. ASCO 2024. abstract#e17505.
54. ESMO GYN 2024. Abstract 23O.
55. Qianxue Wei, et al. ASCO 2024. abstract#e17509.
56. Fo-Ping Chen, et al. ASCO 2024. abstract#5533.
57. Ting Wan, et al. ASCO 2024. abstract#5512.
声明:
本资讯由默沙东医学团队支持,旨在用于医学专业人士间的学术交流,请勿随意转发或转载。文中相关内容不能以任何方式取代专业的医疗指导,也不应被视为治疗建议。医学专业人士对文中提到的任何药品进行处方时,请严格遵循该药品在中国批准使用的说明书。默沙东不承担相应的有关责任。
审批号:MI-PD1-6200-CN
过期日:7/7/2025
查看更多