查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





作者:复旦大学附属华山医院 包丽雯
高血压合并糖尿病并不是一道“加法题”,而是一道“乘法题”。
高血压合并糖尿病患者的治疗,选择具有心血管以及肾脏保护作用的降压药物十分重要,如血管紧张素转换酶抑制剂及血管紧张素受体阻滞剂、盐皮质激素受体拮抗剂等。
高血压及糖尿病是发生心血管疾病(CVD)的2个重要独立危险因素。当患者同时存在糖尿病合并高血压,他们发生CVD的风险及全因死亡风险比仅有糖尿病或仅有高血压的患者成倍增加,需要引起我们更多的重视及积极的干预[1]。
流行病学调查研究表明,胰岛素抵抗与糖尿病不仅会导致以肥胖为代表的代谢异常,并且这部分人群更易出现高血压、动脉硬化。在2型糖尿病的队列研究及随机对照研究中,我们不难发现,其中约70%左右合并存在高血压[2];然而,在高血压的临床研究中,合并存在2型糖尿病的比例约为30%~50%[1]。在李勇教授牵头的全国多中心横断面研究UPPDATE的数据分析中,在高血压患者中,合并糖尿病的比例大约为20.38%[3]。由此,我们推测在2型糖尿病中,以胰岛素抵抗为代表的一系列病理生理变化会对高血压发生、发展产生深远影响,也有专家提出糖尿病性高血压(diabetes-induced hypertension)这一定义[4]。
Framingham offspring研究曾在1933例基线无高血压的患者中,观察胰岛素抵抗与高血压发生、发展的关系,在4年随访期间,即使调整了BMI增加这一混杂效应,胰岛素抵抗与高血压发生、发展也呈显著正相关[5]。Jackson 心脏研究也发现,在黑人种族中,胰岛素抵抗与高血压发病及发展显著相关[6]。4701例人群的队列研究发现,糖耐量受损和2型糖尿病发生动脉硬化的风险远高于血糖正常者,而胰岛素抵抗通过增加动脉僵硬度,进一步导致高血压及CVD发生[7]。由此可见,以胰岛素抵抗为核心的病理生理改变是糖尿病性高血压的主要发生机制[4](图1)。

体内和体外的观察研究发现,胰岛素抵抗会诱导RAAS过度激活,使得血管阻力及动脉压力增加;RAAS过度激活也可以通过损伤胰岛素信号通路影响血压。血管紧张素Ⅱ及醛固酮水平的上调会增加丝氨酸磷酸化水平,使得P13K通路活性下降,导致内皮细胞一氧化氮合成与激活能力降低,抑制一氧化氮介导的血管舒张作用。此外,激活的RAAS通过上调SGK-1通路,增加血管内皮钠离子通道(EnNaC)的活性,促进动脉硬化与高血压发生、发展(图2)。在临床研究中,我们发现在糖尿病人群中使用AT-1受体阻滞剂和盐皮质激素受体拮抗剂可以降低糖尿病患者高血压的发病率。
图2 RAAS激活可通过多途径影响动脉硬化及血压
线粒体生物合成障碍、自噬能力降低、线粒体产能下降等线粒体功能异常是2型糖尿病的主要病理生理改变之一,其所导致的内皮细胞功能异常是高血压发生、发展的主要原因。此外,NADPH氧化酶激活也是过量氧化应激产物(ROS)产生的重要来源,胰岛素抵抗可诱导血管内NADPH氧化酶激活,后者导致过量ROS生成,促使内皮衍生-舒张因子和内皮衍生-收缩因子失衡,使得血管张力增加,过量的ROS也会通过减少NO产生,促进动脉硬化和高血压发生、发展。
因此,线粒体功能障碍和氧化应激是胰岛素抵抗和糖尿病状态下高血压发生、发展的重要机制之一。
如前所述,高血压与糖尿病是CVD的重要病因,选择具有心血管以及肾脏保护作用的降压药物十分重要。
目前,各临床指南一致推荐,应当使用血管紧张素转换酶抑制剂及血管紧张素受体阻滞剂作为糖尿病患者合并高血压的一线用药。
一项荟萃分析[8]发现,在2型糖尿病合并高血压和高血压前期的患者中,SGLT2i具有显著的降压疗效。这项荟萃分析纳入了2450例患者,与使用安慰剂相比,使用SGLT2i者其收缩压及舒张压(诊室血压)降幅分别为5.04 mmHg(95%CI:-3.79~-6.30,P<0.01)和1.67 mmHg(95%CI:-2.45~-0.89,P<0.01),其中恩格列净对降压幅度最大,并且其降压效果随着药物剂量的增加而增加。
此项荟萃分析还对SGLT2i对血压变异度的影响做了相关研究。研究人员分析发现,SGLT2i降低平均日间收缩压的幅度(-4.57 mmHg,95%CI:-3.71~-5.43,P<0.01)大于降低平均夜间收缩压的幅度(-2.8 mmHg,95%CI:-1.84~-3.76,P<0.01)。此外,在亚组分析中,发现达格列净5 mg qd治疗14天,可以将血压从非杓型转变为杓型血压,但由于样本缺失,分析病例较少,尚不能形成可靠结论。
为了研究恩格列净在合并高血压的2型糖尿病患者中的降压效果,Hans团队进行了一项随机对照研究,证实了恩格列净在此人群中的显著降压效果[9]。
研究纳入825例患者,随机给予安慰剂、恩格列净10 mg及恩格列净25 mg,通过24小时动态血压监测观察恩格列净的降压效果。在随访的12周末,与安慰剂相比,10 mg恩格列净组的平均收缩压降幅为-3.34 mmHg,(95%CI:-4.78~-2.09mmHg,P<0.001),25 mg恩格列净组的平均收缩压降幅为-4.16 mmHg(95%CI:-5.5~-2.83mmHg,P<0.001)。(图3)
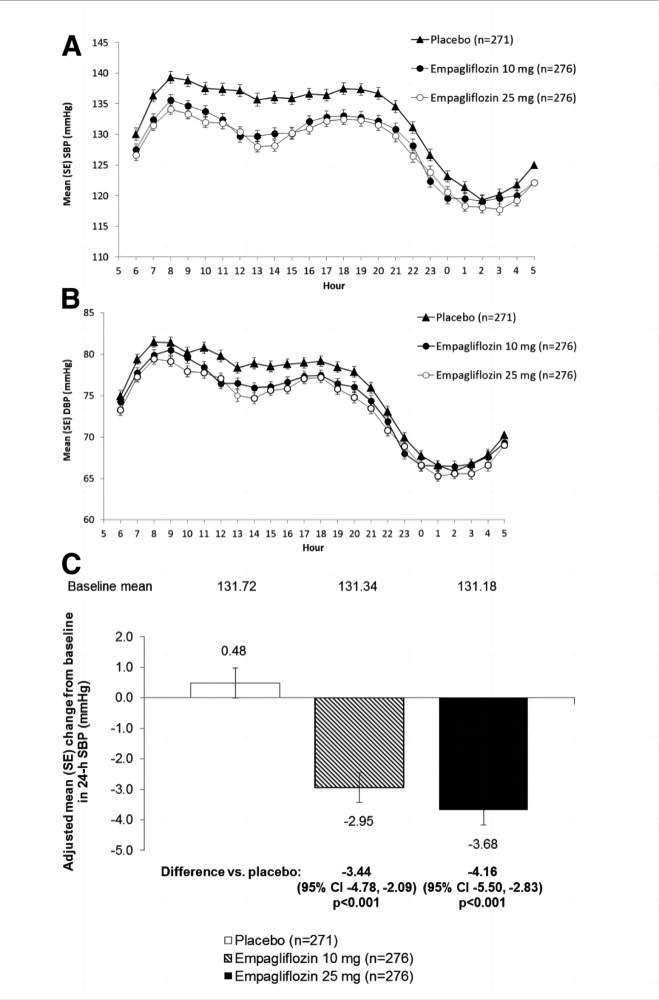
由此,我们不难发现,高血压合并糖尿病并不是一道“加法题”,而是一道“乘法题”。在我们理解了两者合并带来了更多的心肾风险,以及糖尿病性高血压以“胰岛素抵抗为中心”可能机制后,在高血压合并糖尿病患者中,我们应当采用临床证据更加充分的药物——血管紧张素转换酶抑制剂及血管紧张素受体阻滞剂、盐皮质激素受体拮抗剂、SGLT2i、GLP1-RA,来管理这部分患者,以期获得更好的心肾保护作用。
复旦大学附属华山医院心内科副主任医师 医学博士
国家紧急医学救援队队员
华山医院内科学上海市住院医生规范化培训基地秘书
中国高血压联盟理事,长三角心血管急重症联盟委员,中国微循环学会基层慢病管理委员会委员,第七届中西医结合心血管病委员会委员
2018—2019年参加哈佛大学医学院全球临床研究者培训
主持上海市科委、卫健委课题,参与国自然课题各1项
2018年获得科技部颁发的全国优秀微视频科普作品
2020年上海市住院医生规范化培训优秀带教老师
2021年复旦大学本科生“我心目中的好老师”提名
复旦大学优秀抗疫工作者,复旦大学优秀团干部等
下期预告:
超重/肥胖的中青年高血压患者的血压特点及管理方案
查看更多