查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





作者:中南大学湘雅二医院呼吸与危重症医学科 中南大学呼吸疾病研究所 湖南省呼吸与危重症疾病临床医学研究中心 湖南省呼吸疾病诊疗中心 张青 彭雅婷 彭红
近年来,间质性肺疾病发病率和患病率在全球范围内呈持续上升趋势,已成为严重威胁公共健康的重要慢性肺部疾病之一。今日呼吸特邀中国医学论坛报社呼吸与危重症编委会编委、华中科技大学同济医学院附属协和医院呼吸与危重症医学科主任马万里教授以“间质性肺疾病”为主题组稿,分享间质性肺疾病的前沿进展和诊疗经验,将在今日呼吸平台陆续更新。
肺纤维化(PF)是一种慢性、进行性肺部疾病,其主要特征是肺组织受损后不断修复过程中出现的异常纤维组织增生,导致肺部逐渐变硬、失去弹性,最终影响正常的气体交换功能。特发性PF(IPF)作为其中最典型、最具代表性的疾病,具有病因不明、不可逆、进展迅速等特点,诊断后中位生存期为2~4年。除肺移植外,尚无有效治愈方法。流行病学研究显示IPF发病率逐年上升,在欧洲和北美约为2.8~18/10万人年,目前已对全球130万人造成影响,给社会带来沉重的经济负担。
IPF的发生是多种细胞类型和信号通路共同作用的结果。肺泡上皮细胞在多种内外因素作用下反复损伤,继而异常激活并通过多种信号机制促进成纤维细胞活化,导致PF持续进展。其病理过程主要涉损伤阶段、肺泡炎症阶段和纤维化与过度修复阶段。2014年,抗纤维化口服药物吡非尼酮和尼达尼布被美国食品与药物管理局(FDA)批准用于治疗IPF。吡非尼酮通过调节或抑制分泌转化生长因-β(TGF-β)等来抑制成纤维细胞的生物学活性,减少细胞增殖和基质胶原合成,兼具抗炎和抗氧化作用,但易引起胃肠道不适和皮肤不良反应。尼达尼布通过阻断酪氨酸激酶抑制成纤维细胞增殖,主要副作用为腹泻等胃肠道反应。这两种药物只能延缓疾病进展,且价格相对昂贵,药物的可及性受限。
呼吸系统疾病除了常见的静脉或口服给药方式,还有一种简单且常用的局部治疗手段即吸入给药。与传统给药方式相比,吸入给药可使药物直接作用于肺部靶器官,具有起效迅速、疗效显著、全身不良反应少、患者依从性高等优势。研究显示,空气动力学中位直径(MMAD)为1~5μm的药物颗粒可沉积于较小直径的细支气管,而MMAD为1~2μm的颗粒则有可能到达肺泡区域。因此,药物通过吸入方式可直接进入肺泡,并在双肺内实现相对均匀的分布,从而达到良好的局部治疗效果。这为PF的靶向治疗提供了新的思路。目前,已有大量研究致力于探索吸入制剂在PF中的应用,以期突破现有治疗手段的局限。本文将围绕吸入治疗PF的研究进展进行综述与分析。
吸入装置在呼吸系统疾病治疗中至关重要,其通过物理方式将药物转化为微小颗粒或气雾,使药物直接作用于肺部,实现高效局部治疗。临床上常见的吸入装置有四种类型。
雾化吸入器适用于多种药物,可产生粒径<10μm的气溶胶,有效沉积于下呼吸道。智能化设计提升了患者依从性,广泛用于哮喘、慢性阻塞性肺疾病及囊性纤维化等疾病。但超声雾化器可能因产热影响药物稳定性,且雾粒较大,临床应用受限。
干粉吸入器(DPI)具有便携、操作简便等优势,颗粒直径控制在0.5~5.0μm,可直达肺泡区,绕过肝脏首关代谢,生物利用度高。然而,其给药剂量重复性较差,依赖患者吸气流速,可能影响疗效。
加压定量吸入器(pMDI)具有剂量准确、起效快的特点,能有效隔绝光、氧、水分对药物的影响,但使用时需患者精准协调按压与吸气,操作技巧要求较高,且装置性能易受环境条件影响。
软雾吸入器(SMI)释放气雾缓慢、持续时间长,几乎不需患者协调动作,操作简便,药物沉积效率高,常用于单剂量或多剂量递送,依从性良好。但目前市场产品有限,且成本较高,智能化多剂量装置仍在研发中。
近年来,吸入装置在肺纤维化治疗中的研究不断深入。例如,雾化吸入干扰素β(IFN-β)可显著提高治疗效率,抑制TGF-β诱导的人肺成纤维细胞迁移和肌成纤维细胞分化。美国得克萨斯大学药学院通过薄膜冷冻技术成功制备了吡非尼酮、尼达尼布及吗替麦考酚酯的干粉吸入固定剂量组合,显著提高了三者的空气动力学吸入性能。天津中医药大学以L-亮氨酸为辅料,通过喷雾干燥法制备了丹参素B干粉吸入剂,克服了其口服吸收差、生物利用度低的缺点,提高了病变部位的药物浓度,提升了对IPF的治疗效果。
另有研究显示,不同吸入装置吸入沙丁胺醇治疗IPF,药物血浆浓度不同。该研究结果提示需要不断优化吸入颗粒的物理特性和吸入器的设计与性能,以提高药物在IPF患者中的递送效率和治疗效果。
不同类型的吸入器在药物粒径控制、肺部靶向递送以及提升患者依从性方面各具优势,为PF的局部治疗提供了新思路。但吸入治疗在临床应用中仍面临药物沉积效率不均、肺部靶向性不足、黏膜刺激等挑战。目前的研究多聚焦于吸入装置的结构改良以提升药物利用率,但在应对IPF复杂病理环境下仍存在局限。目前,越来越多的研究正转向探索更为精确和高效的药物递送系统,以实现更优的药物释放控制、靶向定位和治疗效果。
药物递送系统(DDS)旨在安全地在体内运输药物并提高其有效性和安全性。将纳米材料应用于DDS中,不仅提升了药物在体内的生物分布特异性,还能实现对特定细胞甚至细胞器的精准靶向输送,显著提高药效并降低毒副作用,这种技术为精准医疗的发展提供了全新的解决方案。常见的几种纳米递送系统类型如表1所示。
表1常见的纳米递送系统类
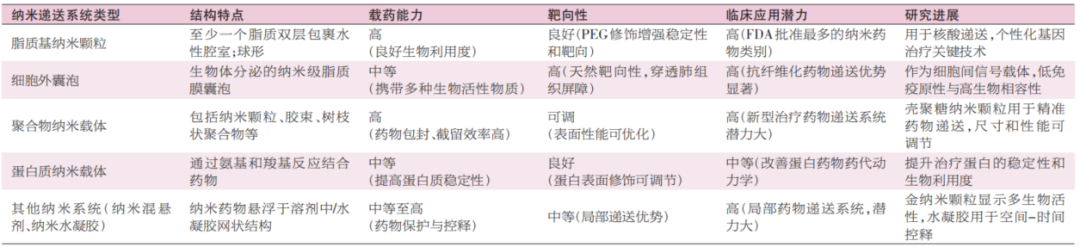
脂质基纳米颗粒脂质基纳米颗粒在PF治疗中应用广泛。韩国忠北国立大学药学院研制的吸入性吡非尼酮低共熔溶剂(DES)高载量纳米乳剂,其在SD大鼠中雾化吸入后,生物利用度和肺内分布优于口服或气管内滴注,可降低毒副作用。韩国成均馆大学开发了12μm可雾化微凝胶μGels,包含尼达尼布-聚乳酸羟基乙酸共聚物PLGA纳米颗粒和吡非尼酮脂质体,能抑制TGF-β诱导的肌成纤维细胞活化和(或)分化,抵抗小鼠肺泡巨噬细胞吞噬,保留时间更长。
国内研究者也在进行积极探索。江西中医药大学药学院设计的酸性敏感Nb-Lips,利用肺部酸性条件实现局部起效,磷脂双分子层可控制药物释放,解决频繁给药问题。中国药科大学药学院构建的双药负载纳米颗粒Lip@VP,通过薄膜分散法制备,将维替泊芬和吡非尼酮封装在脂质层内,借助雾化器递送至小鼠肺部,治疗两周后发现肺纤维化小鼠肺功能和组织结构有所改善。上海交通大学药学院开发的“LOOP”平台,用于肺部mRNA递送的吸入型脂质纳米粒(iLNP),其iLNP-HP08LOOP具有高辅助脂质比例和辅助雾化缓冲液,可有效递送编码白介素(IL)-11单链抗体的mRNA至小鼠肺部并表达IL-11scFv,显著抑制肺纤维化,且兼容商用ALC0315-LNP。
细胞外囊泡(EV)研究表明,人支气管上皮细胞衍生的EV可抑制TGF-β介导的肌成纤维细胞分化和肺上皮细胞衰老,效果优于间充质干细胞衍生的EV。乳源性EV可降低TGF-β1、Smad3和炎性细胞因子水平,在IPF小鼠模型中以低剂量有效减少纤维化发展并改善肺功能。外泌体作为EV的一种,粒径分布在30~200nm,可通过吸入肺球状细胞分泌体和外泌体重建正常肺泡结构,减少胶原蛋白积聚和肌成纤维细胞增殖,减轻博来霉素和二氧化硅诱导的纤维化,具有肺再生治疗潜力。这些研究结果表明,EV及其衍生物可能成为IPF治疗的新策略。
聚合物纳米颗粒聚合物纳米颗粒在PF治疗研究中展现出多样且有效的发展前景。拉希迪普尔(Rashidipour)等研究发现,装载在果胶/壳聚糖/三聚磷酸盐纳米颗粒上的百草枯除草剂可有效降低急性肺损伤和PF。李(Lee)等人发现,使用乳化扩散法制备的吸入性他克莫司负载壳聚糖包衣的PLGA纳米颗粒可显著减少炎症,他克莫司延长释放长达5d,且在肺部表现出良好的沉积率,是一种有效的持续释放型吸入系统。埃尔科米(Elkomy)等开发的非侵入性可吸入硝苯地平壳聚糖-PLGA聚合物纳米粒,包封率为61.81%,24h内持续释放率为50.4%,可调节博来霉素诱导的大鼠肺纤维化模型中的TGF-β/β-catenin通路。磷酸胆碱壳聚糖纳米粒作为递送平台治疗PF,可抑制TGF-β1诱导的成纤维细胞α-平滑肌肌动蛋白(SMA)表达,显著降低PF评分和胶原沉积,提高大鼠存活率。这些研究表明,聚合物纳米颗粒不仅可以有效地递送药物,还能通过多种机制调控纤维化过程,为PF的治疗带来新希望。
蛋白质纳米载体蛋白质纳米载体的创新发展为PF的靶向治疗注入了全新动能。徐(Seo)团队研发的可吸入白蛋白纳米颗粒,将抗纤维化药物他克莫司以85.3%±4.7%的高包封率负载于白蛋白纳米颗粒中,实现药物吸入后48h的肺部长效滞留,显著降低小鼠模型的纤维化病理损伤,展现出优异的安全性。山东大学研究者开发的双重功能化mRNA纳米递送系统,共负载基质金属蛋白酶13mRNA与角质形成细胞生长因子,突破单一疗法局限,可用于修复纤维化病变,促进PF病变中基质降解和肺泡上皮重建,为肺纤维化病变的结构性修复提供了多靶点协同干预策略。
其他多元化纳米递送策略的涌现,进一步丰富了PF治疗的干预手段,不同材料体系的设计均展现出针对纤维化病理特征的精准调控能力。赫马带(Hemmati)等人合成的纳米姜黄素,可降低总羟脯氨酸(HYP)含量,与口服和传统吸入姜黄素相比,纳米姜黄素更有效,副作用更少,炎症标志物水平降低更明显。另一项研究显示,合成的负载抗CD44伊马替尼金纳米颗粒,可抑制肺纤维化细胞的增殖和活性,减少肺泡巨噬细胞中IL-8的释放、M2的活力和极化。沙姆斯库(Shamskhou)等人创建的重组IL-10的水凝胶递送系统,打破了游离IL-10的半衰期限制,在吸入7d后,该制剂在预防和减少肺实质中的胶原沉积方面比游离IL-10明显更有效,可用于预防和逆转博来霉素诱导的PF。
综上所述,纳米类药物递送系统可提高抗纤维化药物的溶解度和生物利用度,增加靶细胞对药物的摄取,提高肺沉积速率,延长体内保留时间并改善药代动力学行为,显著增强低剂量抗纤维化药物的治疗效果并减少副作用,为临床治疗IPF提供了新思路。然而,纳米制剂仍存在安全性问题,如引起局部炎症和细胞因子风暴等。吸入药物的递送对暴露时间、剂量、浓度、粒径、表面积和电荷等因素要求高,这些因素与纳米毒性密切相关。但随着研究的深入,这些问题有望逐步优化和解决,从而进一步提升纳米药物递送系统的安全性和有效性。
AvalynPharma公司开展的一项雾化使用吡非尼酮AP01的Ⅰb期临床试验(NCT06329401)发现,向91名患有IPF的参与者施用AP01(50mgqd和100mgbid),结果显示,100mgbid剂量在48周的治疗中肺功能较为稳定。与口服吡非尼酮相比,AP01耐受性良好,全身不良事件较少。不良事件一般为轻度,最常见的是轻度咳嗽,目前正在开展2b期相关实验。据AvalynPharma官网显示,吸入用尼达尼布AP02已在健康成人志愿者和IPF患者中完成了单次给药剂量递增(SAD)和多次给药剂量递增(MAD)Ⅰ期临床试验,结果显示在所有剂量水平下,AP02都具有安全性且耐受性良好。完整的安全性、耐受性和药代动力学数据于2025年5月的美国胸科学会国际会议上公布且公司计划将AP02推进到IPF患者的Ⅱ期临床研究。
由于上述试验结果显示AP01和AP02可显著减少或消除口服吡非尼酮和口服尼达尼布的不良反应,AvalynPharma公司正在筹备开展吡非尼酮和尼达尼布的固定剂量复方制剂AP03用于吸入气雾剂肺部给药。这显示出吸入给药治疗的巨大潜力。
吸入给药在肺纤维化治疗中展现出显著优势和广阔前景,但仍面临诸多挑战与发展机遇。在技术层面,未来需进一步提升吸入装置的性能,研发智能化设备,实现对药物颗粒大小、分布及释放速率的精准调控,从而提高药物在肺部的沉积效率,减少口咽部沉积引发的不良反应。在药物递送系统方面,纳米载体的研究将迈向更深层次。一方面,应持续探索并优化脂质基、聚合物基等新型纳米材料设计,解决载药量不足和靶向性有限等难题;另一方面,应深入挖掘细胞外囊泡等生物源性载体在肺纤维化微环境中的作用机制,实现抗纤维化药物的高效且特异性递送。
此外,基因编辑和mRNA技术的结合,推动以雾化吸入为途径的基因治疗策略的开发,有望从根本上干预肺纤维化进程。在临床研究方面,应加快推动雾化吸入药物的临床试验,扩大样本规模和延长观察周期,全面评估其长期疗效与安全性,尤其关注不同疾病阶段和病理类型患者的治疗反应差异。同时,积极开展联合治疗研究,探索雾化吸入药物与免疫调节、干细胞治疗等其他疗法的协同效应,力求为肺纤维化患者提供更为优化的综合治疗方案。
随着材料科学、纳米技术、生物医学工程与临床医学的多学科融合发展,雾化吸入给药有望成为攻克肺纤维化的关键突破口,为改善患者生活质量、延长生存期带来新的希望,推动肺纤维化治疗领域取得重要进展。
本文由中国医学论坛报社呼吸与危重症编委会编委、华中科技大学同济医学院附属协和医院马万里教授组稿
查看更多