查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过






神经保护是缺血性卒中治疗的基本策略之一。既往,全球神经保护剂研发裹足不前,鲜有成功。针对这一现状,在美国成立了卒中治疗学术产业圆桌会议(Stroke Treatment Academic Industry Roundtable,STAIR),就急性缺血性卒中临床试验研究研发标准定期进行商榷探讨,该组织过去进行了11次大型会议(图2),撰写了11项神经保护相关的专家共识,指导神经保护相关研究并取得了重大进展。
STAIR之所以能够成功,在于其大胆做了三项突破性假设:①应将神经保护剂的临床前研究修订为临床前试验,并设定Ⅰ、Ⅱ、Ⅲ期。其中Ⅲ期临床前试验要求设计样本量足够大的多中心、盲法、随机对照、前瞻性研究,最大限度地模拟真实临床环境。②神经保护治疗需与再灌注治疗相结合,以保证药物能够顺利进入缺血部位从而发挥作用。③神经保护剂必须是具有多靶点治疗作用的药物。在STAIR原则指导下,近期神经保护研究取得哪些重大进展呢?
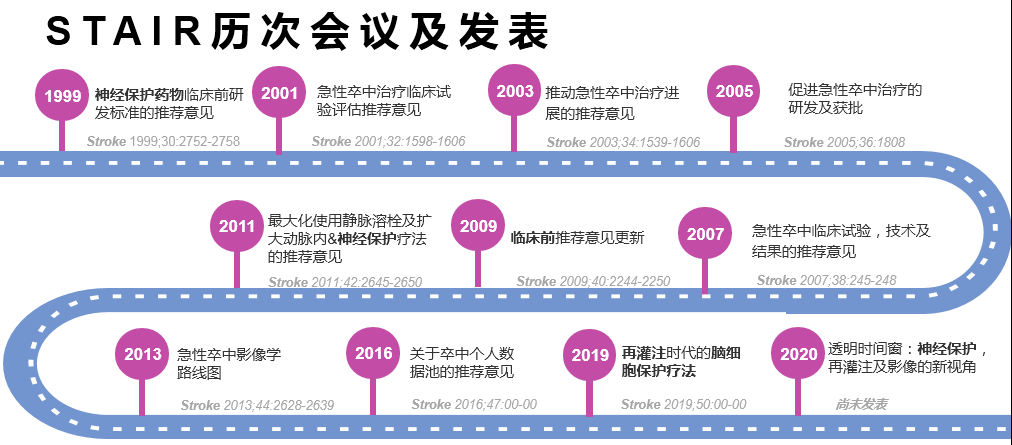
△ 图2 STAIR历次会议及发表
01
基于STAIR原则一:临床前双中心试验证明远隔缺血适应的神经保护作用
RIC(远端缺血适应)是一种通过对器官/组织进行短暂缺血和再灌注来保护远端器官(心脏或大脑)免受随后缺血性损伤的方法。一项双中心、随机、双盲设计的临床前试验显示,RIC显著减少了短暂性大脑中动脉闭塞(tMACO)大鼠的梗死体积,以中位数(四分位间距)表示,对照组vs RIC组=19%(8%~32%)vs 40%(17%~59%)(p=0.028)。校正基线时ADC序列上的病灶大小后,经多因素分析显示差异仍然显著。此外,RIC可显著降低tMCAO大鼠的神经功能评分(评分越高,神经功能缺损越重):对照组vs RIC组=6(3~8) vs 9(7~11)(p=0.032)。
02
基于STAIR原则二:加拿大ESCAPE-NA1研究开启神经保护大门
溶栓/取栓的再灌注治疗已成为各国指南的推荐首选。以往动物研究提示神经保护药物可能需要与再灌注治疗联合,才能发挥理想疗效。
ESCAPE-NA1是一项多中心、随机、双盲、安慰剂对照、平行组、单剂量设计研究,是基于桥接取栓的ESCAPE研究进行的,评估神经保护与再灌注治疗结合对于神经功能预后的影响。该研究纳入来自8个国家、48家中心的1105例缺血性卒中患者,入组患者均由发病12小时内的大血管闭塞所致。所有患者均接受血管内治疗,符合静脉溶栓标准的患者按常规流程进行阿替普酶溶栓治疗,血管内治疗时,随机接受静脉Nerinetide(NA-1)或安慰剂。主要终点为随机化后90天时良好功能预后(mRS 0-2)的患者比例,次要终点为神经功能缺损评价(NIHSS评分)、日常生活功能独立性(改良Barthel指数,mBI),很好的功能独立性(mRS 0-1)比例及死亡率。
针对所有人群的分析结果显示,试验组与对照组主要及次要终点均无统计学差异,主要终点(mRS 0-2)比例为61.4% vs 59.2% (调整RR 1.04, 95% CI 0.96–1.14; p=0·35)。未接受阿替普酶(tPA)治疗的患者中,NA-1组患者良好功能预后的比例显著高于对照组(59.3% vs 49.8%,RR 1.19,95%CI 1.01~1.41);梗死核心体积更低(中位数26.7 mL vs 39.2 mL);90 d内死亡率显著降低(12.8% vs 20.3%,RR 1.13,95%CI 0.88~1.45,p=0.0330)。
虽然ESCAPE-NA1研究并未得到阳性结果,但该研究对未进行阿替普酶静脉溶栓的亚组分析后得出的阳性结论为神经保护剂带来了新的曙光,即直接取栓时应用神经保护剂可能为患者带来更良好的预后。这提示,NA-1仍有望成为缺血性卒中后的神经保护药物之一。
为解决直接取栓治疗中应用神经保护剂是否有效,该团队启动了Ⅱ期临床试验——REPERFUSE-NA1,一项前瞻性、多部位、观察性的影像学研究。作为ESCAPE-NA1的子研究,共计划纳入150例AIS患者,在行血管内治疗前未行阿替普酶溶栓,仅静脉给予NA-1治疗。主要结局指标:早期影像学梗死进展;次要结局指标为90d的卒中延迟性继发损伤发生率。该研究于2020年启动,是未来几年神经保护剂研究领域最值得期待的研究之一!
03
基于STAIR原则三:中国TASTE研究成为多靶点神经保护的应用典范
卒中病理过程复杂,涉及靶点众多,这提示神经保护剂最好是具有多靶点治疗作用的药物。TASTE研究一项中国本土探讨神经保护、新的突破性研究。全国48家临床中心参与,共纳入1200例受试者。本研究采用优效性设计,以评估依达拉奉右莰醇注射液治疗急性缺血性卒中(AIS)疗效是否优于依达拉奉单药。主要疗效终点为治疗第90天mRS评分≤1分的患者比例。次要疗效终点为:治疗第90天时mRS评分,治疗第14天NIHSS评分相比基线时的变化;治疗第14、30、90天时NIHSS评分0-1的比例、日常生活活动能力评分(ADL) ≥ 95分的比例、MoCA评分;治疗第90天脑卒中影响量表(SIS)评分。预先设定年龄、性别、既往卒中史和治疗距发病时间对主要疗效进行亚组分析。
结果显示,与依达拉奉对比,依达拉奉右莰醇以1.42的优势比(OR)显著提高了AIS患者第90天功能独立的患者比例。次要疗效终点:治疗第14天NIHSS评分较基线减少值,依达拉奉右莰醇组显著高于依达拉奉组;安全终点,两组之间不良事件及严重不良事件没有显著性差异;亚组分析结果显示:治疗与性别存在显著的交互作用,依达拉奉右莰醇组在女性中的获益似乎更明显。
过去,由于多个神经保护药物连续在临床阶段试验得到阴性结果,给研发和临床带来巨大打击,甚至出现对“神经保护”整个领域及策略的根本怀疑。在STAIR策略指导下,临床前试验更为规范,TASTE研究取得阳性结果,ESCAPE-NA1在不使用tPA的亚组中得到阳性结果,这为全球神经保护药物研发事业注入了一剂兴奋剂,让人们看到了重启神经保护大门的希望!
来源:天坛会(首都医科大学附属北京天坛医院 王拥军教授报告整理)
查看更多