查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





点击阅读
病例1
一般情况:患者,男性,30岁,终末期尘肺。
现病史:2018年11月30日,于我院在气管插管全麻下行双肺移植术,术后第4天返回普通病房。2018年12月5日,查BALF结核分枝杆菌X-pert阳性,BALF抗酸杆菌涂片阳性,予左氧氟沙星、异烟肼、乙胺丁醇、吡嗪酰胺四联抗结核。2018年12月15日,患者出现发热,体温最高38.5℃,反复CRAB培养阳性(BALF),多黏菌素B+替加环素或舒巴坦抗感染治疗,患者热退、白细胞恢复正常,考虑治疗有效,但患者出现头面部麻木症状。2018年12月23日,出现呼吸、心跳骤停,考虑多黏菌素B引起呼吸骤停。因患者感染重,停用霉酚酸酯类抗排异药,予他克莫司及甲泼尼龙抗排异治疗。
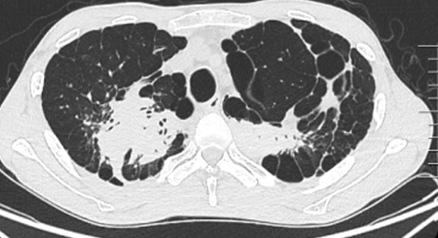
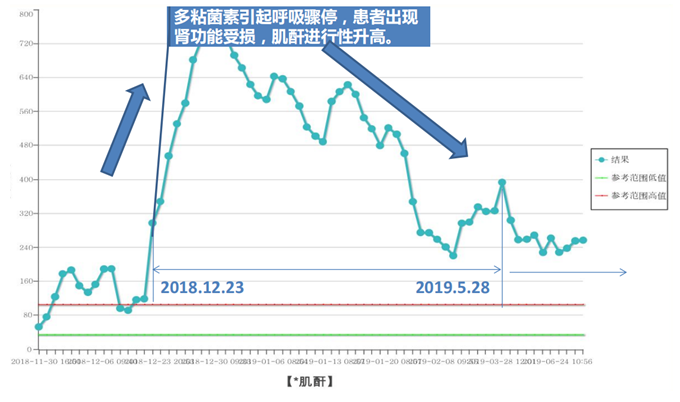
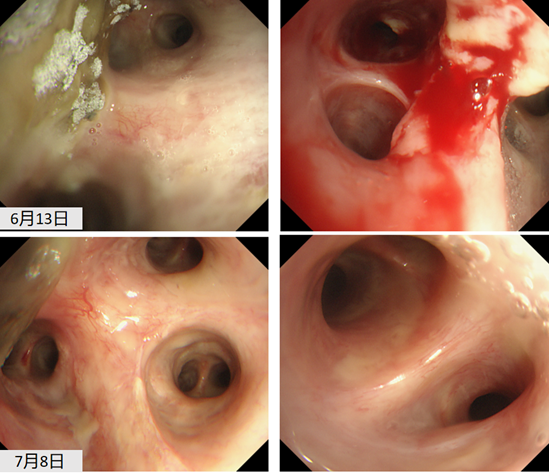
患者存在多黏菌素B引起的肌酐升高。肺移植后半年,间断调整免疫剂抑制剂。半年复查时,肾功能持续减退,eGFR基本上维持在25 ml/(min·1.73m2)左右。2019年5月28日,有咳嗽、咳痰症状,胸部CT可见双肺尤其右肺分布为主的树芽征。2019年6月12日,出现痰中带血丝。2019年6月13日,支气管镜检查可见吻合口良好,支气管黏膜出现霉斑、白膜。2019年6月17日,黏膜活检大量炎性坏死物中可见曲霉菌。
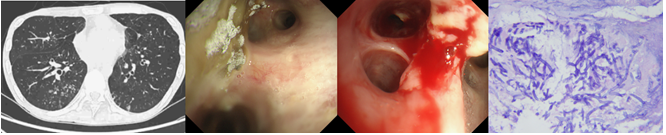
确诊:TBA。临床诊断为IPA。
据ISHLT对肺移植术后曲霉感染的推荐策略,虽然不常规推荐联合应用。但考虑患者同时合并了TBA和IPA,感染较重,遂采取了伏立康唑和米卡芬净的联合治疗策略,疗程为2个月。
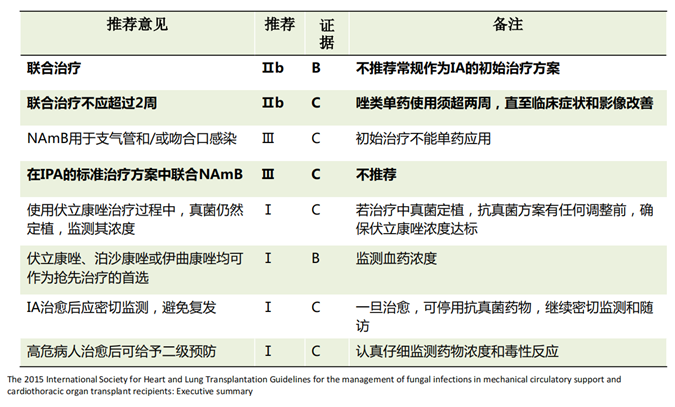
治疗期间对伏立康唑进行了治疗药物监测(TDM),尽量使其浓度保持在需求范围内。
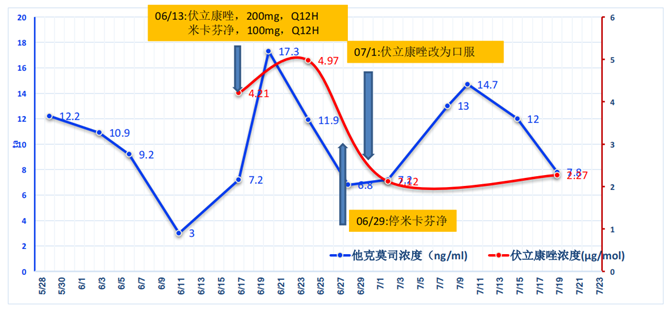
此时面临着一个非常重要的问题,即免疫抑制剂的调整。因为患者肾功能不全,所以将他克莫司改为西罗莫司。患者肾功能有所恢复,肌酐清除率有所上升。考虑长期治疗的问题,结合患者当时的情况,将抗排异药物由西罗莫司调整为他克莫司,同时继续给予伏立康唑治疗IPA。
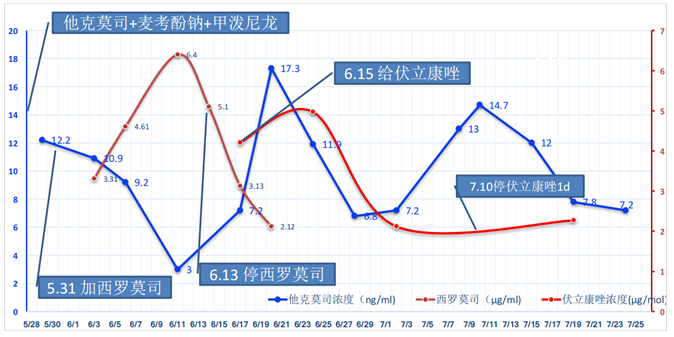
经过上述治疗后,支气管镜下可见霉斑和出血坏死明显好转,时长将近1个月,总疗程约3个月。该患者目前是术后3年,随访生活质量较好。
病例2
一般情况:患者,女性,40岁,氧化铝厂工人,BMI 21.5 kg/m2。15年前开始有“铝粉”接触史,无规范防护措施,5年前停止接触。
主诉:活动后气短5年,加重1年,双下肢水肿4个月。
术前病史:5年前无明显诱因出现气短,活动后明显,于当地诊断为“尘肺”。此后气短症状进行性加重,初仅爬2~3楼后出现,逐渐表现为平路稍快走即出现气短。1年来平均每2个月住院1次,每次给予醋酸泼尼松口服(35 mg/d,每2周减量10 mg,服药约1个月后停药)。利尿、西地那非降肺动脉压,家庭氧疗。4个月来气短症状进一步加重,需持续氧疗,双下肢水肿,伴少尿、纳差、反酸、烧心、腹胀等症状。
胸部CT:双侧胸膜弥漫性磨玻璃影,支气管扩张,肺动脉极度增宽。患者是因长期尘肺导致重度肺动脉高压和心功能不全。
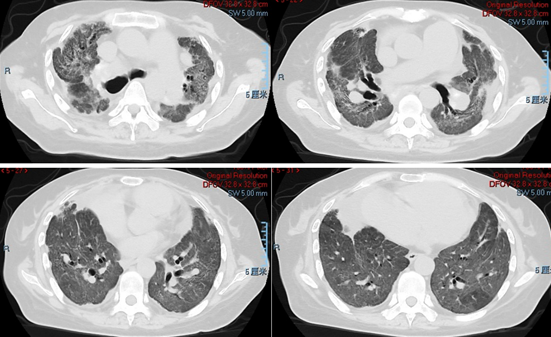
术前肺功能评价:患者术前肺功能提示限制性通气功能障碍、重度弥散功能障碍。
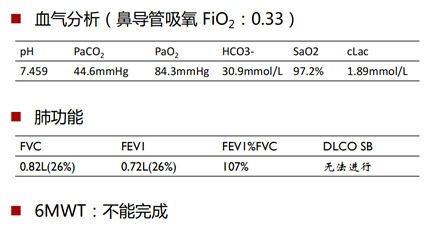
术前心功能评价:心电图示右室肥大,BNP升高(931.8 pg/ml);心脏超声示右室壁运动减低,呈D字征。右心导管提示肺动脉平均压已达43 mmHg,提示肺心病非常严重。
手术评估:
手术指征:诊断“尘肺(氧化铝)”明确,病变类型不可逆,合并呼吸衰竭、肺动脉高压、右心衰竭,符合肺移植指征,完善心肺、肿瘤、感染、免疫等方面评估无禁忌证,于2010年12月24日在VV-ECMO辅助下行双肺移植术。
术前情况:鼻导管吸氧4~5 L/min,SpO2 90%~95%;针对原发病,给予甲泼尼龙15 mg qd;针对心功能不全,给予西地那非20 mg tid、托拉塞米10 mg qd、螺内酯20 mg qd、地高辛0.125 mg qd、那曲肝素0.4 ml。
手术情况:
手术时间:7小时50分钟。
循环:出血1500 ml,尿量2200 ml,入量8500 ml。
术中循环障碍:血压最低70/45 mmHg,去甲肾上腺素[0.5~1.0 μg/(kg·min)]、肾上腺素[0.05~0.10 μg/(kg·min)]、米力农泵入。
移植肺冷缺血时间:R 295 min,L 500 min。
免疫诱导:巴利昔单抗20 mg+甲泼尼龙750 mg。
术中预防用抗生素:头孢哌酮舒巴坦。
术后情况:
(1)原发性移植物功能不全(PGD)1~2级,心功能不佳,利尿脱水困难,CRRT脱水治疗。术后第3天撤除VV-ECMO,第4天拔除气管插管,序贯NIPPV。由于患者术前合并重度肺动脉高压和左心功能障碍,故术后最突出的问题是心源性休克,我们采取了多种治疗手段,最终使其逐渐恢复。术后1.5个月,患者出院。首次出院时,基本可以恢复正常生活,常规抗排异和预防感染,肺功能有所恢复,此时主要症状是胃肠道反应,并无太多呼吸道症状。出院前复查胸部CT可见肺野比较清晰。
(2)术后3个月再次复查,右上肺新发结节,双肺较多弥漫磨玻璃影。
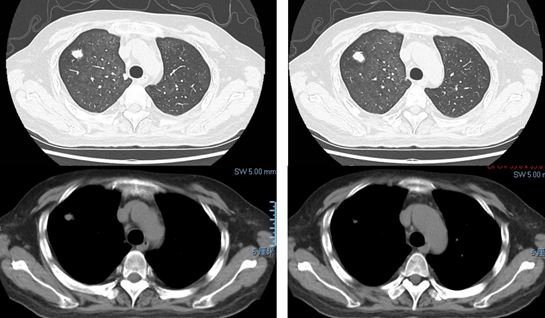
无发热、咳嗽、咳痰、咯血、胸痛、呼吸困难等症状;双肺未闻及干/湿啰音,下肢轻度水肿,心腹无其他异常。感染指标正常。细胞免疫和体液免疫功能低下,同时合并心肾功能不全。对于常规心肾功能不全,采取利尿和肾脏保护治疗。
(3)支气管镜下可见轻度充血,无明显脓性分泌物。
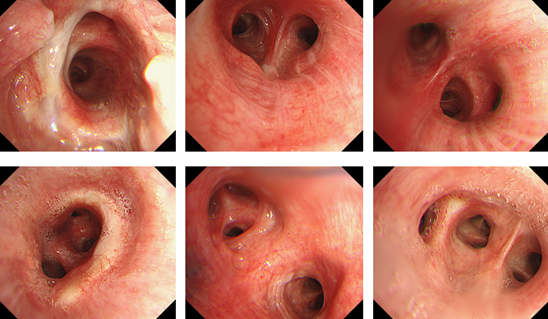
(4)BALF病原学:细菌培养鲍曼不动杆菌;真菌涂片可见丝状真菌;未培养出真菌;BALF GM 0.6;病毒、抗酸涂片Gene-Xpert、T-SPOT、结核抗体、PPD试验、隐球菌抗原均阴性,给予左氧氟沙星治疗2周。(5)影像学:病变进展,结节仍在生长,同时在右上肺后段又出现新发结节。(6)行CT引导下穿刺同时送病理,病原可见丝状真菌,考虑帚霉可能。病理提示两端肺泡结构消失,增生的纤维组织内可见大量中性粒细胞浸润,脓肿形成,小血管增生,组织细胞聚集,可见灶状坏死,特殊染色PAS、银染可见阳性真菌。
治疗情况:根据实体器官移植感染治疗策略,评估患者处于免疫高风险还是免疫低风险阶段。该患者目前属于免疫低风险,但感染问题较为突出(确诊帚霉肺炎),遂停用霉酚酸酯类药物,同时加用丙种球蛋白,加强免疫功能调节;针对帚霉肺炎,采取三联治疗,米卡芬净150 mg qd,2周;泊沙康唑200 mg q6h+特比萘芬250 mg qd,3个月。
随访:用药2周后,病变缩小,但不明显;用药1个月后,病灶明显缩小;用药3个月后,上肺后段结节消失,上肺间段的结节明显缩小。治疗效果较好。
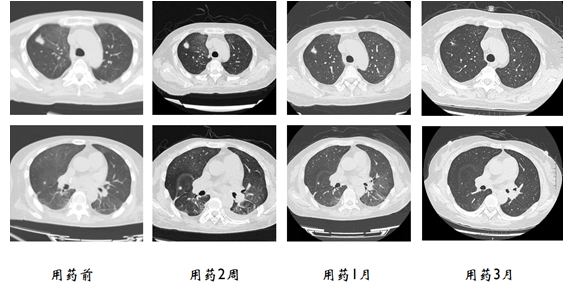
帚霉感染以呼吸困难为主要临床表现,其危险因素可能与既往真菌感染和系统抗真菌治疗有关。
肺移植术后真菌感染仍有很多问题亟待解决,包括如何防控IFD、如何选择和界定普遍预防/抢先治疗方案、哪类患者适合普遍预防/抢先治疗、肺移植BALF GM的cut off值以及耐药真菌防控策略等,这些问题仍需要我们深入探讨。
作者:中日友好医院 陈文慧
本文转发自重症肺言
查看更多