查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





结直肠癌(CRC)是我国年发病率第二、年死亡率第五的恶性肿瘤[1]。虽然基于肠镜技术的CRC筛查显著降低了晚期疾病的发生率,然而,针对CRC的新药研发却未能像非小细胞肺癌(NSCLC)那样不断涌现乐观的成果。从分子生物学角度而言,CRC与NSCLC均存在多类分子生物学标志物,而NSCLC如今已成为分子生物学标志物指导下的精准治疗典范。相比之下,CRC的精准药物治疗仍在演进过程中,从早期病灶位置(左半vs右半),到RAS/BRAF突变状态,再到微卫星不稳定水平(MSI),不同药物治疗方案的最佳获益人群不断被明确[2]。然而,现阶段以驱动基因为靶点的CRC靶向药物较为缺乏。
NTRK融合突变是由NTRK1/2/3基因3'端与伴侣基因5'端形成的嵌合基因,导致TrkA、TrkB、TrkC受体下游PI3K、RAS/MAPK/ERK等介导细胞存活、增殖的信号通路组成性激活,进而导致癌症发生[3]。针对NTRK融合的靶向药物因其出色疗效已获批用于无瘤种限制的实体瘤临床治疗[4,5]。NTRK融合往往富集于罕见癌种,如婴儿型纤维肉瘤、小儿先天性中胚层肾瘤以及分泌性乳腺癌等。然而,在NSCLC和CRC等常见瘤种中,NTRK融合的检出率<1%[6]。因此,在使用NTRK-TKI治疗CRC前,需要使用准确的伴随诊断检测。
目前可用于NTRK融合的检测方式主要有免疫组化(IHC)、荧光原位杂交(FISH)、基于DNA或RNA的二代测序(NGS)等,这些方法存在各自优势及局限性。那么,在CRC的临床实践中该如何选择NTRK的检测方式?
为了解答这一问题,南京大学医学院附属鼓楼医院病理科樊祥山教授团队开展了一项中国人群队列研究[7],在CRC人群中考察了3类NTRK融合检测方式 (IHC、FISH、NGS)的性能,并制定了兼顾检测准确性与经济性的筛查、诊断流程建议。
【解读专家】
樊祥山 教授
南京鼓楼医院主任医师
江苏省病理质控中心主任,南京市病理质控中心主任
医学博士
中华医学会病理学分会青年委员会副主任委员
中国抗癌协会肿瘤病理专委会常务委员
食管癌学组副组长及中国肿瘤结构化病理报告规范项目执行秘书长
中国抗癌协会淋巴瘤专委会委员
中华医学会病理学分会淋巴造血学组委员
美国MD Anderson癌症中心血液病理科访问学者
中国医师协会病理科医师分会委员
中国临床肿瘤学会(CSCO)肿瘤病理专家委员会委员
江苏省医学会病理学分会副主任委员,消化疾病学组组长
中国合格评定国家认可委员会(CNAS)ISO15189医学实验室技术评审员
教育部学位中心评审专家
第三届中国杰出青年病理医师和江苏省六大高峰人才获得者
《中华病理学杂志》和《中华消化内镜杂志》等杂志编委
主持国家、省市级课题9项
近5年以第一/通讯作者发表论文46篇
研究概述
研究纳入819例未经选择的、接受手术切除的CRC患者,该队列中受试者临床分期、分级、错配修复蛋白(MMR)表达情况、KRAS/NRAS/BRAF突变状态等信息均可获取。研究利用手术样本,基于三种方式检测NTRK融合:
IHC:pan-Trk抗体检测;
FISH:基于NTKR1/2/3设计双色断裂探针,即NTKR1/2为5'端红色探针及3'端绿色探针,而NTRK3为5'端绿色探针及3'端红色探针。因为NTRK的TK区均在3'端,所以除了典型的1R1G1F信号模式之外,对NTRK1/2来说1G1F为阳性,对NTRK3来说1R1F为阳性;
NGS:基于RNA(ArcherDx)或DNA(ION TORRENT)NGS检测平台。
主要研究结果
3种NTRK融合模式及分布
根据NTRK融合包含Trk TK结构域的完整性,可将NTRK融合方式分为3种方式:
经典型:包含完整TK结构域,对靶向治疗有效;
亚经典型:包含部分TK结构域,靶向治疗疗效未知;
非经典型:TK结构域丢失,对靶向治疗无效。
因此,预测NTRK-TKI有效性,需要明确区分NTRK融合具体模式。
将基于RNA的NGS检测作为NTRK融合“金标准”,该研究共检出13例NTRK阳性(1.59%),其中包括5例经典型(TPM3-NTRK1 2例, TPR-NTRK1、5'-telomere-NTRK1、ALLC-NTRK3各1例),6例亚经典型、2例非经典型。
3类检测方法一致性结果:FISH较IHC更为灵敏,但局限性仍存
研究中的819例CRC患者,IHC检出10例NTRK融合阳性,FISH检出13例NTRK融合阳性。然而,利用RNA-NGS对两者检测结果进行核验时发现:
10例IHC阳性检出患者中仅6例为RNA-NGS阳性;
13例FISH检出阳性患者中12例为RNA-NGS阳性。
根据IHC、FISH不同阳性判定方法,可对以上结果进行更为深入的解读。
IHC的pan-Trk阳性染色判定有以下3种情况:
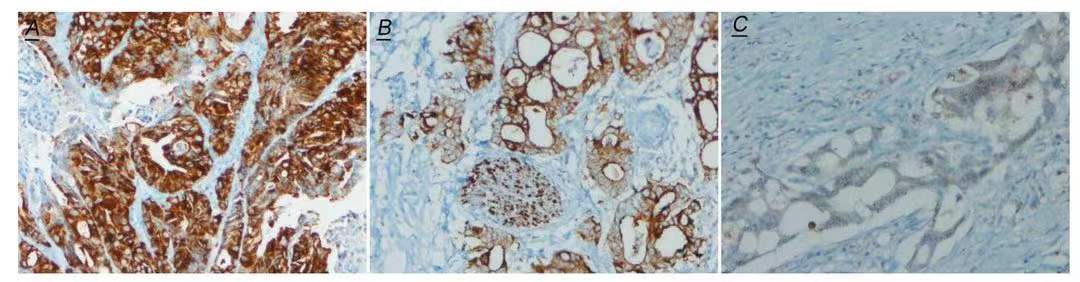
A. 细胞核阳性染色(n=5):NGS检测发现,其中3例经典型,1例非经典型,1例为NTRK融合阴性;
B. 核膜阳性染色(n=1):NGS检测确认为NTRK融合阴性;
C. 弥散性细胞质染色(n=4):1例经典型,1例亚经典性,2例NTRK融合阴性。
由此可见,IHC阳性染色判读NTRK融合灵敏度低;细胞核阳性染色优于细胞质阳性染色。同时,不同panTrk克隆号之间的染色结果很可能有所差别。
FISH双色探针判定的阳性染色有3种情况:

D. 双色断裂(“红-黄-绿”):共6例;
E. 单红:共4例;
F. 单绿:共3例,其中有一例经FISH检查NTRK1为单绿信号,但经NGS证实为NTRK融合阴性。
FISH阳性结果判读NTRK融合局限性在于,无法准确区分经典、亚经典、非经典融合模式。
利用MLH1/PMS2提升NTRK检测准确性
通过考察NTRK融合人群的分子生物学标志物发现,46.15%(6/13)存在MLH1/PMS2丢失,这意味着NTRK融合CRC患者存在明显的DNA错配修复缺陷。
单独考察经典型NTRK融合人群发现,5例患者中均存在MLH1/PMS2缺失;而6例亚经典NTRK融合中仅1例为MLH1/PMS2缺失。
上述结果提示,经典型NTRK融合富集于MLH1/PMS2缺失人群。
研究者建议的CRC患者NTRK临床筛检流程
IHC虽然检测灵敏度低,但简单易行,成本低;FISH检测灵敏度高,但无法分辨经典型NTRK融合;NGS检测虽然是金标准,但检测成本高,可及性较低。
综合考虑各检测方式的优缺点和检测资源可及性,并利用MLH1/PMS2缺失对于经典型NTRK融合的富集效应,研究者提出以下CRC患者NTRK融合筛检路线:
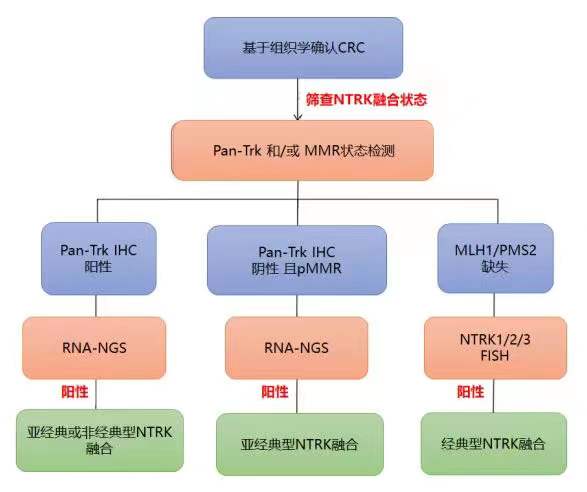
讨论
该研究中CRC人群NTRK融合检出率(1.56%)高于以往研究[6],可能原因是该研究将经典型、亚经典、非经典型NTRK融合均计入NTRK融合阳性;如若仅计算5例经典型NTRK融合,则CRC阳性检出率为0.61%,与以往研究相一致。但从临床意义而言,经典型NTRK融合对于靶向治疗人群的筛选更具临床意义。
欧洲内科肿瘤学会(ESMO)2019年发布了NTRK融合检测的临床实践推荐意见[8]。在该文件中,CRC等并非NTRK融合高阳性率瘤种,推荐的一线检测手段为NGS。虽然RNA-NGS为NTRK融合检测金标准,但NGS技术门槛、检测成本、平台与资源分布等问题为我国CRC人群的广泛检测设置了障碍。本研究充分考虑了检测成本、可及性与检测结果的准确性,在NTRK筛查、确认检测不同环节设置了灵活的可选方案,更具临床可实践性及可推广性。
另外,RAS/BRAF以往被认为在CRC中是具有治疗指导意义的分子标志物,在本研究中未能呈现出与NTRK融合状态的相关性。然而,与MMR缺陷相关的MLH1/PMS2缺失则呈现出经典型NTRK融合的富集效应,提示MLH1/PMS2缺失有望成为富集经典型NTRK阳性CRC患者的潜在分子标志物。
参考文献:
1.World health organization, GLOBOCAN 2020: China
2.CSCO 结直肠癌诊疗指南,2021
3.Gatalica Z, et al. Mod Pathol. 2019 Jan;32(1):147-153.
4.
5.
6.Forsythe A, et al. Ther Adv Med Oncol. 2020 Dec 21;12:1758835920975613.
7.Fu Y et al. Front Oncol. 2021 Apr 29;11:669197.
8.Marchio C, et al. Ann Oncol. 2019 Sep 1;30(9):1417-1427.
查看更多