查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





岁聿云暮,华章将启。当2025年的时间卷轴缓缓收束,消化内镜及消化系疾病领域在临床研究与实践探索中留下了诸多坚实足迹,新技术的涌现、新理念的更迭以及循证医学证据的不断累积,正在深刻重塑着我们对疾病的认知与临床实践决策。
为了帮助广大临床医生系统梳理学科脉络,准确把握前沿进展,《中国医学论坛报》年度盘点栏目特别邀请了消化领域各亚专业的领军专家,对2025年度的临床研究进展进行深度回顾与总结。
超声内镜(Endoscopic Ultrasound,EUS)在消化系统疾病的诊断与治疗中发挥着重要作用,其在扫查胆胰管和识别胰腺较小的实性病变方面具有独特的优势;特别是EUS引导下细针穿刺技术的发展可以更好地完成疾病组织病理学诊断。此外,EUS引导的治疗技术,已经成为胰腺神经内分泌肿瘤、胃静脉曲张出血、严重急性胆囊炎、恶性远端胆管梗阻、胃流出道梗阻的重要治疗手段;尤其适用于传统治疗效果不佳或手术风险较高的患者。为此,《中国医学论坛报》特邀中山大学附属第一医院丁震教授团队对EUS在消化系统疾病诊治中的最新进展(主要包括指南、共识意见及高水平的多中心研究)进行总结盘点,希望能够让读者对EUS技术的最新进展有更清晰和深入的了解。
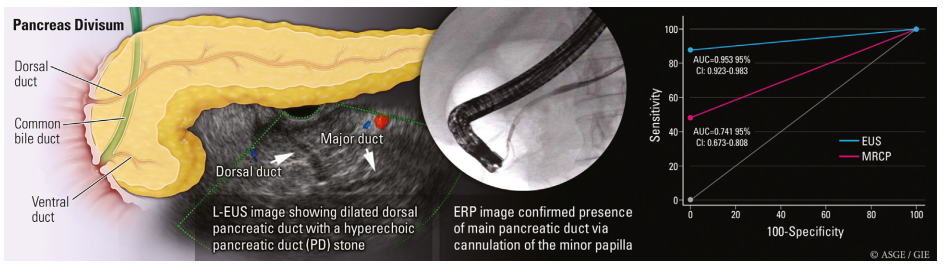
胰腺分裂(PD)诊断的金标准是ERCP,但ERCP属于侵入性操作,会引发术后胰腺炎。磁共振胰胆管成像(MRCP)是一种诊断PD的非侵入性方法,灵敏度为44%至60%。线阵超声内镜(L-EUS)在胰胆管追踪扫查方面表现优秀。李白文团队[15]研究发现L-EUS诊断PD的灵敏度高达90.8%,准确性为99%;显著优于MRCP的灵敏度48.4%、准确性95.4%(P<0.001)。此外,L-EUS诊断PD的AUC下面积为95.7%,高于MRCP的74.1%(P<0.001)。多因素回归分析显示胰管结石(OR,5.627;95%CI:1.391-22.765)和重症胰腺炎(OR,12.818;95%CI:2.280-72.061)与L-EUS诊断PD失败密切相关。
直肠无蒂病变(NPRLs)是早期直肠癌的一种亚型,常表现为黏膜下浸润癌。如果黏膜下层浅浸润(SMs,浸润深度<1000μm)的NPRLs可以采取内镜下切除;而黏膜下层深浸润(SMd,浸润深度≥1000μm)的NPRLs由于发生淋巴结转移的风险高,首选手术切除;因此,准确评估NPRLs的浸润深度对于治疗方案的选择至关重要。李跃等[16]采用NBI和L-EUS评估NPRLs的浸润深度,发现L-EUS和NBI的诊断准确性相当(96.2% vs 93.7%,P=0.625);L-EUS识别黏膜下层深浸润病变的敏感性为81.8%,而NBI为63.6%(P=0.500);L-EUS和NBI的特异性均为98.5%。此外,与单独使用L-EUS或NBI相比,联合使用L-EUS和NBI并未提高诊断准确性(94.9% 、96.2% vs 93.7%,P=0.333)。表明L-EUS和NBI测量NPRLs浸润深度的准确性相当,两种方法联合不能提高诊断准确性;临床实践中应首选单用NBI。
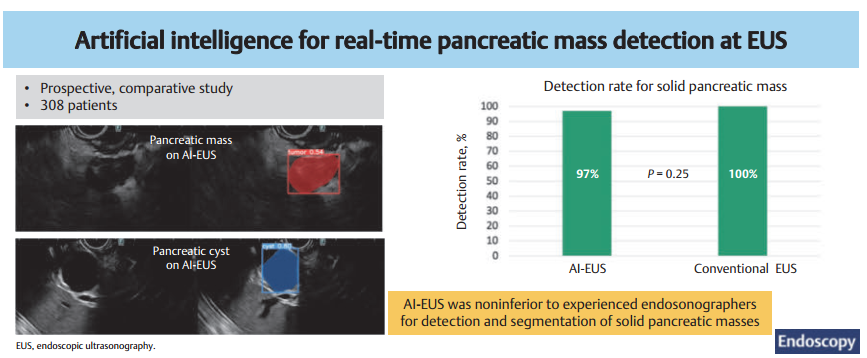
EUS以及EUS引导下组织获取是准确诊断胰腺实性病变患者最敏感的检查方式。然而,小病灶可能难以检测。美国Shyam Varadarajulu[17]开发了一款胰腺人工智能增强超声内镜成像分析软件PANCRAIEUS,其在检测和区分胰腺实性病变方面,性能与经验丰富的EUS医生相当(97.1% vs 100%; P=0.25)。这展示了人工智能超声内镜(AI-EUS)检测胰腺癌的潜力。
欧洲胃肠内镜学会 (ESGE)更新了超声内镜(Endoscopic Ultrasound,EUS)引导下组织采样技术指南,它是近年来对FNA操作引导性最强的指南。重要的新推荐如下[1]:
对于胰腺实性病变的组织取样,推荐使用末端切割型FNB针,而非反向斜面FNB针或者FNA针。19项RCT研究显示叉尖形FNB针在准确性及切割充性分方面均显著优于反向斜面FNA针和FNA针。
02
建议使用末端切割型FNB针,而非反向斜面FNB针或者FNA针,用于自身免疫性胰腺炎的组织病理学诊断。
03
对于尺寸≥20mm的黏膜下病变,推荐EUS-FNB或者黏膜切开辅助活检(MIAB)进行组织取样,后者可能是较小病变(<20mm)的首选。
04
建议使用末端切割型FNB针,而非反向斜面FNB针或者FNA针,进行淋巴结的组织取样。
05
推荐使用扇形穿刺技术,因为该技术可提高EUS引导下获取胰腺实性病变组织的诊断准确性。
06
同等推荐采用湿式抽吸或者慢拉技术进行胰腺肿块的EUS-FNB,因为与干式吸引相比,这两种技术能提供更高比例的合格样本和良好的组织完整性,并减少了标本的血液污染。
07
推荐使用末端切割型FNB针穿刺两次,使用反向斜面FNB针穿刺三次。当没有ROSE时,FNA针至少需要穿刺四次。
08
建议对伴有黄疸的胰头病变患者,在ERCP之前完成EUS引导下组织取样,尤其是在使用自膨式金属支架时更需遵循。
09
推荐在进行EUS-FNA时使用ROSE。对胰腺实性病变和黏膜下病变进行EUS-FNB,尤其使用末端切割型FNB针时,不需要ROSE。
010
推荐对胰腺肿块的EUS-FNB使用肉眼现场评估(MOSE),因为这种方法能以更少的穿刺次数获得更高诊断准确性。
(1)EUS引导下乙醇注射治疗小型胰腺神经内分泌肿瘤(PNEN)安全有效
目前对于≤2cm无功能低级别PNEN多采取随访,需要长期多次复查。日本一项研究评估了EUS引导下乙醇注射(EUS-EI)治疗小型PNEN的疗效,结果表明:PNEN完全消融率达88%,严重不良事件仅4%;追加治疗可显著提升疗效,长径<1cm肿瘤消融率可达91.7%[2]。因此,EUS引导下乙醇注射治疗小型1级胰腺神经内分泌肿瘤安全有效,是除手术或随访外的一种理想治疗选择。
(2)EUS规范化诊治胰岛素瘤
胰岛素瘤是一种少见的功能性PNEN,EUS为胰岛素瘤的诊断和治疗提供了新手段,为此中华医学会消化内镜学分会制定了《胰岛素瘤内镜诊疗专家共识(2025年)》,包括[3]:
① 推荐EUS作为CT及MRI检查的重要补充检查手段,尤其是对于≤10mm胰岛素瘤联合检测价值更高;推荐EUS引导穿刺活检作为胰岛素瘤病理组织检查的首选方法,组织标本建议进行HE染色、Ki‑67/MIB‑1染色及其他必要的免疫组化染色,根据肿瘤组织分化程度和细胞增殖活性进行分类和分级。
② 对于肿瘤<2cm且病理分级为G1/G2 级、无远处转移的胰岛素瘤患者,推荐EUS引导消融治疗(如无水乙醇注射、聚桂醇注射、射频消融);对于肿瘤长径在2-3cm的胰岛素瘤行EUS引导消融治疗应权衡利弊,如选择治疗则采用小剂量、多次注射治疗策略,以缓解临床症状为目标,不追求一次性完全消融肿瘤;对于全胰弥漫分布的多发病灶或合并淋巴结或远处转移,病理分级G3级及以上,有急性胰腺炎,不推荐行EUS引导消融治疗。
2
EUS治疗胃静脉曲张出血
(1)弹簧圈联合组织胶注射比单纯组织胶注射治疗胃静脉曲张更具优势
Jhajharia Ashok等[4]报道EUS引导下弹簧圈联合组织胶注射对比单纯组织胶注射治疗胃静脉曲张的研究,虽然两组患者静脉曲张即刻闭塞率无差异(100% vs 92.3%,P=0.49),但弹簧圈联合组织胶显著降低再干预需求(20.8% vs 53.8%,P=0.03)并延长患者生存期(48.3 vs 42.0周,P=0.04)。
(2)EUS下弹簧圈联合组织胶栓塞伴胃肾分流IGV1的效率更佳
陈洪潭教师牵头的多中心研究[5]比较了金属夹辅助与EUS引导弹簧圈治疗胃肾分流IGV1的疗效:两组患者胃静脉曲张再出血率(14.5% vs 8.7%,P=0.307)、技术成功率(96.4% vs 94.7%,P>0.999)、不良事件发生率(5.5% vs 5.8%,P> 0.999)和死亡率(12.7% vs 8.7%,P=0.467)均无显著差异。两组均未发现异位栓塞。而EUS-coil/CYA组的栓塞效率优于EC-CYA组(2.85±2.05cm²/ml vs 1.98±1.46cm²/ml,P=0.044)。 由此可知,EC-CYA和EUS-coil/CYA在预防IGV1再出血方面均安全有效。对已熟练掌握EUS-coil/CYA技术的医院应优先选择该方法治疗IGV1型患者;无法开展该技术的医院可以采用EC-CYA治疗IGV1。
(3)规范EUS引导弹簧圈栓塞术治疗胃静脉曲张
EUS引导弹簧圈栓塞术治疗胃静脉曲张的临床应用日趋广泛,中华医学会消化内镜学分会超声内镜学组、肝病学组制定了《胃静脉曲张超声内镜引导弹簧圈栓塞术专家共识(2025,杭州)》[6],其适应证:对具有高出血风险的胃静脉曲张进行内镜处理预防首次出血时,影像发现存在明显的门体分流道或内镜下胃静脉曲张表现为粗大或者瘤状外观;对于IGV出血的二级预防;对于胃静脉曲张出血需要急诊止血的患者,存在IGV出血、内镜视野不清或胃镜止血困难等情况;对于内镜下粗大的Leg型食管胃静脉曲张,也可酌情采用在胃曲张静脉内进行EUS引导弹簧圈栓塞术。
3
EUS引导下胆管引流术(EUS-BD)治疗恶性远端胆管梗阻(MDBO)
MDBO会出现黄疸、胆管炎,充分的胆管引流至关重要。一项来自荷兰的多中心研究比较了ERCP治疗MDBO失败后,随机采用PTBD(n=12)和EUS-BD(n=43)治疗:PTBD组患者90天死亡率为66.7%,EUS-CDS组为20.9%(P=0.005);PTBD组91.7%患者发生了一种或多种不良事件,EUS-CDS组不良事件发生率为44.2%(P=0.004);PTBD组术后中位住院时间为4天,EUS-CDS组为1天(P=0.001)[7]。这表明,对于MDBO患者在ERCP治疗失败后,EUS-CDS是更优选择。
另外,长时间胆总管插管会增加ERCP术后胰腺炎(PEP)的风险,对于胆管插管困难最常用的是预切开乳头括约肌切开术(PCP),但它也是PEP的独立危险因素。EUS引导下会师术(EUS-RV)显示出较高的成功率和较低的PEP发生率。一项随机对照试验比较了PCP(n=104)与EUS-RV(n=104)在恶性远端胆道梗阻且胆道插管困难患者中的疗效,结果显示,PCP与EUS-RV的技术成功率(93.3% vs 97.1%,P=0.33)和不良事件发生率(11.5% vs 5.8%,P=0.14)均无显著差异;PCP组胰腺炎发生率更高(8.7% vs 1.9%,P=0.06);EUS-RV的平均操作时间更长(47 vs 27min,P<0.001);两组住院时间相似(1.2天 vs 1.1天,P=0.25)[8]。表明对于不可切除的MDBO患者,PCP和EUS-RV的治疗效果相当。
由此可知,包含胆总管十二指肠吻合术(EUS-CDS)在内的EUS-BD,正逐渐成为ERCP治疗MDBO失败后的一线治疗方案。LAMS支架的出现极大地促进了EUS-CDS的技术应用。最近两项RCT研究表明,使用LAMS的EUS-CDS与ERCP的临床结局相当。但是使用LAMS支架进行EUS-CDS存在一个令人担忧问题,即支架误释放(SMD)。Chen Yen-I等[9]对上述两项RCT数据合并分析,发现152例MDBO患者接受LAMS支架EUS-CDS治疗,技术成功率为93.4%;11例(7.2 %)患者发生SMD,其中81.8%的SMD患者内镜补救成功,SMD相关不良事件发生率为2.6%;多变量分析显示肝外胆管直径≤15mm与SMD发生密切相关。表明EUS-CDS中支架误释放相对常见,但通常不会造成严重后果,因为大多数情况下可通过内镜手段进行补救;肝外胆管直径<15mm这一临界值可用于筛选适合的EUS-CDS患者。
4
EUS引导下胆囊引流术(EUS-GBD)
(1)EUS-GBD可以作为MDBO的挽救性治疗方法
上面已阐述ERCP治疗MDBO失败后,EUS-BD是一种有效的替代方法。但因为胆管扩张程度不足,一些MDBO患者无法接受EUS-BD治疗。对于这些患者,如果胆囊管通畅,EUS-GBD似乎是一种可行的治疗方法。一项来自西班牙的数据显示,ERCP和(或)EUS-BD失败后,采用EUS-GBD补救性治疗MDBO:技术操作成功率为99%;术后14天内胆红素降低超过50%的患者比例为78.1%,其中65.6%的患者胆红素水平恢复正常;57.1%(44/77)的患者术后能够开始化疗,70.6%(12/17)的患者后续能够手术治疗;但有26.3%的病例出现不良事件,其中3例死亡与EUS-GBD相关[10]。因此,仅考虑将EUS-GBD作为ERCP和(或)EUS-BD失败情况下的一种潜在补救性方法。
然而,另外一项国际多中心的研究却显示:对于胆囊管通畅的DMBO患者,ERCP失败后,EUS-GBD和EUS-CDS的技术成功率(96% vs 99%,P=0.36)和临床成功率 (86% vs 92%,P=0.17)无明显差异;每组不良事件发生率也相似;但EUS-GBD操作更简单[11]。
(2)规范EUS-GBD的临床应用
意大利介入超声内镜小组(i-EUS)对EUS-GBD的适应证、技术和管理的标准化做了一些建议[12]:① 对不适合外科手术的急性胆囊炎患者,EUS-GBD应优先于ERCP经乳头胆囊引流术(ET-GBD)、经皮胆囊引流术(PT-GBD)。②建议对保守治疗无效的患者应尽早(<48h)进行EUS-GBD。③建议在EUS-GBD术中使用双蘑菇头全覆膜金属支架(LAMS)。④不建议对适合手术切除胆囊的患者采用EUS-GBD。EUS-GBD不会增加胆囊切除术的复杂性,建议在手术前取出LAMS支架。
5
EUS引导下胃肠吻合术(EUS-GE)治疗胃流出道梗阻
目前EUS-GE治疗胃流出道梗阻已在国际上广泛应用。一项高质量的多中心研究显示,对于恶性胃流出道梗阻、胃出口梗阻评分(GOOS)为 0(无法经口摄入食物或液体)的患者,与传统十二指肠支架置入术相比,EUS-GE的6个月再干预率更低 (29% vs 2%,P=0.002)、支架通畅时间也更长(见下图)、1个月时的GOOS更高(1.91±0.9 vs 2.41±0.7,P=0.012);两组的技术成功率、临床成功率、30天内死亡率、不良事件发生率无明显差异[13]。因此,与十二指肠支架置入术相比,EUS-GE能减少再次介入的需要,可使患者拥有更好的饮食质量。
另一项发表于Gut的多中心随机试验则表明,与外科胃空肠吻合术(SGJ)相比,EUS-GE在治疗恶性胃流出道梗阻方面展现出全面优势:首先,EUS-GE组的治疗失败率显著低于SGJ组(7.9% vs 38.9%);其次,EUS-GE组患者恢复固体饮食的中位时间仅需2天,显著短于SGJ组的5天,且出院时所有EUS-GE患者均能进食固体,而SGJ组仅有80.6%患者能进食固体;然后,EUS-GE组术后中位住院日仅为3天,较SGJ组的9天大幅缩短,同时平均治疗成本也显著降低(33,934 vs 51,437美元),节省近17,503美元;最后,EUS-GE组患者在出院时的躯体功能和社会功能评分显著更高,疼痛与呼吸困难症状显著减轻。在安全性方面,两组操作相关严重不良事件发生率相近(EUS-GE: 2.6% vs SGJ: 2.8%)[14]。由此可知,对于恶性胃流出道梗阻的姑息治疗,EUS-GE在临床疗效与成本效益方面均优于传统外科胃空肠吻合术,应成为首选治疗方案。

(本文版权属于中国医学论坛报社,转载须授权)
查看更多