查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





这项研究在小鼠模型中发现,一种通常与结肠炎和结肠癌有关的微生物——产肠毒素脆弱拟杆菌(ETBF)可以在乳腺和肠道定植,迅速诱导乳腺上皮增生,并促进了乳腺癌的发生和转移进程。

人体共生菌群的失调可能会导致多种疾病,包括肠道炎症、神经退行性疾病以及癌症。值得一提的是,尽管已知微生物存在于人体的胃肠道、鼻腔通道和皮肤等部位,但长期以来,乳房组织通常被认为是无菌的。
然而,近期的一些研究已经证实乳腺中也存在微生物群落,但它们对乳腺癌的生物学影响仍然难以捉摸。基于此,我们可以通过对比正常乳腺和患病乳腺的微生物谱系,从而推测出哪些非正常类型的乳腺微生物具有潜在的致病能力。
在这项研究中,本研究的通讯作者 Dipali Sharma 教授对此表示:“我们的研究发现了另一个风险因素,那就是微生物群。如果微生物群受到干扰,或者体内含有具有致癌功能的产毒微生物,这可能被认为是乳腺癌的另一个风险因素。”
研究人员对已发表的比较乳腺癌幸存者和健康志愿者良性和恶性乳腺肿瘤微生物组成的研究进行了临床数据的荟萃分析。他们发现,在乳腺癌幸存者的所有乳腺组织样本和乳头分泌液中都检测到了脆弱拟杆菌。
紧接着,研究团队将产肠毒素脆弱拟杆菌(ETBF)给一组小鼠口服。首先,产肠毒素脆弱拟杆菌(ETBF)迅速在小鼠的肠道中定植,且在三周内,小鼠的乳腺组织发生了通常表现为乳腺癌的癌前病变——导管组织增生。
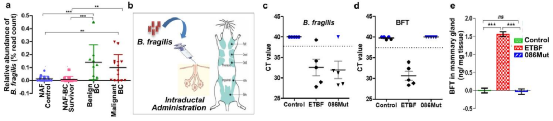
引入ETBF后,小鼠的乳腺组织的导管发生增生
不仅如此,研究人员还观察到,当他们将产肠毒素脆弱拟杆菌(ETBF)直接注射到小鼠的乳头后,两到三周内就会出现类似增生性的症状,并且暴露于毒素的细胞比未暴露于毒素的细胞表现出更快的肿瘤进展和更强的肿瘤侵袭性。
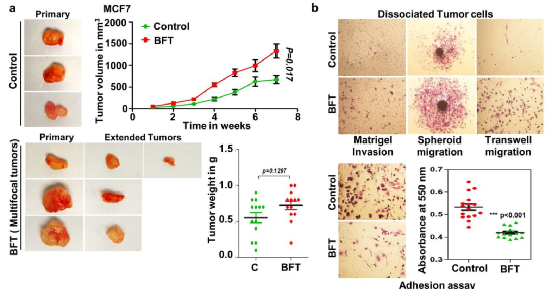
暴露于毒素的细胞比未暴露于毒素的细胞表现出更快的肿瘤进展和更强的肿瘤侵袭性
有趣的是,与非产毒的脆弱拟杆菌相比,产肠毒素脆弱拟杆菌(ETBF)更能强烈诱导植入乳腺导管的肿瘤细胞的生长和转移进展,而暴露在毒素中的乳腺癌细胞似乎保留了对毒素的记忆,在接种到健康小鼠之后,增殖速度更快,侵袭性更强。研究人员将其称为“BFT-记忆”。
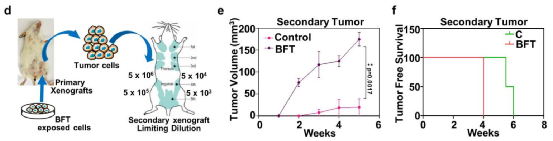
暴露在毒素中的乳腺癌细胞产生了“BFT-记忆”
除此之外,研究人员还观察到Notch1和β-catenin细胞信号通路参与了产肠毒素脆弱拟杆菌(ETBF)促进乳腺组织病变的过程。
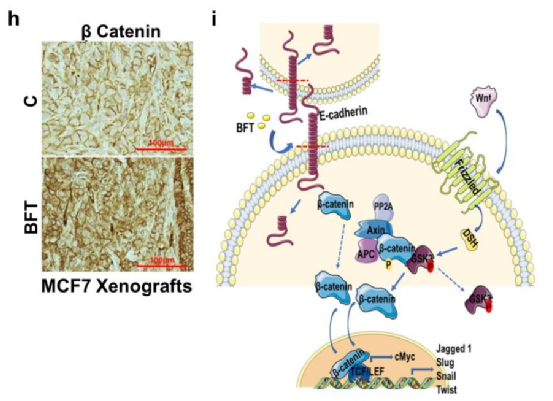
Notch1和β-catenin细胞信号通路参与了EBFT促进乳腺组织病变的过程
总而言之,这项研究观察到,当产肠毒素脆弱拟杆菌(ETBF)被引入小鼠的肠道或乳腺导管时,它总是会诱导肿瘤细胞的生长和转移性进展,由此揭示了诱发乳腺癌的另一个潜在风险因素。
当然,后续还需要更多的研究来了解产肠毒素脆弱拟杆菌(ETBF)是如何在全身移动的,并确定其是否是触发人类乳腺细胞转化的直接驱动因素。由此看来,未来我们或许就可以通过检查粪便或乳腺样本中的微生物组变化,以评估自身的乳腺癌患病风险。
生物世界平台发布
查看更多