查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





近日,上海交通大学医学院附属仁济医院消化科陈豪燕、洪洁团队在国际权威期刊《细胞·代谢》(Cell Metabolism)发表重要研究成果,首次系统揭示了肥胖肿瘤患者免疫治疗效果更优。研究发现,肠道菌群能通过激活脂肪组织的脂质代谢程序,有效增强肿瘤内部的免疫细胞功能,为通过调控菌群或代谢途径提升癌症免疫治疗疗效提供了全新策略。



免疫检查点抑制剂(immune checkpoint blockade,ICB)已深刻改变多种恶性肿瘤的治疗格局,但其疗效在不同患者之间仍存在显著差异。近年来,一个引人关注却尚未得到充分阐释的现象是:部分肥胖肿瘤患者在接受免疫治疗时反而表现出更优的疗效。这一被称为“肥胖悖论”的现象,其背后的生物学机制仍有待深入解析。
本研究系统揭示了一条此前未被充分认识的“肠道菌群–脂肪组织–抗肿瘤免疫”调控轴,阐明了宿主代谢状态如何通过肠道微生物与脂肪代谢的协同作用,塑造免疫治疗应答。
研究显示,在接受ICB治疗并获得良好疗效的肥胖患者中,其肠道菌群结构与非应答者显著不同,表现为核黄素(riboflavin)合成菌的显著富集、微生物核黄素生物合成通路增强,以及其代谢衍生物黄素腺嘌呤二核苷酸(flavin adenine dinucleotide,FAD)水平的显著升高。这一特征性微生物–代谢谱系提示,FAD代谢可能是连接肠道菌群与宿主抗肿瘤免疫反应的重要枢纽。
在饮食诱导性肥胖(diet-induced obesity,DIO)小鼠模型中,研究进一步证实,无论是实施粪菌移植、补充特定Lachnospiraceae菌株,还是直接给予FAD,均可显著增强抗PD-1治疗的抗肿瘤效果。机制研究表明,这些干预并非直接作用于T细胞本身,而是通过激活肠系膜脂肪细胞内源性的脂质重塑程序,促进多不饱和脂肪酸(polyunsaturated fatty acids,PUFAs)的合成,从而增强肿瘤浸润CD8⁺ T细胞的细胞毒功能。
值得注意的是,当脂肪酸去饱和酶2(fatty acid desaturase 2,FADS2)被抑制后,FAD介导的免疫增强效应完全消失,明确了脂肪细胞内FADS2依赖的脂质代谢重编程在该免疫调控轴中的关键作用。
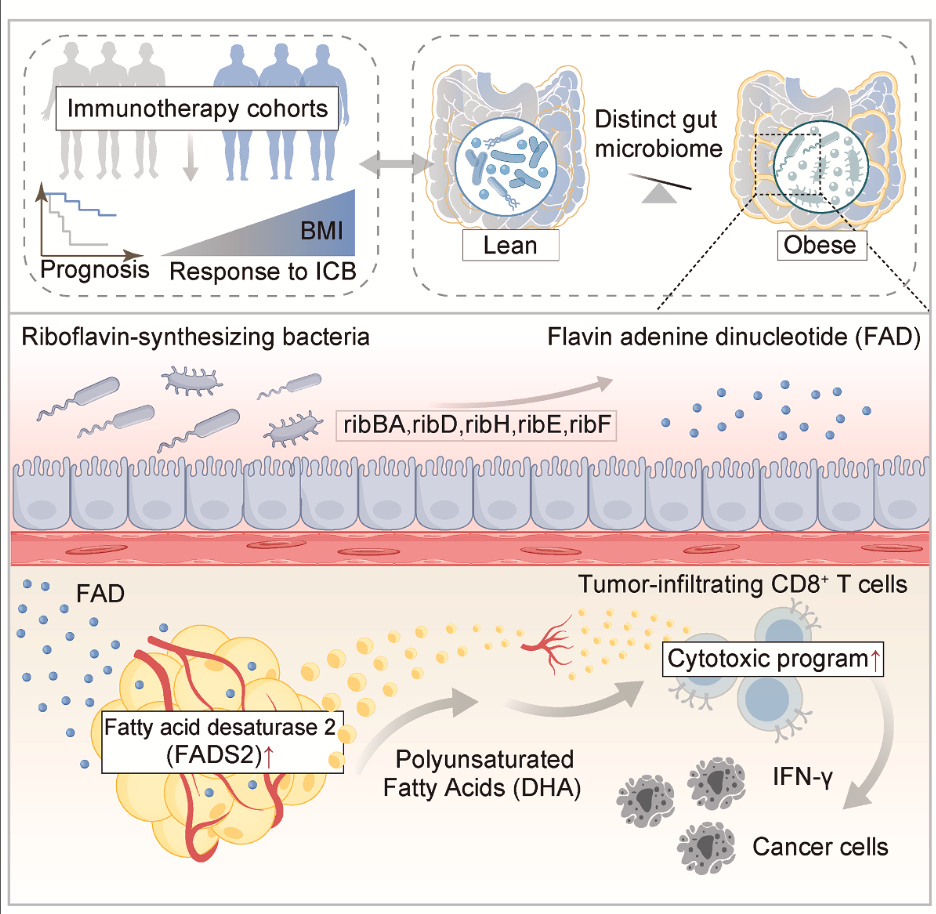
临床队列分析进一步支持了上述机制:血液中PUFAs水平较高,尤其是二十二碳六烯酸(docosahexaenoic acid,DHA)水平升高的患者,其肿瘤组织中CD8⁺ T细胞浸润更为丰富,免疫治疗疗效亦更为显著。更具转化意义的是,DHA补充可显著改善瘦型小鼠对ICB治疗的应答,提示通过代谢干预有望在一定程度上“模拟”肥胖相关的免疫治疗获益。
综上所述,本研究首次系统阐明了肠道菌群衍生的FAD代谢信号如何通过脂肪组织介导的脂质代谢重塑,放大抗肿瘤免疫反应。该研究不仅为理解肥胖人群中免疫治疗获益提供了机制层面的解释,也为通过微生物调控、代谢重编程及精准营养干预优化癌症免疫治疗疗效提供了新的思路。
本研究由仁济医院消化科主导完成。论文的共同第一作者包括博士研究生童天颖、博士研究生黄孝雯及硕士研究生李灵翕;仁济医院消化科陈豪燕研究员、洪洁研究员、中国医科大学附属盛京医院尹燕主任以及复旦大学附属肿瘤医院刘凤林主任医师为共同通讯作者。本研究还得到了中国科学院院士、仁济医院消化科主任医师房静远教授的大力支持。研究团队表示,该研究不仅为免疫治疗应答提供了新的潜在生物标志物,也为通过微生物与代谢调控优化免疫治疗疗效提供了新的研究方向。
来源:上海交通大学医学院附属仁济医院
查看更多