查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过








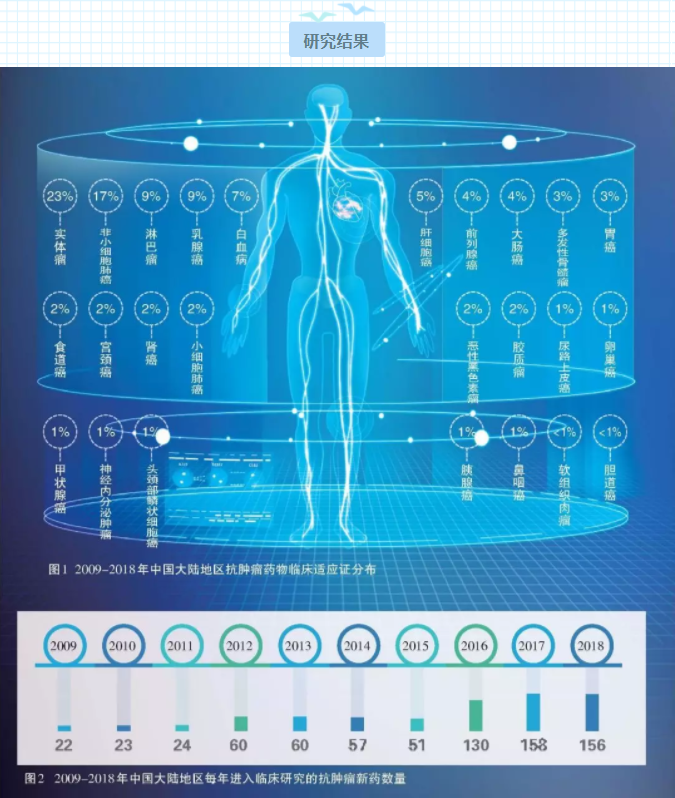


从抗肿瘤药物临床试验项目数量到在研抗肿瘤药物品种数量、新型靶向药和免疫药数量,从临床试验机构能力到医政、药监部门的管理举措,十年间中国肿瘤药物研发领域已经取得了足以令世人瞩目的巨大进步—— 我们迫切地希望将这些变革展现给全世界,从而提升中国肿瘤临床试验的国际影响力。为此,在国家药品监督管理局药品审评中心的支持下,由赫捷院士领衔、李宁教授牵头,中国医学科学院肿瘤医院联合全国多家兄弟医院GCP 中心共同完成“中国大陆地区抗肿瘤药物临床试验十年发展”这一研究,并得到国际学术界的认可。
在骄傲和欣喜的同时,我们也冷静地认识到,中国肿瘤药物研发水平与欧美发达国家仍然存在着差距,未来还有很大的挑战。过去很长一段时间,国内医药企业主要着眼于仿制药的开发,自主产出的新药也以“模仿”国外成熟药物结构机制的“me-too”药为主,真正具有创新机制、创新靶点的抗肿瘤药物还很稀缺。一方面,这是历史的必然,中国有太多肿瘤患者迫切地渴望用上便宜而有效的治疗药物,药物开发必须加速再加速,甚至可能牺牲创新;另一方面,在党和政府的引领下,中国的经济、科技水平已经不可同日而语,必须通过创新追赶全球医药产业步伐,再通过创新引领全球医药产业发展。
我们欣喜地看到,最近两三年,我国自主研发的抗肿瘤新药越来越多,以安全性和药代动力学指标为研究终点的Ⅰ期临床试验比例逐渐增高,其中不乏与欧美处于同等研发阶段、甚至世界首创的新药早期研究,也有不少国产新药在早期研发阶段就覆盖多个国家或地区,但临床开发策略和试验设计同质化较为明显。根据欧美国家理念和我国药审政策最新要求,新药在首次人体试验之前就应当确立产品开发目标和开发策略,以临床需求为导向,体现与现有产品的优势,实现差异化竞争,并在临床研究过程中实现良好的风险管控,不断修正目标和路径。这种以终为始、基于临床、控制风险的新药开发思路值得我国所有医药从业人员学习和借鉴。
药物研发的过程极其复杂和艰苦,临床研究其实已经到了“ 临门一脚”,在这之前还需要机制研究、药物发现、筛选、制剂、生产、临床前研究等一系列“ 规定动作”。新药研发不仅是临床研发人员的职责,更离不开基础研究人员的辛勤付出;只有探索清楚肿瘤的发病机制,才有可能从根源上开发出更好的药物。我国一些特色瘤种(胃癌、食管鳞癌、鼻咽癌、肝细胞癌),正是得益于基础研究才揭示了中国人群与西方人群发病机制上的差异。然而,从基础转化到临床需要时间的沉淀、耐心和一点运气,在“精准医学”的大背景下,由病因学、分子生物学引导的药物研发势必成为主流。尽管现阶段临床试验比例不高,国内针对特色瘤种、罕见瘤种的研究一定是未来重要的发展方向。中国想要在创新药、特色瘤种上进一步突破,基础研究和临床研究都要有持续性鼓励和支持。
作者 | 吴大维 黄慧瑶(国家癌症中心 中国医学科学院肿瘤医院)
编辑 | 郝冉(中国医学论坛报)
美编 | 刘孝炎(中国医学论坛报)
本文首发于2019.11.21《中国医学论坛报》B1版


查看更多