查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





35岁男性患者,病程长达四个月,主要表现为反复上腹部疼痛,近两周症状加重,并伴有高热四天。
患者最早于2022年7月因高脂血症性胰腺炎在当地医院住院治疗两个月,出院半个月后,进食引发腹痛,再次入院。当地医院CT检查显示胰腺肿胀、周围水肿与渗出,保守治疗七天后,实施ERCP下支架置入术。术后三天,患者出现高热与腹痛,复查腹部CT提示胰管扩张合并假性囊肿、胃体大弯侧外侧假性囊肿或包裹性积液,遂进行经皮超声引导下囊肿穿刺引流。然而,三次引流后症状未缓解,患者因持续高热、腹胀加重,转入我院胰腺外科。
既往无特殊病史与手术史。
转入时生命体征不稳定,血压101/60 mmHg,心率118次/分,体温38℃,神志萎靡,心肺检查无异常,腹部膨隆,可触及包块,有压痛,反跳痛不明显,肠鸣音减弱。外院引流管穿刺引流200 ml液体后,再无液体引出。
感染性胰腺坏死

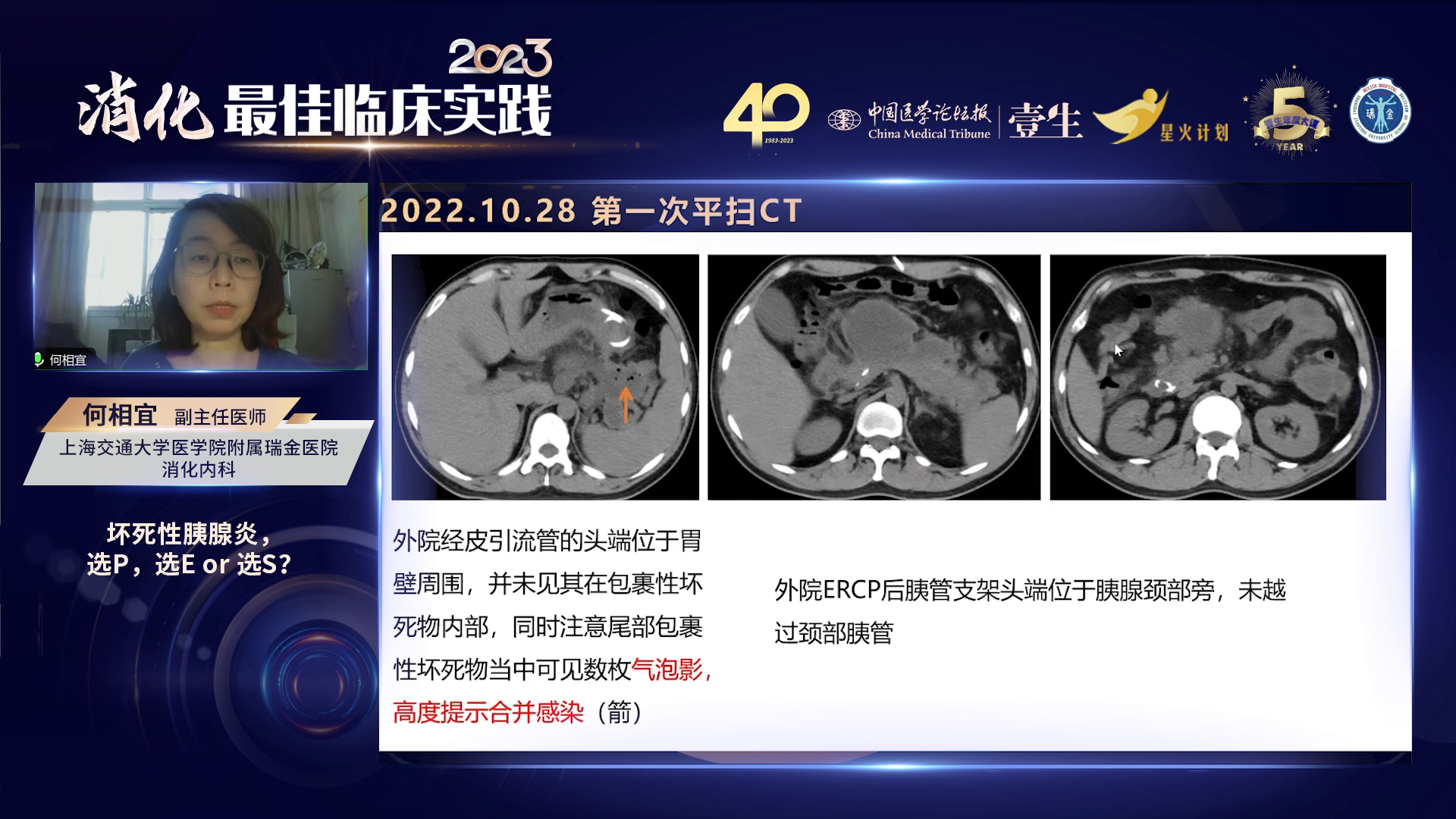
参考2021年急性胰腺炎诊治指南,早期坏死合并感染及后期包裹性坏死合并感染,无论囊壁成熟与否,均属于感染性坏死。该患者有发热、腹痛症状,CT显示气泡征,符合感染性胰腺坏死特征。指南不推荐常规使用细针穿刺明确感染,当胰腺炎出现发热、腹痛及全身症状恶化等感染症状时,应考虑评估感染性胰腺坏死的可能。
此病例感染性胰腺坏死的成因可能包括:急性胰腺炎后一周内进行ERCP,操作中注入造影剂,而患者胰腺颈部损伤严重,多数胰管颈部段受损,可能导致引流不畅,造影剂进入体尾部远端胰管,引发继发感染;胰管引流不畅、胰管颈部损伤也是加重感染的因素;ERCP术后,肠道屏障功能障碍,菌群紊乱和移位,以及胰腺炎后十二指肠水肿、压力增高,支架可能加重肠液逆流,进而导致感染。
指南指出,对于感染性胰腺坏死的治疗,采用step - up策略,即先进行抗菌药物保守治疗,若无效则考虑经皮穿刺,因其相对安全;若经皮穿刺效果不佳,可进行内镜下引流;若仍不适合或效果不理想,再进行外科清创。
2020年美国急性坏死性胰腺炎管理共识表明,对于早期急性期(小于2周)感染性坏死物积聚的患者,可考虑经皮引流,无需等待囊壁成熟,多作为危重病人或手术风险大的患者的紧急治疗手段。而内镜介入目前不推荐在早期阶段实施,因其并发症发生率较高,且后续内镜操作次数可能增加,建议在四周后形成假性囊肿或包裹性坏死病灶,患者出现压迫症状或感染征象时进行。
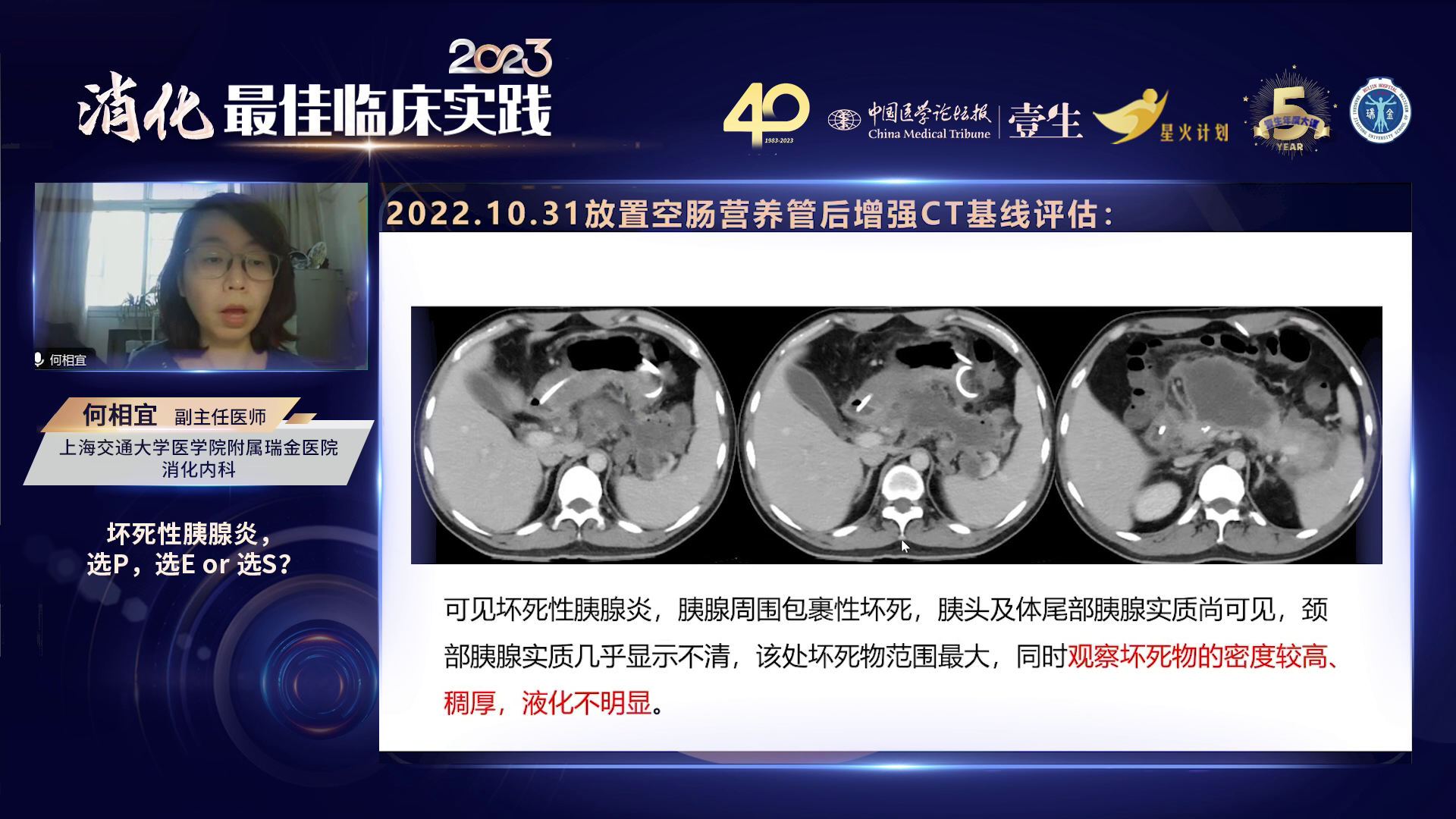
本病例在外院进行的经皮引流,符合早期感染性坏死物积聚患者可经皮引流的原则。但外引流效果欠佳,可能原因包括引流管移位脱位、坏死物质密度高且黏稠、液化不良,即使留置引流管,引流效果仍可能不佳,导致胰腺病情难以控制。
患者术后十天转入普通病房,恢复较快,但出院后引流管逐渐拔除,仅剩下胰体部的引流管,每天有350毫升清亮液体持续流出约三个月,复查CT显示引流管无法拔除,ERCP发现胰管在颈部断裂,考虑为SAP后合并的DPDS。
DPDS分为胰外漏,包括端漏和侧漏,侧漏又分为术后漏和炎症漏,漏的流量分低、中、高,此病例属于中等胰管断裂,是重症坏死性胰腺炎少见且极具挑战的并发症。在SAP发生胰管断裂的概率为45.9%,其中2/3为部分断裂,1/3为完全离断,多合并于SAP且包裹性坏死较多,单纯假性囊肿断裂少见。
对于DPDS的治疗原则,首先是通畅引流和抑制胰液分泌,其次需要内镜和外科介入。部分胰瘘病例可在中位时间70天左右自发闭合,概率约为38%,有报道生长抑素可能增加自发闭合的作用,但存在较大争议。如使用奥曲肽5-8天引流量无明显减少,可考虑停用。
本病例因提前放置引流管,无法进行超声内镜下的闭合引流,故首先考虑胰管支架桥接治疗,包括主动桥接和被动桥接。主动桥接是内镜引流管通过裂口连接体尾部和头部胰管;被动桥接是当导丝难以越过裂口进入体尾部胰管时,将引流管置于囊内,通过囊内引流降低胰管内压力,促进裂口愈合,也可能为主动桥接创造机会。
2023年2月进行ERCP,胰管插管后导丝在胰腺颈部中断,注射造影剂后,造影剂仅在头颈部胰管显影,导丝无法越过颈部狭窄段。反复尝试后,导丝进入类似于窦道样的通道,但并非体尾部胰管,而是外引流管相关窦道。最终将支架头端置入窦道口内,实现被动引流,即将体尾部胰液经窦道、支架引流到乳头外。
术后第一天,未关闭外引流管时,造瘘管出现胆汁样液体,推测可能因腹腔内压略高于胆道压力,十二指肠区域肿胀,乳头、支架与外引流相通,外引流管未夹闭承受大气压力,导致肠液胆汁逆行进入引流袋。口服亚甲蓝后,引流袋内出现亚甲蓝,证实此猜测。随后夹闭引流管,隔绝外部大气压,使引流液进入肠腔,并放置空肠营养管减少胰液分泌或肠液反流。四天后CT显示无明显积液,内引流通畅,患者无不适症状。
患者夹闭引流管带管回家,一个月后复诊,入院第二天突然出现腹痛腹胀,开放腹腔引流管后引出400 ml清亮胰液,考虑支架堵塞或移位,引流不畅。复查CT发现引流管移位,堵住窦道口。再次进行ERCP时,考虑到直接拔掉支架,导丝可能再次进入窦道,于是在保留胰管支架的基础上进行胰管插管,结果导丝沿着支架成功进入体尾部胰管,造影显示体尾部胰管明显扩张,颈部有明显狭窄。使用探条对颈部狭窄处充分扩张后,置入F型支架,越过颈部狭窄口进行主动桥接,连接体尾部胰管和乳头。术后腹腔引流管不再有液体渗出,患者开放饮食,无不适后出院。
查看更多
专家点评
1) 坏死性胰腺炎的诊断需结合患者症状、影像学检查及实验室指标,如本病例中患者的发热、腹痛症状,CT显示的气泡征及相关实验室炎症指标升高等,均支持感染性胰腺坏死的诊断 。
2) 治疗策略应遵循step - up原则,根据患者具体情况选择合适的治疗手段。经皮穿刺、内镜引流及外科清创各有其适用时机与条件,需多学科团队讨论制定个体化方案 。
3) 对于重症胰腺炎后胰瘘,尤其是DPDS的处理,要注重通畅引流、抑制胰液分泌,并合理选择内镜或外科介入。内镜下胰管支架桥接治疗是重要手段,包括主动与被动桥接,需根据实际情况灵活应用 。