查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





心血管药物管理长期聚焦于“何时启动治疗”,但近年来“何时停药”逐渐成为临床用药的重要问题。本文基于《欧洲心脏杂志》(Eur Heart J)前沿综述分为上下两篇,系统梳理需停用或替换的心血管药物,旨在降低药物相关风险、减少无效治疗,推动个体化精准用药。
本篇为上篇,重点介绍需要停用的具有潜在危害的药物。
药物停用的阻碍:
停药研究的缺乏和临床惰性
停药研究的缺乏 由于随机对照试验(RCT)的随访时间通常较短,大多数的大型RCT主要研究的是启用某种新治疗方案的效果,而非在长期治疗后停用某些特定治疗方案产生的影响。
临床惰性 当患者就诊时,临床医生总是倾向于不断加用药物,而较少考虑停药。“临床惰性” 或 “如果患者病情稳定,就不应停止治疗” 的观念会加剧这一现象。事实上,即使某种药物本身无害,继续使用不必要的药物仍可能造成损害,因为多重用药本身就存在害处。
本文总结了两类需要考虑停用的心血管药物:①存在潜在危害的药物。②缺乏明确临床获益的药物。
为了预防潜在危害而停药
针对接受口服抗凝治疗的稳定性冠心病患者的抗血小板治疗策略
在急性冠脉综合征(ACS)和/或接受经皮冠状动脉介入(PCI)术后,建议采用双联抗血小板治疗来预防复发性心脏不良事件。如果这些患者同时伴有房颤,目前的临床指南建议:①首先采用短期三联治疗,即直接口服抗凝药(DOAC)、P2Y12抑制剂和阿司匹林;②随后过渡到双联抗栓治疗,即DOAC联合一种抗血小板药物,持续最长1年;③之后调整为单独口服抗凝治疗。
调查显示,有相当一部分房颤合并稳定型缺血性心脏病患者,在接受口服抗凝治疗的同时,还联用阿司匹林。ORBIT-AF研究显示,接受不恰当阿司匹林治疗的患者中,有1/3甚至无动脉粥样硬化型心血管疾病(ASCVD)病史。多个注册分析和专项RCT研究表明,与单用口服抗凝药相比,口服抗凝药联用阿司匹林并未降低缺血事件的发生率,反而大出血的风险却增加。
一项最具说服力的研究表明,将2236例合并稳定性冠心病的房颤患者随机分配至两组,即利伐沙班单用和利伐沙班联用一种抗血小板药物。不出所料,利伐沙班联用抗血小板药物与单用利伐沙班相比,联用使大出血风险增加了近70%,并且联用抗血小板药物还会使死亡和血栓事件的复合终点发生率增加了36%,死亡率增加了80%。因此,当遇到因房颤而接受口服抗凝治疗的患者时,临床医生应仔细评估联合用药以及联用抗血小板治疗的指征。在ACS或PCI术后,最晚不超过1年,通常应考虑停用抗血小板治疗。
小剂量阿司匹林在ASCVD一级预防中的应用
为了减少动脉粥样硬化事件,指南推荐所有ASCVD患者使用小剂量阿司匹林。而在无ASCVD,但有心血管疾病风险患者的多项试验中,阿司匹林治疗虽然可减少非致死性缺血事件,但同时也增加非致死性出血事件。类似的结果出现在了糖尿病患者的研究中。尤其是在老年人中,阿司匹林的出血风险似乎超过了心血管获益。因此当前指南建议,糖尿病患者可以考虑使用阿司匹林,而在中、低心血管疾病风险的患者中,阿司匹林可能有害,因此需要禁用。
β受体阻滞剂和钙通道阻滞剂(CCB)的联用
虽然β受体阻滞剂联合二氢吡啶类CCB在血压管理中具有额外疗效,但应避免将β受体阻滞剂与非二氢吡啶类CCB联合用于心律失常或高血压治疗。这是因为这种联合用药的负性心率作用可能导致严重的不良事件。
然而,在伴有代偿性射血分数降低型心衰(HFrEF)的患者以及控制不佳的快速心室反应的房颤患者中,尤其是当认为左室功能因持续心动过速而受到抑制时,可以谨慎地联用小剂量非二氢吡啶类CCB与β受体阻滞剂。
需要注意的是,在HFrEF中禁用非二氢吡啶类CCB的证据有些过时,这些研究并非主要针对房颤患者的心率控制问题。
CCB在射血分数降低型心衰(HFrEF)患者中的应用
非二氢吡啶类CCB,如地尔硫䓬和维拉帕米,常用于治疗心绞痛和心律失常。但因其负性肌力作用,当前指南不推荐在HFrEF患者中使用CCB。
二肽基肽酶-4(DPP-4)抑制剂在合并心血管疾病的糖尿病患者中的应用
DPP-4抑制剂能防止胰高血糖素样肽-1(GLP-1)和葡萄糖依赖性促胰岛素多肽的分解,从而增加胰岛素分泌,抑制胰高血糖素释放,使血糖水平恢复正常。先前的RCT研究证实了5种DPP-4抑制剂的心血管安全性,但它们是否具有心血管益处目前尚未证明。
在一项与安慰剂对照的研究中,DPP-4抑制剂沙格列汀显著增加了心衰的住院风险,因此对于心衰或有心衰风险的患者,不推荐使用DPP-4抑制剂。
鉴于GLP-1受体激动剂和钠-葡萄糖协同转运蛋白-2(SGLT-2)抑制剂已被证实具有明显的心血管获益,对于已确诊有心血管疾病且正在使用DPP-4抑制剂的患者,这两类药物应优先考虑使用,并进行相应地药物转换。
多巴酚丁胺或米力农在未发生危及生命低灌注的失代偿性心衰患者中的应用
虽然正性肌力药可以暂时改善心输出量,但在无生命危险的低灌注患者中,使用正性肌力药已被证实弊大于利。
OPTIME-CHF试验结果表明,在失代偿性心衰的住院患者中,米力农使死亡、心肌梗死、房颤、低血压和室性心动过速的复合事件增加了2~3倍。后续的大量研究均证实其弊大于利,因此应避免将其作为常规治疗手段。然而,如果患者因等待移植而使用该治疗,则必须确保已植入心律转复除颤器。
缺血性卒中患者双联抗血小板治疗(DAPT)超过3周
当前指南基于两项大型RCT研究提出一个建议:对于发生轻型非心源性缺血性卒中或处于短暂性脑缺血发作(TIA)高危状态的患者,推荐在症状出现后24小时内接受持续21天的DAPT(阿司匹林+氯吡格雷),以降低90天内复发性缺血性卒中风险。
CHANCE试验的事后时程分析表明, DAPT降低复发性卒中的获益主要体现在治疗的最初3周内,此后,相关出血风险大于缺血性获益。
另两项大规模RCT研究也表明,DAPT不能减少复发性卒中,却显著增加了出血风险,甚至在一项试验中还增加了死亡率。基于这些结果,DAPT应限于最初的21~30天,对于长期服用的患者应予以处方优化。
烟酸
烟酸可通过肝脏和脂肪组织的双重机制,降低低密度脂蛋白胆固醇和甘油三酯,并升高高密度脂蛋白胆固醇。两项大型RCT研究表明,尽管烟酸能改善血脂谱,但未观察到对心血管结局有获益影响。此外,烟酸治疗还增加了严重不良事件发生率。因此,在心血管疾病患者中,目前尚无烟酸的适应证。
非类固醇类抗炎药(NSAID)
NSAID广泛用于治疗疼痛和减轻炎症。NSAID主要有两种类型:①非选择性NSAID,如双氯芬酸和布洛芬,它同时抑制环氧合酶(COX)-1和COX-2;②选择性COX-2抑制剂,如罗非昔布(rofecoxib)。
尽管选择性NSAID的胃肠道不良反应较少,但有研究表明,它能显著增加主要血管事件的风险。大型荟萃分析显示,一些非选择性NSAID也会增加主要血管事件的风险。因此在一般人群使用NSAID应具有选择性,对于确诊的冠心病患者,应尽量减少NSAID的使用。
此外,NSAID会抑制肾脏中前列腺素的分泌,从而导致水钠潴留和肾脏血管收缩。这可能对HFrEF和射血分数保留性心衰(HFpEF)患者有害。几项观察性研究表明,在HFrEF患者中使用NSAID治疗会加重心衰,导致患病率和死亡率增加。因此,在心衰患者中,应避免使用或停用NSAID。
肾素-血管紧张素-醛固酮系统抑制剂的联合用药
当前指南建议,所有HFrEF患者均应使用血管紧张素受体-脑啡肽酶抑制剂(ARNi),仅在ARNi治疗不适用时,才考虑使用血管紧张素转换酶抑制剂(ACEi)和血管紧张素受体拮抗剂(ARB)。
此外,鉴于盐皮质激素受体拮抗剂(MRA)对改善死亡和住院结局的显著益处,建议所有在使用ARNi、ACEi、ARB的患者中,加用MRA。
值得注意的是,在ACEi治疗基础上加用ARB的方案,尤其是在同时使用MRA的情况下,由于未明显改善死亡结局,并且增加了更多不良事件,现已被淘汰。
噻唑烷二酮类药物在心衰患者中的应用
噻唑烷二酮类药物,也称为格列酮类,是一类治疗糖尿病的药物。该类药物已被证明与心衰住院风险增加相关。因此,噻唑烷二酮类药物不应用于存在心衰风险或有心衰病史的患者。
鉴于SGLT-2抑制剂与GLP-1受体激动剂在心血管方面呈现出的一致益处,因此,在治疗合并心血管疾病的糖尿病时,应优先使用。然而,考虑到噻唑烷二酮类药物作为仿制药的可获及性,在无心衰的糖尿病治疗中,噻唑烷二酮类药物仍是一种可能有效的替代选择。
表1. 存在潜在危害药物
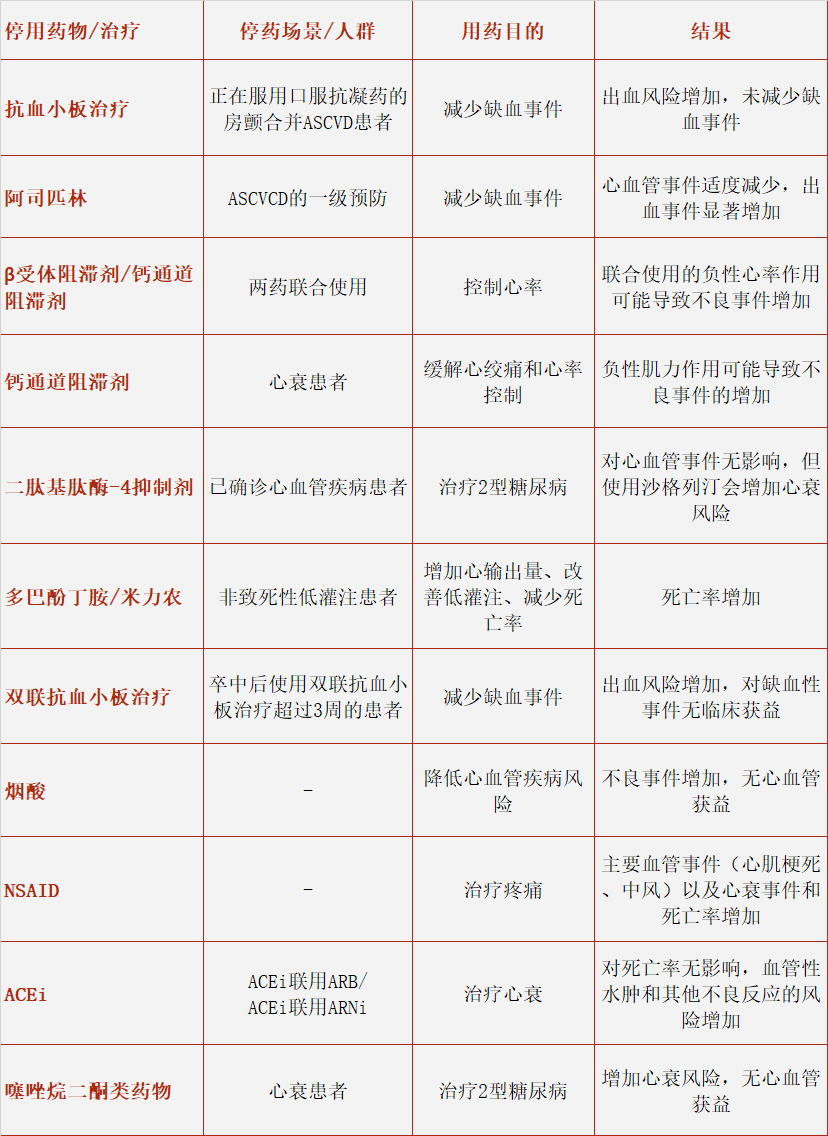
注:血管紧张素转换酶抑制剂(ACEi)、血管紧张素受体拮抗剂(ARB)、血管紧张素受体-脑啡肽酶抑制剂(ARNi)、动脉粥样硬化型心血管疾病(ASCVD)、非类固醇类抗炎药(NSAID)。


编译:王天任
审校:邢英

互动有奖


所有参与互动答题的医生都将获得价值150元的《中国医学论坛报》数字报一年期权限和《35天医疗AI实战计划》训练营观看权限。
活动截止时间:2025年7月9日

查看更多