查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





随着医学的发展,肿瘤的治疗已经进入了精准治疗时代,多个瘤种都有了靶向治疗选择。靶向治疗涉及基因检测,只有在精准靶点的指导下进行抗肿瘤治疗,才有可能使患者获得更长的无进展生存(PFS)和总生存(OS)。然而,在过去的20年里,卵巢癌的精准治疗一直处于沉寂状态,直到PARP抑制剂的出现,卵巢癌的靶向治疗才迎来希望的曙光。本期特邀天津医科大学总医院张琳琳教授,为大家深入解读卵巢癌的精准治疗之路。
张琳琳 教授
天津医科大学总医院 肿瘤内科
副主任医师,肿瘤学博士
芬兰赫尔辛基大学访问学者
天津医科大学总医院“新世纪人才”、“青年技术骨干”
中国中西医结合学会身心专业委员会委员
北京医学奖励基金会肺癌青年医学专家委员会青年委员
天津市抗癌协会中西医结合肿瘤治疗专业委员会常委
天津市中西医结合学会呼吸病专业委员会青年委员
《中国肺癌杂志》编委会的青年编委
PARP酶在DNA单链修复中起关键作用,而双链断裂有两种修复方式:同源重组修复(HRR)和非同源末端连接(NHEJ)。HRR是一种高保真、精准、缓慢的修复方式,BRCA1/2,RAD51等修复酶在HRR中发挥关键作用。NHEJ是一种相对快速,非保真的修复方式,可能会造成碱基排序错乱,形成基因组瘢痕,导致基因组不稳定性增加。在具有同源重组修复缺陷(HRD)的细胞中,使用PARP抑制剂后, 单链DNA 断裂损伤不能被修复,同时,双链DNA 断裂不能被同源重组(HR)通路修复,而通过NHEJ通路进行修复,造成过多的碱基错乱排列,基因组不稳定性明显增加,从而导致细胞死亡,这个过程就是所谓的“合成致死”效应 [1]。
自2019年V1版美国国立综合癌症网络(NCCN)指南[2]中就推荐对所有新确诊的卵巢癌(包括输卵管癌、原发腹膜癌)患者进行BRCA1/2检测。目前,对于卵巢癌的诊断不仅仅局限于病理诊断,分子基因层面的诊断也非常重要,这不仅能了解患者的发病机制,还能为医生选择治疗方案提供指导。
有1/3卵巢癌存在BRCA1/2突变或启动子甲基化[3],BRCA基因检测方法主要为二代基因测序(NGS)。依据国际癌症研究机构(IARC)分类标准[4],BRCA基因变异按照风险程度由高至低,分为以下5类:5类⁃致病性、4类⁃可能致病性、3类⁃意义未明、2类⁃可能良性以及1类⁃良性。
在SOLO1、PRIMA等研究中,PARP抑制剂用于新诊断卵巢癌一线维持治疗,BRCA突变亚组获益明显;在SOLO2、Study19、NOVA等研究中,PARP抑制剂用于铂敏感复发性(PSR)卵巢癌维持治疗,BRCA突变亚组获益明显。
目前,HRD检测尚无统一标准,检测HRD的方法包括寻找HRD形成的原因——HR基因Panel检测,以及寻找HRD造成的影响——基因组瘢痕检测。目前HRD检测有2个比较成熟的技术平台:Foundation Medicine's LOH检测平台和MyriadGenetics myChoice® HRD检测平台。检测HRD导致的基因组不稳定状态包括:杂合性缺失(LOH)、端粒等位基因失平衡(TAI)和大片段迁移(LST)。
LOH实际就是杂合子,一对染色体上某一个染色体上基因缺失,与之配对的染色体仍然存在。ARIEL2研究[5]中,应用LOH百分比作为评价HRD的指标,结果发现BRCA突变亚组和LOH high亚组的PFS较LOH low亚组显著延长,mPFS分别为12.8个月对5.2个月 (HR 0.27, 0.16–0.44, P<0.0001),以及5.7个月对5.2个月 (HR 0.62, 0.42–0·90, P=0.011)。端粒等位基因失平衡是另一种基因组疤痕。Nicolai J等人的研究[6]表明,TAI与DNA损伤修复缺陷相关(与BRCA突变相关),可以预测铂类药物敏感性。LST是指相邻区域的染色体断裂≥10Mb的断点, 排除所有≤3Mb的变异,也是反映基因修复瘢痕的方式。Tatiana Popova等人的研究[7]表明,LST评分在BRCA功能缺失情况下会升高。MyriadGenetics myChoice®HRD检测平台主要针对基因组不稳定状态的3项指标在肿瘤样本中出现的数量进行综合评分:若分值≥42分或BRCA1/2突变,则定义为HRD阳性;若分值<42分,且BRCA为野生型,则定义为HRD阴性。多项研究表明,HRD阳性卵巢癌患者对PARP抑制剂维持治疗获益显著,而HRD阴性人群获益有限。目前,多数研究应用MyriadGenetics myChoice®检测平台的HRD评分进行基因瘢痕的检测,来预测PARP抑制剂的治疗疗效。
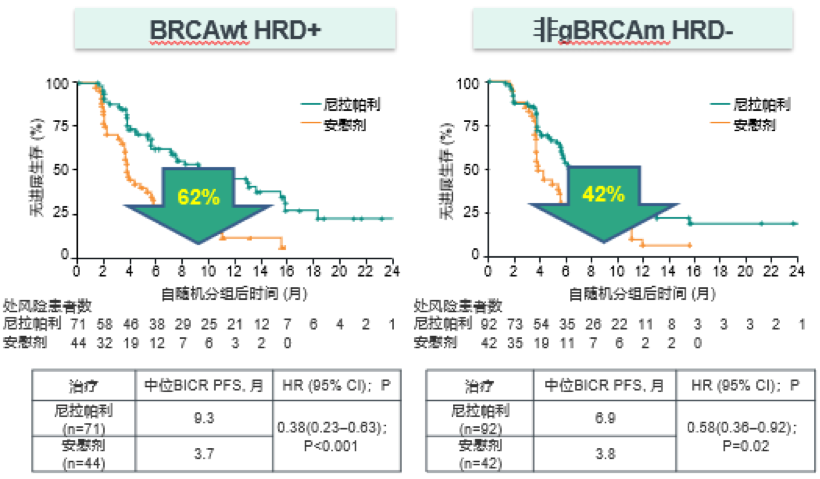
NOVA研究[8]是尼拉帕利对比安慰剂用于PSR卵巢癌的III期临床研究,非胚系BRCA突变(non-gBRCAm)/HRD+患者mPFS延长5.6个月(9.3个月对3.7个月),复发或死亡风险降低62%(HR=0.38,95%CI: 0.23-0.63,P<0.001);non-BRCAm/HRD-患者mPFS延长了3.1个月(6.9个月对3.8个月),复发或死亡风险降低了42%(HR=0.58,95%CI: 0.36-0.92,P=0.0226)。
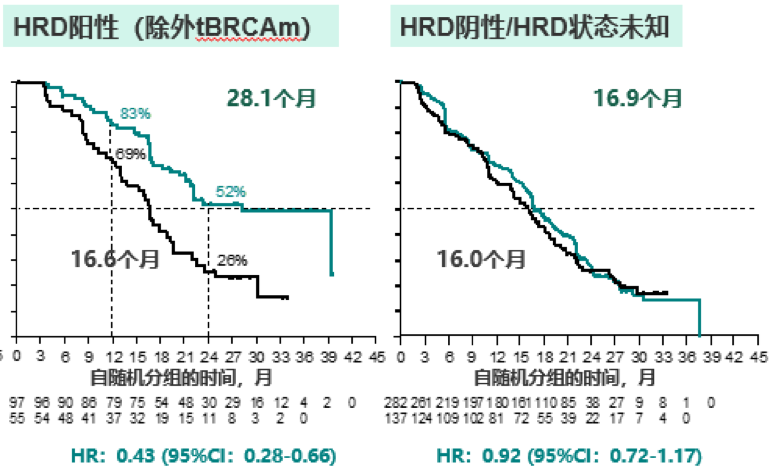
PAOLA-1研究[9]探索了一线含铂类药物联合贝伐珠单抗治疗有效的晚期上皮性卵巢癌(EOC)患者,在继续应用贝伐珠单抗维持治疗的同时加用或不加用奥拉帕利的疗效。双药联合治疗体系BRCA野生型(tBRCAwt)/HRD+患者mPFS延长了11.5个月(28.1个月对16.6个月),复发或死亡风险降低了57%(HR=0.43,95%CI: 0.28 ~ 0.66);双药联合治疗tBRCAwt/HRD-或未知患者mPFS时间延长了0.9个月(16.9个月对16.0个月),复发或死亡风险降低了8%(HR=0.92,95%CI: 0.72-1.17),差异无统计学意义。
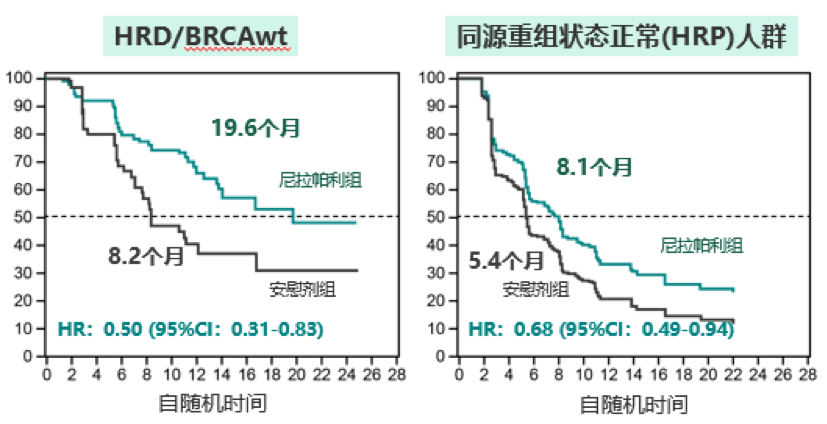
PRIMA研究[10]中,将新诊断的晚期卵巢癌患者随机分组,两组分别在对铂类化疗产生应答后接受尼拉帕利或安慰剂治疗。在BRCAwt/HRD+患者中,尼拉帕利组较安慰剂组mPFS延长了11.4个月(19.6个月对8.2个月),复发或死亡风险降低了50%(HR = 0.50,95%CI : 0.31 - 0.83,P = 0.006);BRCAwt/HRD-的患者中,与安慰剂组相比,尼拉帕利组患者mPFS延长了2.7个月(8.1个月对5.4个月),复发或死亡风险降低了32%(HR = 0.68,95%CI :0.49-0.94,P=0.020)。
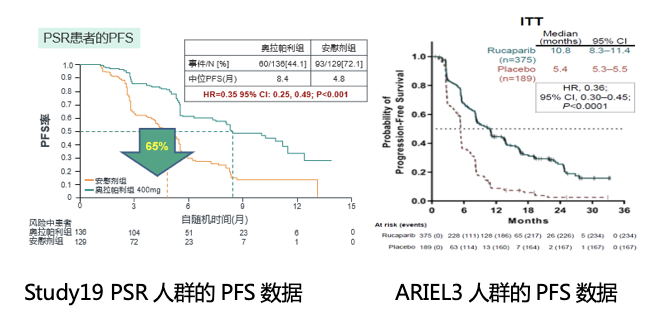
近年来,PARP抑制剂用于PSR卵巢癌维持治疗的研究取得了较大突破,已被公认为铂敏感复发后维持治疗的标准方案。Study19研究[11]中,奥拉帕利维持治疗PSR卵巢癌患者,较安慰剂组mPFS延长了3.6个月(8.4个月对4.8个月),复发或死亡风险降低了65%(HR = 0.35,95%CI :0.25- 0.49,P<0.001)。ARIEL3研究[12]中,卢卡帕利维持治疗PSR卵巢癌患者,较安慰剂组mPFS延长了5.4个月(10.8个月对5.4个月),复发或死亡风险降低了64%(HR=0.36,95%CI: 0.30-0.45,P<0.0001)。
综上所述,基因瘢痕检测HRD有临床试验结果的数据支持,但是仍没有统一的检测标准。此外,铂敏感仍然是目前选择对PARP抑制剂敏感人群的简便指标。NCCN指南[2]以及中国《卵巢癌PARP抑制剂临床应用指南》[13]均推荐奥拉帕利、尼拉帕利和卢卡帕利用于含铂化疗方案达到完全缓解(CR)或部分缓解(PR)的铂敏感复发患者的维持治疗。
参考文献
[1] McLornan D P, List A, Mufti G J. Applying synthetic lethality for the selective targeting of cancer[J]. New England Journal of Medicine, 2014, 371(18): 1725-1735.
[2] NCCN Guidelines Version 1.2019 Epithelial Ovarian Cancer / Fallopian Tube Cancer / Primary Peritoneal Cancer.
[3] Konstantinopoulos P A, Ceccaldi R, Shapiro G I, et al. Homologous recombination deficiency: exploiting the fundamental vulnerability of ovarian cancer[J]. Cancer discovery, 2015, 5(11): 1137-1154.
[4] Plon S E, Eccles D M, Easton D, et al. Sequence variant classification and reporting: recommendations for improving the interpretation of cancer susceptibility genetic test results[J]. Human mutation, 2008, 29(11): 1282-1291.
[5] Swisher E M, Lin K K, Oza A M, et al. Rucaparib in relapsed, platinum-sensitive high-grade ovarian carcinoma (ARIEL2 Part 1): an international, multicentre, open-label, phase 2 trial[J]. The lancet oncology, 2017, 18(1): 75-87.
[6] Birkbak N J, Wang Z C, Kim J Y, et al. Telomeric allelic imbalance indicates defective DNA repair and sensitivity to DNA-damaging agents[J]. Cancer discovery, 2012, 2(4): 366-375.
[7] Popova T, Manié E, Rieunier G, et al. Ploidy and large-scale genomic instability consistently identify basal - like breast carcinomas with BRCA1/2 inactivation[J]. Cancer research, 2012, 72(21): 5454-5462.
[8] Mirza M R, Monk B J, Herrstedt J, et al. Niraparib maintenance therapy in platinum - sensitive, recurrent ovarian cancer[J]. New England Journal of Medicine, 2016, 375(22): 2154-2164.
[9] Ray-Coquard I, Pautier P, Pignata S, et al. Olaparib plus bevacizumab as first-line maintenance in ovarian cancer[J]. New England Journal of Medicine, 2019, 381(25): 2416-2428.
[10] González-Martín A, Pothuri B, Vergote I, et al. Niraparib in patients with newly diagnosed advanced ovarian cancer[J]. New England Journal of Medicine, 2019, 381(25): 2391-2402.
[11] Ledermann J, Harter P, Gourley C, et al. Olaparib maintenance therapy in platinum-sensitive relapsed ovarian cancer[J]. New England Journal of Medicine, 2012, 366(15): 1382-1392.
[12] Coleman R L, Oza A M, Lorusso D, et al. Rucaparib maintenance treatment for recurrent ovarian carcinoma after response to platinum therapy (ARIEL3): a randomised, double-blind, placebo-controlled, phase 3 trial[J]. The Lancet, 2017, 390(10106): 1949-1961.
[13] 鹿欣, 姜洁, 李宁, 等. 卵巢癌 PARP 抑制剂临床应用指南[J]. 现代妇产科进展, 2020, 29(5): 321-328.
审批号:MI-OLA-0050-CN
本资讯由默沙东医学团队提供旨在用于医学专业人士间的学术交流,请勿随意转发或转载。文中相关内容不能以任何方式取代专业的医疗指导,也不应被视为治疗建议。医学专业人士对文中提到的任何药品进行处方时,请严格遵循该药品在中国批准使用的说明书。默沙东不承担相应的有关责任。
查看更多