查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





亲爱的读者朋友,您的意见对我们非常重要!为了更好地了解您的需求,提升文章内容质量,诚邀您花几分钟参与本次有奖问卷调研。参与者有机会获得精美奖品!

上期回顾

内镜黏膜下剥离术(ESD)作为消化道早癌及癌前病变的微创治疗金标准,其技术核心在于“精准切除”的动态平衡。其中,在ESD中掌握两项最关键的技术非常重要,即精准的“止血技术”和高超的“缝合技术”。据文献统计,胃ESD术中急性出血发生率达2.9%~22.2%,术后迟发性出血率为 4.1%~11.8%,尤其胃上2/3区域因黏膜下血管粗大,出血风险显著升高。本文结合最新临床证据,系统梳理ESD止血的关键策略。
有效的黏膜下注射可形成“液体垫”,能够隔离血管并减少剥离损伤。传统生理盐水注射吸收快速,推荐使用甘油果糖或可溶性止血绫混合液(如1%肾上腺素+生理盐水+可溶性止血绫),不仅延长抬举时间(30 分钟内隆起高度维持3.3 mm以上),还可通过物理屏障减少术中渗血(动物实验显示出血量降低34%)。对于直径>40 mm的病灶,建议分点注射,避免抬举不均导致的血管暴露。
术前需评估病灶位置(胃上2/3、贲门区)、形态(隆起型>凹陷型>平坦型)、抗栓药物使用(双联抗血小板增加3.9 倍的出血风险)及患者凝血功能。对长期服用抗凝药者,建议术前5~7 天暂停,并桥接低分子量肝素,术后48 小时重启PPI 治疗。
原则:预止血>即时止血,精准电凝>盲目夹闭。
沿标记点外侧切开黏膜时,采用“由浅入深”法,边切边凝。发现直径>0.5 mm 的裸露血管,立即用电凝刀前端接触止血(功率 20~30W,强凝模式),避免“一刀切穿”导致喷射性出血。胃底静脉曲张区域,优先使用止血钳预凝(常采用软凝模式),钳夹血管后脉冲式电凝,减少热扩散。
(1)小血管渗血:透明帽辅助下生理盐水冲洗(含8 mg/L 去甲肾上腺素),暴露出血点后刀头前端凝固(功率30-40W),适用于直径<1 mm 的血管。
(2)活动性出血(动脉性):立即用止血钳钳夹提拉,采用 “先凝后切” 策略 —— 电凝功率 30-40W,直至血管闭合(可见灰白色凝固带),再离断血管。若术中出现大出血,先用注水冲洗后保持视野清晰的瞬间,立即用止血钳钳夹出血处血管后止血(见视频1)。若视野模糊,无法继续止血,可切换可重复开闭止血夹,通过多次调整夹闭位置,避免影响后续剥离。
视频 ESD术中出血止血术
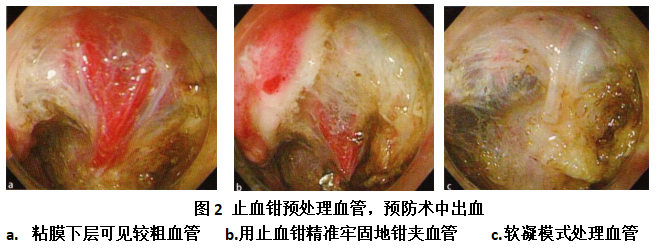
(3)难以暴露的深在血管或瘢痕处的粗大血:采用止血钳边凝边切开的模式,预防术中大出血,并精准止血。
剥离完成后,对所有可见血管实施 “地毯式” 处理:直径<1mm 的血管用电凝刀头滑动凝闭;直径>1mm 或裸露肌层的血管,止血钳 “8 字缝扎” 电凝;对于剥离深度达固有肌层(E3)或怀疑穿孔的创面,金属夹连续缝合(如 Over-the-Scope Clip),闭合同时加固止血。
退镜前采用“抽吸凝血法”:用内镜吸引器头轻压创面,观察5 分钟无渗血,可降低迟发性出血率76%(P=0.032)。对胃角、贲门等易摩擦部位,喷洒纤维蛋白胶,或止血粉形成物理屏障。
术后48 小时内静脉推注 PPI(如艾司奥美拉唑 80 mg),随后8 mg/h持续输注72 小时,维持胃内pH>6。高危患者(如联用抗栓药、CrCl<30 ml/min)联合口服聚普瑞锌,促进溃疡愈合。
术后 24~48 小时为高发期,若出现呕血或血红蛋白下降>20 g/L,立即急诊内镜。首选止血钳二次电凝,对复发出血的裸露血管,联合止血夹+尼龙绳荷包缝合。极少数内镜失败病例,须介入栓塞(IVR)或外科手术。
优先夹闭穿孔,再处理血管。可采用“三明治夹闭法”:先夹闭穿孔边缘,再对出血点电凝,最后加固夹子。
避免热凝,直接用大口径止血夹(如 Resolution 360)闭合血管,联合组织胶注射。
全程使用冷止血技术(如机械夹闭、止血绫喷洒),减少热损伤。
ESD 的止血艺术,在于“预判-精准-微创”的闭环管理。术者需结合病灶特征(位置、大小、深度)、器械特性(热效应、闭合能力)及患者状态(凝血功能、基础疾病),制定个体化方案。未来,随着智能内镜(如 AI 血管识别)和新型材料(可降解止血夹)的发展,ESD止血将向“零出血” 目标迈进。
ESD中的缝合技巧 | 中日携手・遵医领航⑨
作者:遵义医科大学附属医院 王海波

查看更多