查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





3月28—31日,2026年世界肾脏病大会(WCN)在日本横滨举行。本次会议亮点纷呈,高影响力临床研究专场备受瞩目,其中,由南方医科大学南方医院侯凡凡院士领衔、杨小兵教授主会场汇报的HR19042治疗原发性IgA肾病关键临床试验,成为中国原创研究的重要亮点。
作为肾病与泌尿系统疾病国家临床医学研究中心,南方医院肾内科在侯凡凡院士带领下,长期引领我国肾小球疾病临床研究与转化应用,具备国际一流药物试验的研究设计、执行与质控能力。
本次HR19042胶囊Ⅱ/Ⅲ期试验为国内多中心、随机、双盲、安慰剂对照研究,纳入经肾活检确诊、优化标准治疗后仍持续蛋白尿的原发性IgA肾病患者,旨在评估新型肠道靶向制剂对蛋白尿、肾功能作用。

研究背景
IgA肾病是目前世界范围内最常见的原发性肾小球疾病,也是慢性肾脏病和肾功能衰竭的主要原因[1]。IgA肾病的发病机制复杂,研究认为,在回肠末端派尔集合淋巴结会产生半乳糖缺乏型IgA1抗体,参与IgA肾病的发病过程[2]。传统治疗以生活方式干预、血压控制与降蛋白尿药物为主,难以从发病机制层面阻断疾病进展。
HR19042胶囊是中国国内自主研发的一款新型肠道靶向释放布地奈德制剂,允许布地奈德在不被吸收的情况下通过胃和肠道,仅在到达回肠末端时才快速释放,将药物集中递送至派尔集合淋巴结。靶向释放的布地奈德将于该处集中发挥抑制黏膜免疫的作用,以减少异常IgA的产生,进而防止IgA免疫复合物形成并沉积于肾脏系膜区引起后续损伤。本研究为HR19042胶囊治疗IgA肾病患者的Ⅱ/Ⅲ期临床试验,旨在评价在RAS阻滞剂治疗基础上,HR19042胶囊相较于安慰剂治疗原发性IgA肾病的有效性和安全性。

研究设计
本研究为随机、双盲、多中心、安慰剂对照的Ⅱ/Ⅲ期临床试验。
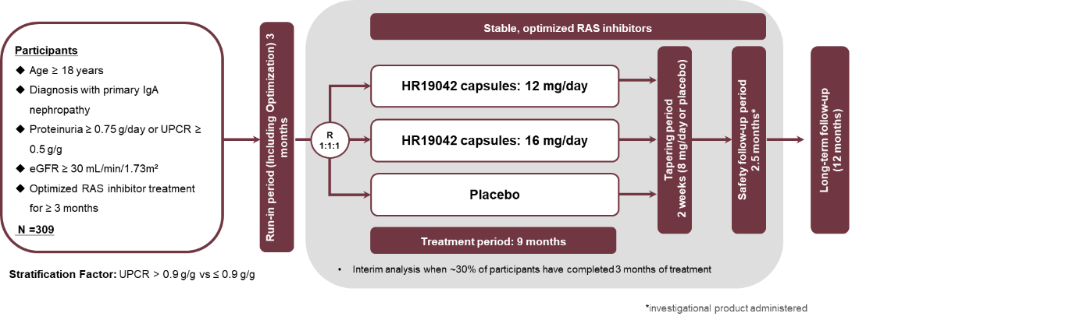
研究对象
纳入≥18岁、经肾活检确诊原发性IgA肾病患者,且满足:经优化肾素-血管紧张素系统(RAS)阻滞剂治疗≥3个月,24小时尿蛋白定量≥0.75 g或尿蛋白/肌酐比值(UPCR)≥ 0.5 g/g;估算肾小球滤过率(eGFR)≥30 ml/(min・1.73m²)。
分组与干预
研究实际入组316例受试者,按照1:1:1随机分为三组,在RAS阻滞剂稳定治疗基础上,试验组口服HR19042胶囊12mg或HR19042胶囊16mg,每日1次;对照组给予匹配安慰剂,每日1次,总治疗期9个月。
为了避免长期应用糖皮质激素突然停药引起的肾上腺皮质功能不全的风险,治疗期结束后进行2周减量期给药。试验组口服HR19042胶囊8mg,每日1次;对照组给予匹配安慰剂,每日1次。随机分层因素为基线UPCR水平(≤0.9 g/g vs >0.9 g/g)。
研究终点
主要终点:9个月UPCR较基线的变化以及12个月eGFR较基线的变化。
次要终点:24个月内的年化eGFR总斜率,9个月的24小时尿蛋白定量的变化,9个月的尿白蛋白/肌酐比值(UACR)的变化等。
安全性终点:不良事件、严重不良事件等。

研究结果
基线数据
本研究实际入组316例受试者,HR19042胶囊12 mg组106例,HR19042胶囊16mg组和安慰剂组各105例,所有随机的受试者均接受了试验治疗。
HR19042胶囊12mg组、16mg组和安慰剂组受试者基线UPCR的中位值分别为1.0g/g、0.95g/g和0.98g/g,24小时尿蛋白定量分别为1.25g/24h、1.16g/24h和1.24g/24h,基线eGFR平均值分别为77.2mL/(min·1.73 m2)、78.7mL/(min·1.73 m2)和 81.0mL/(min·1.73 m2)。
各组的人口学和基线特征基本均衡,符合经优化的RAS阻滞剂治疗后仍存在进展为终末期肾病风险的患者特征。
主要疗效终点
1.降低蛋白尿
治疗9个月后,与安慰剂组相比,HR19042胶囊12mg组、HR19042胶囊16mg组UPCR分别降低40.9%(95% CI:28.1%,51.3%)和47.7%(95% CI:36.4%,56.9%),均具有统计学显著性意义(单侧P值< 0.0001)。
图2 [3]UPCR较基线变化
2.延缓eGFR下降
第12个月,HR19042胶囊12mg组、HR19042胶囊16mg组和安慰剂组eGFR较基线变化值的最小二乘均值(LSM)分别为 -1.06 (95% CI:-3.03, 0.90)、0.85(95% CI:-1.08, 2.78)、-4.37(95% CI:-6.36, -2.37)mL/(min·1.73 m2)。
与安慰剂组相比,HR19042胶囊12mg组、16mg组12个月eGFR净获益分别为3.30(95% CI:0.50, 6.11;单侧P值=0.0105)、5.22(95% CI:2.44, 7.99;单侧P值=0.0001)mL/(min·1.73 m2),均具有统计学显著性意义。
图3 [3] eGFR较基线变化
次要疗效终点
24个月内的eGFR年化总斜率:HR19042胶囊12mg组、HR19042胶囊16mg组和安慰剂组24个月内的eGFR年化总斜率的估计值分别为 -1.53、 -0.88、 -3.59 mL/(min·1.73 m2)/年。HR19042胶囊12mg组、16mg组与安慰剂组相比,总斜率分别改善2.06 mL/(min·1.73 m2)/年(95% CI:0.25, 3.88;单侧P值=0.0129)、2.71 mL/(min·1.73 m2)/年(95% CI:0.93, 4.49;单侧P值=0.0015),均具有统计学显著性意义。
9个月的24小时尿蛋白定量的变化: 治疗9个月后, HR19042胶囊12mg组、HR19042胶囊16mg组24小时尿蛋白定量分别降低36.4% 和39.9% ,而安慰剂组则升高0.1%,提示具有明显获益趋势(名义P值< 0.0001)。
9个月的尿白蛋白与肌酐比值(UACR)的变化:治疗9个月后, HR19042胶囊12mg组、HR19042胶囊16mg组和安慰剂组UACR分别降低47.1%、 54.4% 和4.9%,提示具有明显获益趋势(名义P值< 0.0001)。
安全性
HR19042胶囊12mg、16mg治疗组的安全耐受性良好,绝大多数不良事件(TEAE)为轻度至中度,重度TEAE发生率分别为1.9% vs 7.6% vs 1.9%。严重不良事件发生率分别为8.5% vs 10.5% vs 3.8%,导致停药的AE分别为 0.9% vs 3.8% vs 1.0%,无死亡病例。

研究结论
在经优化的RAS阻滞剂治疗后仍存在进展风险的IgA肾病患者中,经9个月治疗,HR19042胶囊可显著延缓eGFR下降,降低尿蛋白,且整体安全性与耐受性良好,为IgA肾病提供了新的靶向治疗选择。
参考文献:
[1]. Rodrigues JC, Haas M, Reich HN. IgA Nephropathy. Clin J Am Soc Nephrol. 2017 Apr;12(4):677-686.
[2]. Barratt J, Rovin BH, Cattran D, Floege J, Lafayette R, Tesar V, Trimarchi H, Zhang H. Why target the gut to treat IgA Nephropathy? Kidney Int Rep. 2020 Aug;5(10):1620-1624.
[3]. Yang X, et al. Efficacy and Safety of a Targeted-Release Formulation of Budesonide (HR19042 Capsules) in Patients with Primary IgA Nephropathy: A Randomized, Double-Blind, Multicenter, Placebo-Controlled Phase 2/3 Trial. Oral. WCN 2026.
来源:南方医科大学南方医院侯凡凡院士团队供稿
查看更多