查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





饮食、营养、活动/运动等生活方式的改变,一定程度上使得肥胖的患病率逐年上升;而随着医学研究的进展,对于肥胖的认识也在不断深化。在最近举行的ObesityWeek 2025大会上,专家们强调了这样一个观点,“肥胖是一种体重调节疾病”。基于这种诊疗新理念,科学家们开始探索更多潜在获益的新靶点,比如胰高血糖素受体(GCGR)等。特别是GCGR/GLP-1R双激动剂等新型药物,已经在多个国际国内学术会议(包括ObesityWeek 2025、AHA 2025及CDS 2025等)上披露了多项研究进展,《国际糖尿病》特邀南方医科大学南方医院薛耀明教授总结最新诊疗理念并分享相关研究数据,以期为受困于肥胖的患者提供新的解决方案。

肥胖是一种体重调节疾病,能量平衡调节成为重要方向
世界卫生组织(WHO)将肥胖症定义为对健康产生不良影响的异常或者过度脂肪蓄积[1]。随着科学研究的不断深入,我们对肥胖的理解也在发生变化:虽然脂肪过多是肥胖的核心特征,但它是持续“能量累积”的结果(能量摄入与消耗之间长期处于不平衡状态),Daniel H.Bessesen教授在ObesityWeek 2025大会表示[2],肥胖是一种体重调节疾病(能量平衡调节疾病);并且随着年龄增长,体重调节遵循逐渐增重的轨迹。
肥胖成因复杂,但均与调节系统改变相关。Daniel H.Bessesen教授认为,消化道似乎在体重调节中起着核心作用[2]。饮食摄入的能量调节是高效减重药物的主要作用机制,这类药物可能会改变人体体重:使用初期,身体似乎处于“营养过剩”状态;一旦体重稳定下来,人体就趋于能量平衡状态。这些高效减重药物的出现,有助于我们更深入地了解系统中哪些部分对体重影响最大,从而开发更具价值的治疗策略[2]。
新星GCG逐渐引起重视,双靶协同带来全新减重策略
在肥胖治疗领域,除了已经应用于临床的胰高糖素样肽-1(GLP-1)受体和葡萄糖依赖性促胰岛素多肽(GIP)受体外,胰高血糖素受体(GCGR)逐渐引起了医学界的研究和重视。Kirk M. Habegger教授在ObesityWeek 2025大会演讲中指出[3],胰高血糖素最初被认为是与胰岛素作用相反的激素,然而这只是它功能的一部分[3,4];随着科学研究的深入,人们发现GCGR激动剂还具有影响脂质代谢、调节能量平衡、影响体脂质量及抑制食物摄入等多方面的作用[3,4]。
这种能量消耗主要来源于肝脏,并且依赖于FXR和FGF21,FGF21对能量消耗和体重减轻的影响依赖于KLB,且起源于中枢神经系统[3]。加上其能够增强饱腹感的特点,使得GCGR激动剂成为治疗肥胖的一个非常有潜力的药物选择[3,4]。那么GCGR联合GLP-1的双靶方案,能否发挥1+1>2的作用?目前也有研究进行了探索,结果发现,GCGR激动剂可增强单/多分子受体激动剂的抗脂肪生成、抗纤维化、能量代谢和血糖调节作用,并能够延长这些作用的持续时间[3]。
其中的Survodutide作为在研创新GCGR/GLP-1R双激动剂的代表,能够协同激活两种受体,具体表现为GLP-1R可促进葡萄糖依赖性胰岛素分泌、延缓胃排空、抑制食欲,通过改善糖代谢与减少食物摄入间接改善肝脏代谢;GCGR可直接作用于肝脏,调节脂肪代谢,促进肝细胞内脂肪酸氧化、减少肝脏脂肪合成、促进肝脏脂肪分解;间接促进脂肪组织的脂肪分解;直接促进糖原分解、糖异生能量消耗[5,6]。GCGR/GLP-1R双激动剂可直接靶向肝脏,通过GLP-1R激动作用(减少能量摄入)与GCGR激动作用(增加能量消耗)相结合,为改善肥胖等代谢疾病患者的代谢健康提供了一种新的治疗策略。
超重/肥胖患者治疗开拓获益新可能
Survodutide已经在一项针对超重/肥胖成人患者的2期临床试验中显示了减重获益:治疗46周后,Survodutide组的平均体重减轻高达18.7%[7]。基于Survodutide的独特机制及前期研究数据,多项3期研究在超重/肥胖患者中进行了减重疗效分析,包括合并或不合并T2DM的超重/肥胖成人患者[7,8],中国超重/肥胖患者[9],以及伴有心血管疾病、慢性肾病或并存风险因素的超重/肥胖患者[10]等。这些临床研究的基线数据已经公布于ObesityWeek 2025大会、AHA 2025年会,以及中华医学会糖尿病学分会年会(CDS 2025)等国内外大型会议;进一步疗效/安全性研究结果预计明年发布,有望为更多肥胖人群治疗开拓多维临床获益新可能[7-10]。
超重/肥胖成人患者
一项在全球14个国家开展的多中心、随机、双盲3期临床试验SYNCHRONIZE-1正在评估Survodutide在超重/肥胖成人患者中的减重疗效、安全性和耐受性。研究纳入身体质量指数(BMI)≥30kg/m2或BMI≥27 kg/m2且合并至少一种肥胖相关并发症的不合并2型糖尿病(T2DM)的患者。入组患者随机分组接受每周一次安慰剂或Survodutide(剂量逐渐增加至3.6 mg或6.0 mg;允许剂量灵活调整),并结合饮食和运动。研究的主要终点为第76周的体重变化百分比以及第76周体重减轻≥5%的患者比例[7]。
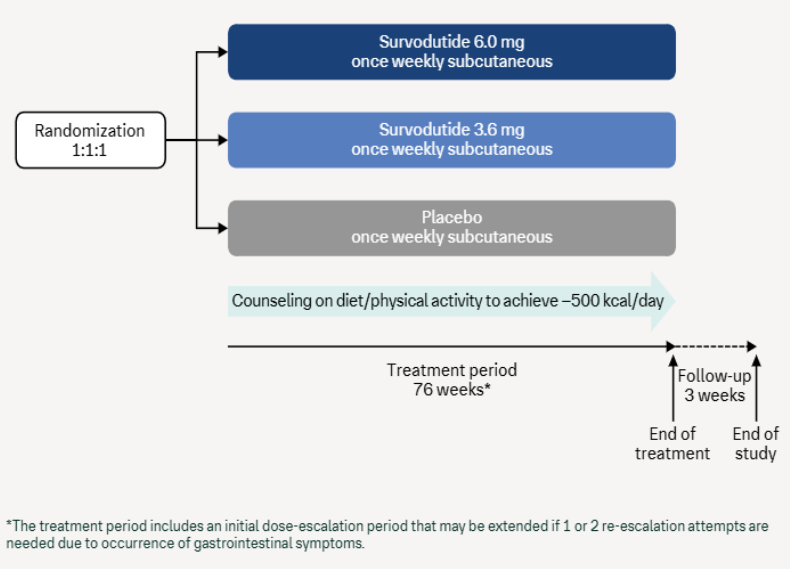
图1. SYNCHRONIZE-1研究设计示意图
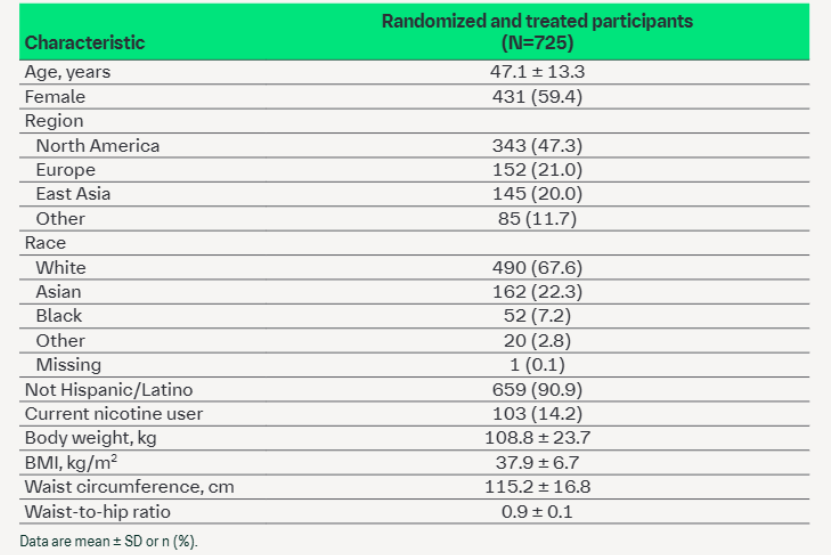
ObesityWeek 2025大会公布了该研究的基线特征(表1)[7]。随机分组并接受治疗的患者(n=725)平均年龄为47.1岁,59.4%为女性(n=431),BMI为37.9 kg/m2,体重为108.8 kg,腰围为115.2 cm。平均糖化血红蛋白(HbA1c)为5.5%,收缩压/舒张压为127.0/82.7 mmHg。大多数患者存在肥胖相关并发症,包括高血压(40.0%;n=290)、血脂异常(33.7%;n=244)、糖尿病前期(30.2%;n=219)、阻塞性睡眠呼吸暂停(18.3%;n=133)、代谢相关脂肪性肝炎(MASH,5.0%;n=36),共有21.8%(n=158)的患者正在服用降脂药物[7]。进一步疗效/安全性分析预计明年发布。
表1. SYNCHRONIZE-1研究患者的基线特征
合并T2DM的超重/肥胖成人患者
与不合并T2DM的肥胖患者相比,合并T2DM的肥胖患者接受减重药物治疗后,体重减轻幅度通常较小。一项在全球19个国家开展的多中心、随机、双盲3期临床试验SYNCHRONIZE-2针对合并T2DM超重/肥胖成人患者评估Survodutide的减重疗效、安全性和耐受性[8]。研究纳入BMI≥27 kg/m2且经降糖治疗后HbA1c为6.5%-10%的患者。入组患者随机分组,接受每周一次安慰剂或Survodutide(剂量逐渐增加至3.6 mg或6.0 mg;允许剂量灵活调整),并结合饮食和运动。研究主要终点均为第76周的体重变化百分比以及第76周体重减轻≥5%的患者比例。
ObesityWeek 2025大会披露了该研究的基线特征(表2)[8]。研究结果显示,752名患者的平均年龄55.7岁,50.7%为女性(n=381),BMI 36.5 kg/m2,体重104.1 kg,腰围115.5 cm, HbA1c 7.4%,收缩压/舒张压为129.8/81.5 mmHg。并发症包括高血压(69.0%;n=519)、血脂异常(67.6%;n=508)、阻塞性睡眠呼吸暂停(17.3%;n=130)、MASH(7.7%;n=58)。合并用药主要包括二甲双胍(78.7%;n=592)、钠-葡萄糖协同转运蛋白2抑制剂(SGLT2i,34.2%;n=257)和降脂药(58.6%;n=441)[8]。进一步疗效/安全性分析预计明年发布。
表2. SYNCHRONIZE-2研究患者的基线特征
中国超重/肥胖患者
中国超重/肥胖诊断标准与WHO不同,既往减重药物在中国人群的证据相对薄弱。SYNCHRONIZE-CN研究针对中国超重/肥胖患者旨在评价Survodutide减重的疗效[9]。这是一项为期76周、全国多中心、随机、双盲、三臂、平行分组、安慰剂对照、优效性、3期临床试验,入组标准更符合中国人群特征:BMI≥28 kg/m2,或BMI≥24 kg/m2并存在至少一种体重相关并发症(高血压;血脂异常;阻塞性睡眠呼吸暂停;心血管疾病;T2DM;MASH)。入组患者在生活方式改变的基础上按照1:1:1随机分配接受每周一次的皮下注射Survodutide或安慰剂治疗,Survodutide通过剂量递增逐步升至3.6 mg或4.8 mg,继而维持至试验结束。主要终点是第52周时体重较基线的变化百分比和较基线体重减轻≥5%的患者比例。
CDS 2025大会公布了该研究的基线特征(图2)[9]。随机分组并接受治疗的患者(n=306)平均年龄为36.9岁,49%为女性(n=150),BMI为33.22 kg/m2,体重为93.9 kg,腰围为105.62 cm,收缩压/舒张压为121.1/82.7 mmHg。大多数患者存在肥胖相关并发症,包括血脂异常(41.5%)、高血压(27.8%)、T2DM(16.7%)、代谢相关脂肪性肝病(9.5%),MASH(5.9%)[9]。进一步疗效/安全性分析预计明年发布。
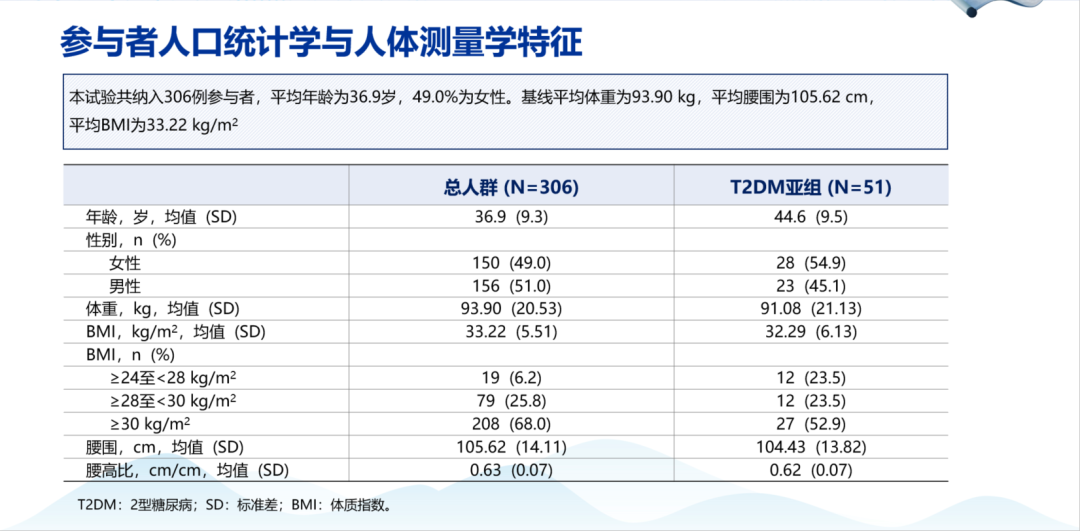
图2. SYNCHRONIZE-CN研究患者的基线特征
伴有心血管疾病、慢性肾病或并存风险因素的超重/肥胖患者
GCGR/GLP-1R的双重激动作用可有效降低体重和脂肪含量,但其心血管作用尚不明确。全球多中心、随机、安慰剂对照的3期临床试验SYNCHRONIZE-CVOT临床研究,旨在验证与安慰剂相比,Survodutide在首次发生主要复合终点事件(定义为5项主要不良心血管事件,包括心血管死亡、非致死性卒中、非致死性心肌梗死、缺血相关冠状动脉血运重建或心力衰竭事件)的非劣效性[10]。研究纳入BMI≥27 kg/m2且合并心血管疾病(CVD),或BMI≥30 kg/m2且合并CVD或慢性肾脏病,和/或≥2种肥胖相关心血管并发症或风险因素。入组患者随机分组,接受每周一次安慰剂或Survodutide(剂量逐渐增加至3.6 mg或6.0 mg;允许剂量灵活调整),并结合饮食和运动。
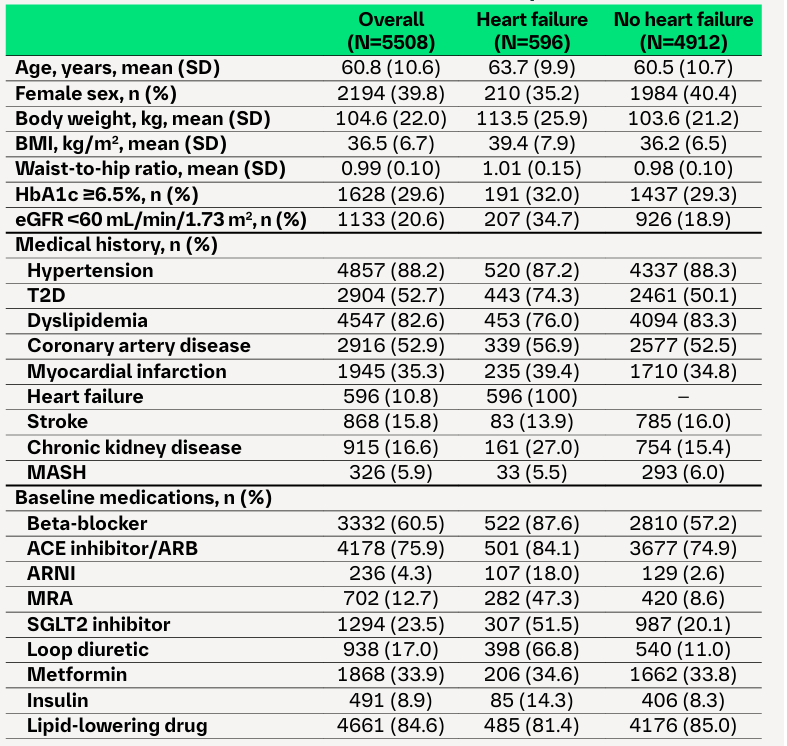
近期举行的AHA 2025大会披露了SYNCHRONIZE-CVOT研究的基线特征(表3)[10]。研究结果显示,随机分组并接受治疗的5508名患者,平均年龄60.8岁,39.8%为女性(n=2194),平均BMI 36.5 kg/m2,596名患者合并心力衰竭,17%的患者有慢性肾脏病,20.6%患者平均估算肾小球滤过率(eGFR) <60 mL/min/1.73 m2。常见的心血管风险因素包括高血压(88.2%)、血脂异常(82.6%)和T2DM(52.7%)。已确诊的CVD包括冠状动脉疾病(53%)、既往心肌梗死(35%)、既往卒中(16%)和心力衰竭(11%)。SYNCHRONIZE-CVOT研究纳入了预先设定的患有心力衰竭的亚组患者。在596名患有心力衰竭(筛选时NYHA分级为II-III级)的受试者中,NT-proBNP中位数为426 pg/ml,堪萨斯城心肌病问卷总症状评分平均值为70.4。基线时,超过一半的心力衰竭患者接受了SGLT2i治疗,66%的患者接受了袢利尿剂治疗。
表3. SYNCHRONIZE-CVOT研究的总体人群和不同心力衰竭状态人群的基线特征
结 语
近年来,我国超重和肥胖人群的患病率呈持续上升趋势,疾病负担沉重,已成为医学界的重要关注话题。目前减重药物的研发进展迅速,尤其是GCGR/GLP-1R双激动剂等新型减重药物的出现,带来“能量平衡”减重新策略,有望在未来为多种类型肥胖人群带来新的治疗选择。期待未来相关研究数据的早日公布,实现改善肥胖等代谢疾病患者的多维临床获益。探
专家简历

审批号:SC-CN-18241
有效期至:2026年11月25日
仅供相关医药专业人士进行医学科学交流
PART
↓↓↓
查看更多