查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





胃癌作为全球范围内发病率和死亡率均居高位的恶性肿瘤,其规范化诊疗对于提高患者生存质量和延长生存期具有至关重要的作用。随着医学科技的进步和对胃癌病理机制的深入理解,胃癌的诊疗已经进入了精准医疗的新时代。规范化诊疗不仅包括早期诊断、手术切除、辅助治疗和个体化治疗,还涉及多学科团队合作、患者管理以及持续的随访和康复。通过整合化疗、放疗、靶向治疗和免疫治疗等多种治疗手段,制定个体化的治疗方案,旨在为每一位胃癌患者提供最合适、最有效的治疗选择。
本期精选一例胃癌病例,特邀宁波市医疗中心李惠利医院董哲斌医师整理病例、虞伟明副主任医师为我们带来精彩点评。
基本信息
患者基本信息
60岁,女性
已婚,离退人员
主诉:发现左侧颈部淋巴结肿大10余天。
现病史:患者10余天前无意间发现左颈部淋巴结肿大,不伴疼痛,皮肤完整无破溃,遂至我院就诊,查颈部CT提示:“双侧颈部、胸廓入口处多发肿大淋巴结,考虑肿瘤转移可能。”查胃镜提示:“胃体CA,(病理未归)。”现患者无腹胀乏力、反酸嗳气,无恶心呕吐、厌食纳差,无腹痛,无腹泻、便秘、呕血、黑便、粘液、脓液便、畏寒、发热、肤黄目黄、胸骨后烧灼感等不适,今为求进一步诊治到我院就诊,门诊拟"胃恶性肿瘤"收住治疗。
既往史:既往体质可,否认肝炎、结核等传染病史,否认冠心病、糖尿病、高血压等“心、肺、肝、肾、内分泌、脑”等脏器重大疾病史,无用药史。
个人史:20余年前于“慈城保利医院”因宫外孕行手术治疗(具体不详);
初中文化,否认“吸毒”史,否认“吸烟”史、“饮酒”史,否认药物成瘾史。
家族史:父母已故,有1哥,有1姐,均体健。否认家族二系三代成员中有遗传病、精神病、肿瘤等类似的疾病史。否认与患者该病相类似病史。
体格检查
皮肤、巩膜无黄染,左侧颈部可触及肿大淋巴结,约1.2cm*1cm大小,质硬,活动度较差, 腹部平坦,无腹壁静脉曲张,无胃、肠型及蠕动波,腹肌软,无压痛,无反跳痛及肌紧张,肝脏肋下未触及,未扪及包块,Murphy氏征阴性,叩诊呈鼓音,移动性浊音阴性,肠鸣音正常,未听及血管杂音。
实验室检查
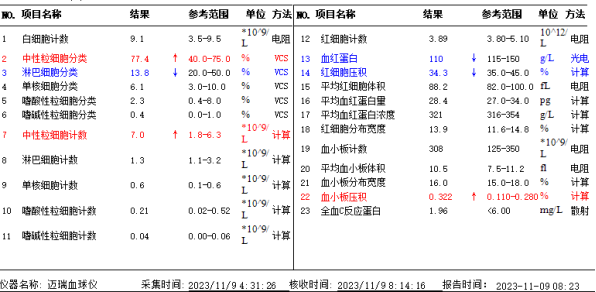
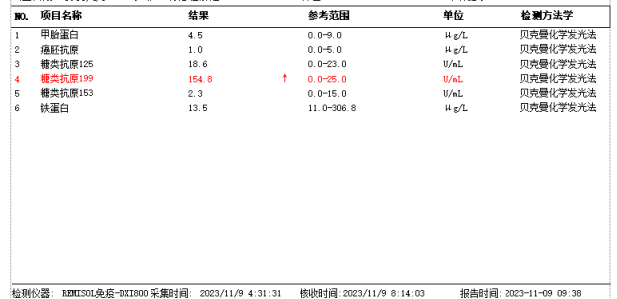
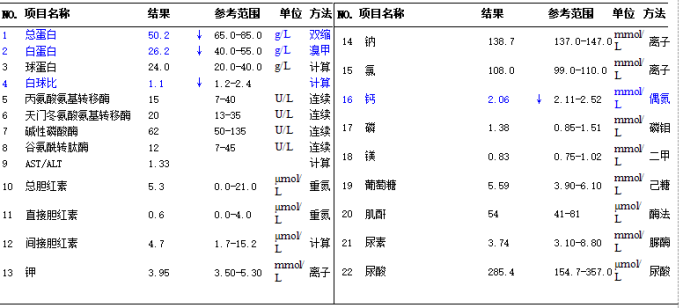
其他辅助检查
检查结论:
甲状腺双侧叶回声增粗(桥本可能)
甲状腺左侧叶结节(TI-RADS:3类)
左侧颈部淋巴结肿大
免疫组化结果:
(左侧颈部淋巴结针吸细胞块)结合免疫组化考虑(胃)腺癌转移。
免疫组化:GATA-3(-),CDX-2(+),Villin(+),Her2 GC(4B5)(3+),CK7(+),CK20(+),TTF-1(克隆号SPT24):(-),MLH1(未缺失),MSH2(未缺失),MSH6(未缺失),PMS2(未缺失)。
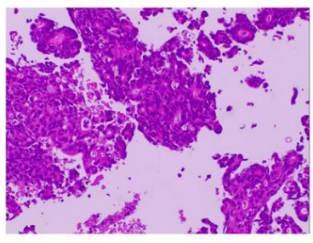
细胞学病理诊断结果:
(左侧颈部淋巴结针吸细胞块)转移或浸润性(腺)癌。
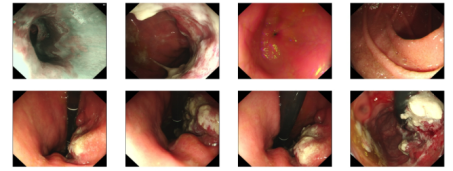
镜检所见:食管黏膜光滑,血管纹理清。
贲门齿状线清晰,开闭可。
胃体小弯侧肿物,大块活检。
胃角黏膜光滑,形态规整,弧度存在,RAC消失。
胃窦黏膜肿胀,红白相间,以红为主。
幽门圆,开闭可。
十二指肠球部及降部黏膜光滑,未见异常。
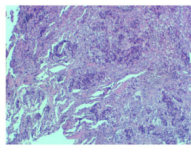
巨检描述:
(胃体粘膜):灰白组织一颗,最大径0.5cm,全取。
病理诊断:
(胃体,活检)低分化(腺)癌。幽门螺杆菌(HP):(-)。
免疫组化结果:
1(蜡块)(胃体粘膜):MLH1(未缺失),MSH2(未缺失),MSH6(未缺失),PMS2(未缺失),Her2 GC(4B5)(3+),CK(pan)(+)
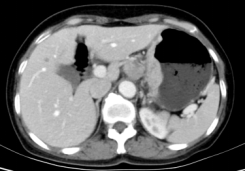
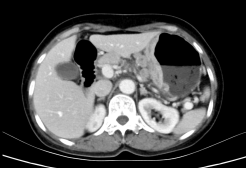
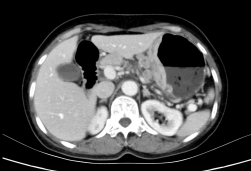
影像诊断及建议:
考虑胃癌,胃周及后腹膜多发肿大淋巴结,建议年度复查。肝囊肿。右肾小囊肿。盆腔少许积液。
病理诊断:(胃体,活检)低分化(腺)癌。
A片:PD-L122C3 CPS=20。(CPS<1为阴性,CPS≥1为阳性)
阳性对照组织:(+);试剂阳性质控:(+)。
待检组织阴性对照:(-);阴性对照组织:(-)。
试剂阴性质控:(-);细胞系质控:合格。
PET-CT报告
影像诊断:
1、胃底、胃体小弯侧占位,FDG摄取异常增高,考虑胃癌,请结合病理。胃周、左侧颈后三角、双肺门、纵隔、双侧膈脚后、腹膜后及右侧髂总动脉旁多发转移性淋巴结。
2、肠系膜多发小斑片灶,FDG摄取未见增高,转移瘤可疑,请随诊复查。盆腔少量积液。
3、左侧胸膜局部增厚,FDG摄取增高,请随诊复查,以除外转移瘤。
4、甲状腺左叶结节,FDG摄取增高,考虑腺瘤可能性大,请随诊复查,以除外甲状腺癌。
5、两肺多发微小结节,FDG摄取未见增高,请胸部CT随诊复查。
6、两肺炎症。双侧乳腺小叶增生。双侧乳腺纤维腺瘤。
7、肝小囊肿。老年子宫。子宫肌瘤。盆腔大小肠慢性炎症。
8、双枕骨蛛网膜颗粒。老年性脑改变。脑白质变性。双侧下鼻甲肥大。双侧筛窦慢性炎症。右侧慢性中耳乳突炎、咽喉炎。
9、脊柱退行性改变。C3~7及L3~S1椎间盘膨突。S2骶管囊肿。双髋关节周围少量积液。
病历摘要
女性,60岁;BMI:1.30
20余年前因宫外孕行手术治疗(具体不详)
查体:左侧颈部可触及肿大淋巴结,约1.2cm*1cm大小,质硬,活动度较差
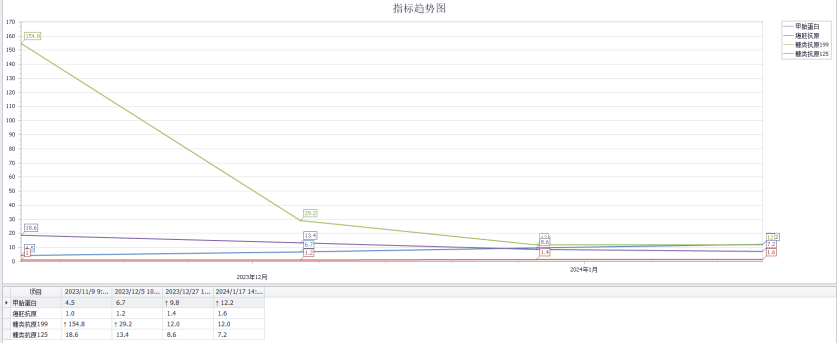
辅助检查:Hb:110g/L、Alb:26.2g/L、CA19-9:154.8U/ml
影像学及病理提示:胃恶性肿瘤(胃体小弯侧,cT4bN3bM1)、伴左锁骨上淋巴结转移、伴全身多发淋巴结转移、小肠系膜转移待排
免疫组化:Her2阳性,pMMR,CPS=20
诊 断
初步诊断
胃恶性肿瘤(胃体小弯侧;cT4bN3bM1)
伴左锁骨上淋巴结及全身多发淋巴结转移
小肠系膜转移待排、低蛋白血症、肝囊肿、右肾囊肿、盆腔积液、营养风险
鉴别诊断
患者胃癌伴淋巴结转移,有病理结果支持,主诊断无需鉴别,需进一步完善检查明确肿瘤全身性情况
治疗方案
患者考虑胃癌伴远处转移,拟行综合抗肿瘤治疗,排除手术禁忌后于2023-11-13局麻下行“输液港置入术”
排除化疗禁忌症,分别于2023-11-14、2023-12-05、2023-12-27行全身静脉治疗,方案为 :“SOX(奥沙利铂150mg+替吉奥40mg bid)+纳武利尤单抗(360mg)+曲妥珠单抗(279mg)”
出院副主用药信息
艾司奥美拉唑:质子泵抑制剂,护胃;
甲钴胺:内源性辅酶B12,预防化疗导致周围神经病变;
复方嗜酸杆菌:肠道益生菌,预防化疗导致肠道菌群失调;
利可君:促进骨髓造血,预防化疗导致血液系统并发症。
预后情况
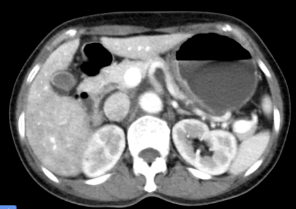
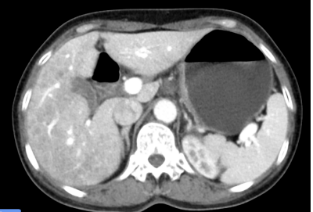
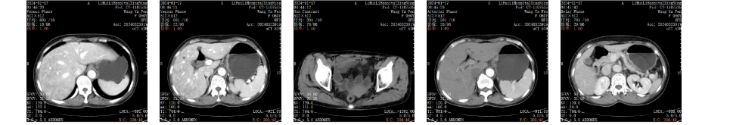
影像诊断及建议:
胃恶性肿瘤伴胃周及后腹膜多发淋巴结转移,对比2023-11-08片病灶明显较前减轻,建议复查。门静脉期肝实质密度强化不均,肝损待排,请结合临床。肝囊肿。右肾小囊肿。子宫后壁肌瘤。
PET-CT报告
影像诊断:
1.a.胃癌并多发转移化疗后,现胃底近贲门处、胃体小弯侧粘膜增厚,FDG代谢轻度增高,考虑肿瘤治疗后改变,肿瘤活性部分抑制,请结合临床。
b.左侧颈后三角区、左侧锁骨上窝片絮影,FDG代谢未见明显异常;纵隔(4R区)、胃周、肝胃间隙、双侧膈角后间隙、腹主动脉周围、右侧髂总动脉旁及肠系膜、大网膜散在淋巴结,FDG代谢未见明显异常,以上考虑均治疗后改变(肿瘤活性部分抑制)合并有部分反应性增生性淋巴结,建议继续随诊;
c.全身未见新发转移灶。
2.a.两肺散在微小实性结节,考虑炎性肉芽肿。
b.纵隔(4R区)淋巴结反应性增生。双侧乳腺增生。
3.喉咽形态、结构未见异常,FDG代谢增高,考虑紧张性摄取。
4.甲状腺密度不均匀减低,甲状腺左叶FDG代谢增高,不除外腺瘤,请结合超声。双侧颈部Ib-III区淋巴结反应性增生。
5.肝S2、S5段小囊肿。
6.胆囊、双肾实质密度均匀增高,考虑碘造影剂残留。
7.部分结肠FDG代谢增高,考虑肠炎。
8.颈椎变直。L3/4、L4/5、L5/S1椎间盘轻度膨出。脊椎退行性变。
后续治疗
患者三次转化治疗后复查提示肿瘤较前明显退缩,转移灶FDG摄取无异常,存在手术指征,排除手术禁忌后于2024-01-24行“腹腔镜探查+胃癌根治术(全胃切除+D2淋巴结清扫+毕II式吻合+Braun吻合)+肠粘连松解术”,术后予抗感染、抑酸、补液、营养等对症支持治疗,术后恢复可。
标本类型:全胃切除术
肿瘤所在部位:胃体小弯侧
大体分型:BorrmannⅢ型(浸润溃疡型)
肿瘤大小:8.5cm ×5 cm ×1cm
组织学类型:管状腺癌
组织学分级:G3/低分化
Lauren分型:混合型
镜下肿瘤浸润深度:侵及浆膜下的结缔组织(未累及脏层腹膜)(T3)
溃疡(瘢痕):(+)

术后患者继续术前治疗方案维持治疗,目前我科定期随访治疗,病情稳定。
专家点评
董哲斌医师点评:本病例中,患者为60岁女性,确诊为胃恶性肿瘤(胃体小弯侧;cT4bN3bM1),伴左锁骨上淋巴结及全身多发淋巴结转移。治疗方案综合考虑了手术与药物治疗的结合,符合当前胃癌治疗的原则。在无法直接手术切除的情况下,先行药物治疗进行转化治疗,待肿瘤缩小后再行手术切除,这一策略是合理的。患者接受了“SOX(奥沙利铂+替吉奥)+纳武利尤单抗+曲妥珠单抗”的全身静脉治疗方案,三周期治疗后,肿瘤明显退缩,转移灶FDG摄取无异常,表明治疗反应良好。此方案针对HER2阳性的胃癌患者,结合了化疗、免疫治疗和靶向治疗,多方位攻击肿瘤,取得了显著的疗效。
本病例提醒我们在治疗晚期胃癌时,需综合考虑患者的整体状况、肿瘤特性及基因表达情况。在无法手术切除的情况下,通过化疗和靶向治疗实现肿瘤的转化,为手术创造条件。同时,免疫治疗的加入为患者提供了额外的治疗选择。此外,患者治疗后的病理结果显示低分化腺癌,提示我们在治疗过程中应密切关注病理变化,及时调整治疗方案。
值得注意的是,尽管新药物和新疗法不断涌现,化疗在胃癌治疗中仍占据重要地位。本病例中,患者对化疗反应敏感,说明在精准医疗指导下,传统化疗仍有其不可替代的价值。未来,随着更多靶向药物和免疫疗法的应用,我们期待能为患者提供更为个性化、更为有效的治疗方案。
虞伟明副主任医师点评:本病例中,患者确诊为胃恶性肿瘤伴多发淋巴结转移,治疗方案综合考量了手术与药物治疗的协同效应。在评估手术指征的基础上,优先采取手术切除的策略是适宜的。对于手术不可切除的情况,依据临床指南先行药物治疗,以期实现肿瘤的转化,为后续手术创造条件,此法符合胃癌治疗的现代原则。
患者确诊时已处于晚期,伴多发转移,初始手术切除不适宜。因此,先行三周期化疗方案,观察到显著的治疗效果,肿瘤标志物得到有效控制。满足手术指征后,采取手术切除,符合肿瘤治疗的根本原则,即彻底移除肿瘤组织以防复发。本病例展示了在晚期胃癌治疗中,综合治疗方案的合理性和有效性。
对于晚期且手术不可切除的胃癌患者,临床治疗需着重考虑在无手术条件下实现肿瘤转化的策略。无论是靶向治疗、化疗还是新辅助治疗,均旨在达到肿瘤降期,为手术创造机会。若患者经治疗后达到病理完全缓解(PCR),则需综合评估维持药物治疗、手术切除或继续观察的方案。当前,尽管新兴药物不断涌现,化疗在胃癌治疗中的核心地位未变,其与手术及其他药物的综合应用策略,对于提高治疗效果具有重要意义。展望未来,随着靶向治疗、免疫治疗及抗体药物偶联物(ADC)等新疗法的发展,预期将为胃癌患者带来更为有效的治疗方法。
患者经过转化治疗后成功进行了胃癌根治术,并继续术前治疗方案作为维持治疗。建议定期随访,密切关注患者的恢复情况和潜在复发风险。影像学检查和肿瘤标志物监测应作为随访的重要组成部分。
查看更多