查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





钟文昭 教授
广东省肺癌研究所 所长
广东省人民医院肺外科 主任医师
广东省肺癌转化医学重点实验室 副主任
广东省抗癌学会 副会长
中国研究型医院学会胸外科专委会副主委
中国医院协会健康医疗大数据专委会常委
获2020年广东省科学技术进步奖一等奖
获2022年中华医学科技奖一等奖
J Thorac Oncol associate editor
Medicine Advance associate editor
2022年IASLC- Naruke Award for surgery
广东省人民医院、广东省肺癌研究所肺外科医师
国际肺癌研究协会(IASLC)成员
18th WCLC International Mentorship Award
18th WCLC Developing Nations Award
WCLC/AATS等国际会议多次壁报及口头汇报
钟文昭教授您好,张潮博士您好。首先我们在此热烈祝贺贵团队研究成果在AATS 2023大会上做口头报告。此前,较少有关于ALK+NSCLC围术期治疗的临床探索,本次贵团队的研究也吸引了大量研究者的目光,能否请您简述一下该研究开展的初衷,及本次报告的数据?
钟文昭教授
ALK融合是肺癌中一类重要的驱动基因,与其他驱动基因常见的点突变、片段缺失不同,ALK融合使肺癌的生物学行为表现得更具侵袭性。ALK融合突变整体发生率约为6%,但考虑到庞大的肺癌患者基数,以及ALK融合突变常发生于年轻患者的特点,它仍是非常重要的一个驱动基因。
另一方面,这部分患者的影像学表现较为隐匿,与之对比,EGFR突变患者的影像学表现通常为磨砂玻璃样的线性进展,有较长时间窗留给医生观察,而ALK融合突变患者的观察时间窗较短,往往一个实性、不典型的病灶会在很短时间内转变为晚期病灶。但针对ALK的靶向药物发展同样很快,目前,一代药物克唑替尼,二代药物阿来替尼、塞瑞替尼、恩沙替尼、布格替尼及三代药物洛拉替尼都已经在国内上市,为原本预后较差的ALK融合患者带来了生存期的极大改善。
由于ALK融合突变高度依赖ALK通路,因此在通过靶向药物进行抑制后,将取得很好的疗效。一代药物克唑替尼就已经取得了很高的有效率,但是对晚期患者的无进展生存期(PFS)还不够理想,而第二代ALK-TKI阿来替尼在全球Ⅲ期临床研究ALEX中取得了34.8个月的中位PFS,这一数据即便是第三代EGFR-TKI也难以达到,针对亚洲患者的Ⅲ期研究ALESIA研究中的中位PFS达到41.6个月;此外,由于阿来替尼的血脑屏障透过性较好,而约20%~60%的ALK+NSCLC患者都可能出现脑转移,阿来替尼对于这部分患者的脑转移也可起到很好的抑制作用,有效降低脑转移发生、进展的风险。因此,ALK融合突变如今被视为黄金突变,即便患者已经发展至中晚期,仍然可通过靶向治疗获得很好的生存。这部分患者在ALK-TKI的治疗下,将有望真正实现长期慢病化管理,甚至有部分患者能达到pCR。
前面提到的是靶向治疗为Ⅳ期患者带来的生存改善,即出现远处转移的患者。还有很大一部分患者未发生远处转移,但出现了局部的肿瘤侵犯或淋巴结转移,包括肺门、纵隔、锁骨上淋巴结转移等,对于这部分局晚期患者而言,仍然具有潜在的根治性治疗可能。
考虑到ALK+NSCLC是一种全身性疾病,对于局晚期患者的治疗,系统治疗同样排在首位。我们希望通过系统治疗将肿瘤降期,再采取手术、放疗等手段进行局部干预,使这部分患者得到潜在临床治愈的机会。特别是对于年纪较轻的患者,虽然在靶向治疗的帮助下可以达到长期生存,但很多患者都在关心能否达到完全治愈,在经过系统治疗与局部治疗后,将血液中肿瘤的ctDNA清零,接受手术根治,这也是我们开展研究的初衷。
不过,由于ALK融合发生率较低,难以开展前瞻性研究,因此我们首先从个案病例报道或小样本量多中心回顾性研究入手,整理严谨的研究数据,对肺癌患者的数据进行连续的密切监测,包括术前、术中、术后的血液样本、组织样本等,并得到了初步的数据,下面由张潮博士进行这些数据的分享。

张潮博士
我中心开展这项ALK新辅助治疗研究主要出于两个初衷:其一,在既往大样本量研究,如纪念斯隆-凯特琳癌症中心(MSKCC)开展的研究中,我们观察到ALK融合突变患者,即便接受根治性切除,整体预后也还要较EGFR突变患者更差。其二,对于驱动基因阳性患者,在早期或局晚期围术期治疗中靶向治疗的应用缺乏足够的循证医学证据,包括我中心之前开展的CTONG 1103研究,即便观察到围术期靶向治疗可为患者带来无病生存期(DFS)获益,但却未到达总生存期(OS)的临床终点,因此结论提示并不支持对EGFR突变NSCLC患者开展新辅助靶向治疗。
另外,我们也考虑到针对驱动基因阳性晚期患者,ALK-TKI可以取得远优于EGFR-TKI的疗效,因此我们尝试在ALK+NSCLC患者中应用新辅助靶向治疗,探索能否为患者带来更好的预后。
我们最早于2020年进行了尝试,患者是一例T3N2M0 Ⅲb期男性患者,ALK融合阳性,我们于术前对患者进行了两个周期(56天)的阿来替尼新辅助治疗。两个周期后,我们通过影像学检查观察到肿瘤的明显缩小,接近50%。术后,我们对切除肿瘤进行病理检测,发现达到MPR,仅剩约7%的肿瘤细胞。基于这样成功的案例,以及此前在EGFR+NSCLC患者中进行探索的经验,我们有序开展了ALK+NSCLC患者的资料搜集,并于本次AATS 2023年会进行了公布。
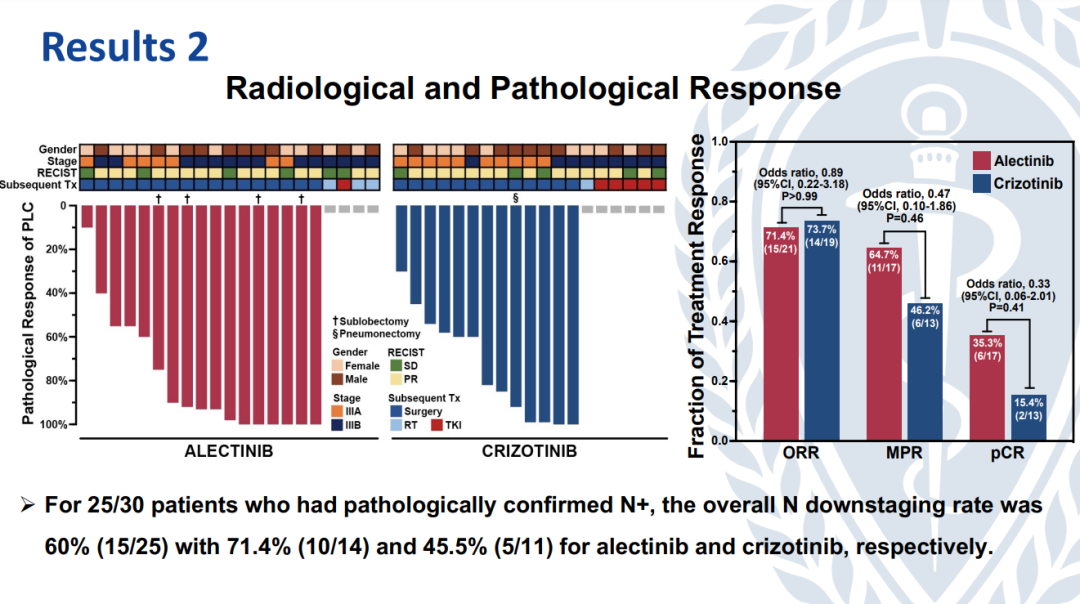
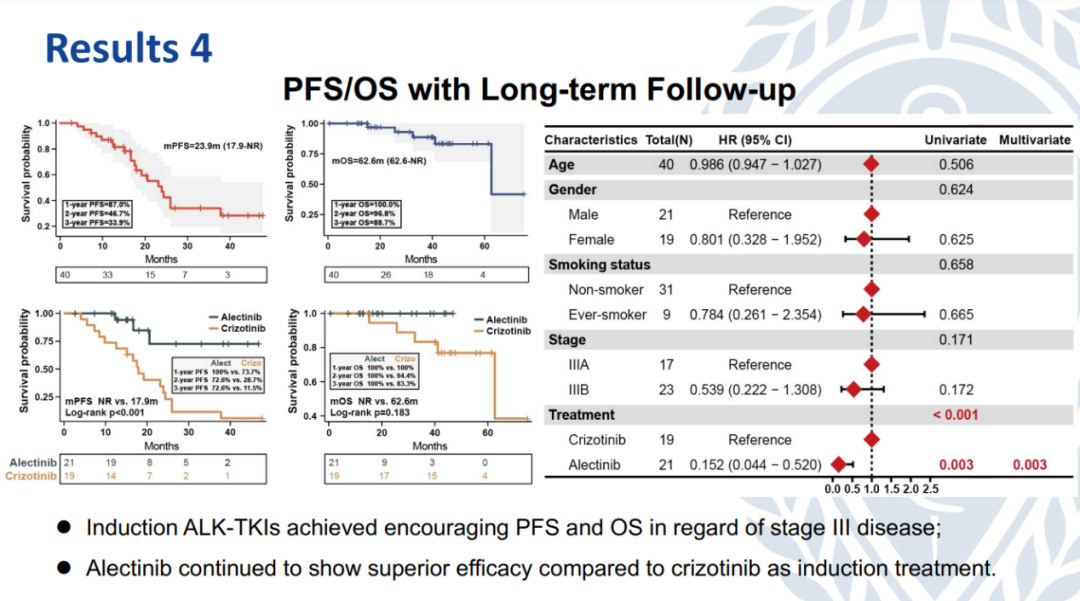
本次公布数据总计纳入了40例患者,其中21例接受了阿来替尼的新辅助治疗,19例接受了克唑替尼新辅助治疗,两组患者的影像学缓解未有显著差别,但接受阿来替尼新辅助治疗的患者的MPR率与pCR率更高。40例患者中有30例接受了外科手术,其中25例患者在术前病理检测中已发现转移,在这部分患者中,接受阿来替尼与克唑替尼治疗的淋巴结降期率分别达到71.4%和45.5%。术后,经过中位三年的随访,目前看来,接受围术期阿来替尼新辅助治疗的患者较接受克唑替尼治疗的患者取得了更好的预后,从围手术期TKI治疗后的复发模式及后续治疗分析看来,这部分患者的病理缓解率、颅脑转移控制率均更高。值得关注的是,接受围术期克唑替尼治疗的患者,超过60%都在术后出现了孤立性脑转移或合并其他部位的远处转移。这也提示阿来替尼的围术期治疗可以更好地改善ALK+NSCLC早期患者的预后。

目前,国际上也开展了多项针对ALK+NSCLC早期患者的靶向治疗研究。例如伞式研究NAUTIKA1,我们曾与其研究人员进行交流,该研究预计将于WCLC进一步公布扩展队列相关数据。此外,今年ESMO大会上,ALINA研究也将公布数据,这是全球首个阿来替尼头对头对比标准术后辅助治疗的Ⅲ期随机对照研究。这些研究的公布有望进一步佐证ALK-TKI应用于早期ALK+NSCLC患者新辅助治疗、辅助治疗的临床价值。

图2. 张潮博士在103rd AATS年会
您认为ALK+NSCLC围术期治疗的最佳模式会是什么?如何确定最佳治疗周期?
张潮博士
既往在CTONG 1103研究中,我们发现单纯两个周期的新辅助治疗,药物暴露时间不一定足够,因此我们进行了更长时间的新辅助治疗尝试。一些海外研究针对ALK+NSCLC都采取了更长时间的两周期56天治疗模式,例如意大利ALINO研究就采取了术前两周56天,术后2年辅助治疗的模式,NAUTIKA1研究也采取了类似的治疗模式。
治疗周期的延长是否可以提高患者的MPR率与pCR率,目前根据我们的研究看来,的确存在这样的趋势。患者接受治疗越久,MPR率,pCR率可能会更高,但并没有显著的统计学差异。另外,我们也需考虑长时间新辅助治疗对后续手术难度的影响,根据NAUTIKA1研究于去年WCLC公布的数据看来,接受两个周期阿来替尼治疗的患者,中位手术时间约为4小时,但既往接受免疫联合化疗新辅助治疗模式的患者,中位手术时间仅为3小时。基于现有的前瞻性研究数据及我们的临床经验直观看来,ALK-TKI治疗后的患者由于肺门淋巴结的粘连,可能会导致手术的难度上升。
因此,目前最佳的围术期治疗周期有待商榷,两周期56天的治疗周期是考虑到ALK-TKI在晚期治疗中约1个月的中位起效时间,以这样的周期可以更大概率地涵盖尽可能多的患者,达到比较好的效果,但进一步延长能否为患者带来更多获益,则需要综合手术难度的增加进行权衡。目前我们也有开展三周期治疗的前瞻性研究,期待更多的数据公布以后可以得到更加直观的结果。
钟文昭教授
根据目前有限的证据看来,三个周期可能是更好的治疗选择,当然,新辅助治疗对于手术难度的影响也是很多外科医生关心的问题。但与免疫治疗相比,靶向治疗确实由于作用机制的不同,对pCR率、降期率、淋巴结降期等的影响不同,因此对于手术难度的影响也存在差异,目前很多医生都在进行相关的研究。
您提到ALK-TKI可能对患者的手术难度造成影响,那么在新辅助治疗后,是否可以选择其他局部治疗方案以代替手术,例如放疗?
张潮博士
新辅助治疗后的局部治疗方案选择是一个有趣的话题。手术治疗对于患者的获益到底有多大影响?实际上,即便接受了新辅助治疗,接受手术后,患者依然有较大的术后复发风险,而对于ALK+NSCLC患者而言,即便是晚期患者,接受ALK-TKI的治疗可以在真实世界中获得超过80个月的中位生存时间。对于这部分晚期患者来说,ALK-TKI的治疗意义远大于局部治疗。
以目前我中心数据看来,无论患者接受克唑替尼还是阿来替尼治疗,是否接受手术,总体在PFS层面确实没有明显差异,而在OS层面,接受手术治疗的患者会有一定的获益倾向,但未观察到显著的统计学差异。
当然我们现在也有在开展一些更深入的研究者发起的临床研究(IIT),在Ⅲ期患者中纳入了初始可手术切除与不可手术切除的患者,采用固定短周期ALK-TKI治疗后,多学科评估患者是否适合接受放疗或手术治疗。
在EGFR+NSCLC中,不同的突变形式对于药物的反应不同,使得药物的选择需根据具体突变亚型进行指导,那么您认为ALK突变的异质性是否会对治疗方案产生影响?
张潮博士
ALK变异较为复杂,除驱动基因外也有很多不同的长效基因,我们也曾探索不同ALK突变的患者对于治疗的反应。从晚期数据看来,ALK+NSCLC患者接受ALK-TKI治疗,整体表现是获益,可能由于ALK+NSCLC肿瘤非常依赖ALK通路,因此不会出现类似EGFR+NSCLC患者那样因基因突变的异质性影响治疗的反应。此前,一些研究者开展过针对EGFR+NSCLC患者的研究,包括对于早期EGFR突变患者多区域的测试分析,确实发现早期EGFR突变患者的肿瘤存在较大异质性。但目前看来,ALK+NSCLC肿瘤并未出现如此大的异质性,结合目前一些ALK合并伴随突变的相关研究看来,ALK突变的异质性尚未影响到对治疗药物的选择。
而且目前二代、三代ALK-TKI的疗效提升较大,即便存在异质性的影响,也难以抹消二代、三代ALK-TKI与一代ALK-TKI的疗效差异。因此目前我们并不考虑根据伴随突变指导TKI的选择。此前我们对于ALEX研究的分析也指出,不同ALK融合亚型对于克唑替尼的疗效存在影响,但对阿来替尼的影响较小,考虑到克唑替尼对于颅脑病灶的控制效果不是太好,目前晚期临床实践中以二代、三代ALK-TKI为主,因此在围术期治疗中,我们也不会根据ALK突变的形式选择药物。
最后,您对于ALK+NSCLC围术期治疗的探索还有哪些期待?
张潮博士
目前,对于ALK+NSCLC的围术期随机对照临床研究开展,最大问题在于这部分患者比例较低。我此前曾经与NAUTIKA 1研究北美负责人进行过交流,探讨是否可通过现有单臂研究、Ⅱ期临床研究及真实世界数据,推动FDA批准新的临床适应症。其实对于包括ALK在内的少见突变,确实很难开展前瞻性随机对照研究。而在晚期临床研究中,我们也可以看到ALK-TKI足够大的疗效改善,因此我认为,或许单臂研究的结果已经足够推动临床实践的变革。
目前,开展中的临床研究不止局限于Ⅲ期患者,同样包括Ⅰ期、Ⅱ期患者,但ALK+NSCLC患者较少在确诊时处于Ⅱ期,多数患者通常通过早筛在Ⅰa期发现,或发现时已经处于局晚期或晚期,因此我们的临床探索也主要集中在Ⅲ期围术期治疗。而对于晚期患者来说,通常治疗模式是接受ALK-TKI治疗直到疾病进展或不可耐受的毒性,但对于围术期治疗,我们还需要探索如何识别需要继续治疗的患者与不需要继续治疗的患者。对于ALK+NSCLC的围术期应用,依然存在很多未知的谜团,我希望未来看到更多关于ALK+NSCLC的深入临床研究解答这些疑问。
图3. 广东省人民医院 钟文昭教授 张潮博士
在103rd AATS年会会场
查看更多