查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





研究名称:Disitamab Vedotin plus Toripalimab in HER2-Expression Advanced Urothelial Cancer(DV联合特瑞普利单抗治疗HER2表达晚期尿路上皮癌)
发表期刊:《新英格兰医学杂志》(NEJM,影响因子:78.5)
第一作者:北京大学肿瘤医院盛锡楠教授、湖南省肿瘤医院曾恭谦教授、北京大学第一医院张崔健教授
通讯作者:北京大学肿瘤医院盛锡楠教授、郭军教授,中国医学科学院肿瘤医院周爱萍教授
主要作者单位:北京大学肿瘤医院
该研究是全球范围内尿路上皮癌抗HER2治疗领域首个开展的确证性随机对照3期临床研究,其结果将改变临床实践,并使得我国在尿路上皮癌抗HER2治疗领域取得世界领先,具有里程碑式意义。
研究背景:
HER2(人表皮生长因子受体2)是一种酪氨酸激酶受体,参与细胞增殖和存活信号的调控,其扩增或过表达可能导致肿瘤细胞侵袭性增强。尿路上皮癌是仅次于乳腺癌与胃癌的HER2高表达瘤种,一直以来HER2被认为是尿路上皮癌潜在的治疗靶点,但既往开展的一系列靶向HER2的疗法均未在尿路上皮癌领域取得突破。
郭军/盛锡楠教授团队前期采用针对HER2的抗体偶联药物维迪西妥单抗,在既往化疗以及免疫治疗失败的晚期尿路上皮癌开展了维迪西妥单抗单药的Ⅰ/Ⅱ期临床试验,展现出令人鼓舞的疗效,研究结果发表在国际肿瘤学权威杂志《临床癌症杂志》(Clinical Cancer Research)与《临床肿瘤学杂志》(Journal of Clinical Oncology)(Sheng X. et al.Clin Cancer Res 2020,Sheng X. et al.J Clin Oncol 2024.),并推动全球第一个针对HER2阳性尿路上皮癌的疗法的国内获批上市,改变了中国晚期尿路上皮癌后线治疗的现状。
在2025年3月,国际肿瘤学知名杂志《肿瘤学年鉴》(Annals of Oncology)发布了郭军/盛锡楠教授团队采用抗HER2-ADC药物维迪西妥单抗与抗PD-1单抗特瑞普利单抗的联合疗法用于晚期尿路上皮癌的Ⅰ/Ⅱ期临床研究的突破性结果(Zhou L.et al.Ann Oncol 2025),该研究为抗HER2-ADC药物联合免疫用于晚期尿路上皮癌的深入探索提供了关键科学依据。基于上述研究结果,团队设计主导了抗HER2-ADC维迪西妥单抗联合特瑞普利单抗疗法与化疗对照用于HER2表达晚期尿路上皮癌一线治疗的随机对照3期临床研究。
研究设计:
该项临床研究是一项在中国开展的开放标签、多中心、随机对照3期试验,旨在对比维迪西妥单抗与特瑞普利单抗联合方案与一线化疗方案(吉西他滨联合铂类化疗)用于既往未接受过系统治疗的HER2表达(定义为经中心实验室免疫组化检测HER2表达为1+、2+、3+)的晚期尿路上皮癌的有效性与安全性。筛选合格的受试者根据顺铂耐受(耐受vs不耐受)、HER2表达(IHC 1+ vs 2+/3+)以及内脏转移(有 vs 无)等分层因素,以1:1的比例随机分配至维迪西妥单抗与特瑞普利单抗联合疗法组,或吉西他滨联合铂类化疗组接受相应治疗,直至疾病进展或不能耐受,主要研究终点为独立评审委员会(IRC)评价的无进展生存(PFS)期与总生存(OS)期,次要研究终点为研究者评估的无进展生存期、客观有效率以及安全性。

RC48-016研究的主要研究设计
研究结果:
截至2025年3月31日,本研究共对811例受试者进行筛选,共有484例合格受试者随机入组,分别有243例与241例接受联合治疗组或化疗组,两组受试者的基线特征相当,两组HER2(2+或3+)的比例分别为77.4%与78.0%。截至数据分析,中位随访时间为18.2个月,联合治疗组仍有37.4%受试者接受治疗,而化疗对照组为0。
主要研究终点-无进展生存期方面,基于独立影像学评估,联合治疗组较对照组可显著延长无进展生存期(13.1个月 对 6.5个月,HR 0.36,95%CI:0.28-0.46;P<0.001),生存期方面,联合治疗组较对照组可显著延长总生存期(31.5个月 对 16.9个月,HR 0.54,95%CI:0.41-0.73;P<0.001),整体临床试验结果达到本试验的主要终点。
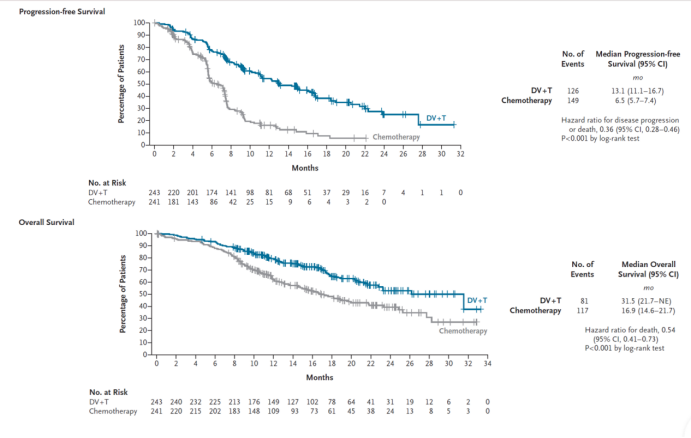
RC48-016研究主要研究终点:联合治疗组较化疗对照组的无进展生存期(Progression-Free Survival,上图)与总生存期(Overall Survival,下图)双终点达到显著差异
次要研究终点方面,独立影像评估的客观有效率两组分别为76.1%与50.2%,中位疗效持续时间两组分别为14.6与5.6个月,既定亚组分析显示:性别、年龄、一般情况、原发病灶起源部位、内脏转移、HER2表达、铂类耐受等不同亚组均能从联合治疗中获益。
安全性方面,联合治疗组与对照组所有不良反应发生率相当,但治疗相关的3级及以上不良反应发生率两组分别为55.1%与86.9%,治疗相关的严重不良反应两组发生率分别为28.4%与40.5%。
研究结论:
研究结果显示,在既往未接受系统治疗的HER2表达的晚期尿路上皮癌患者中,抗HER2-ADC药物维迪西妥单抗与PD-1单抗特瑞普利单抗联合对比标准化疗可显著改善无进展生存期与总生存期,同时具有可控的安全性。上述结果支持抗HER2-ADC药物维迪西妥单抗与PD-1单抗特瑞普利单抗联合可以用于HER2表达的晚期尿路上皮癌患者一线治疗。
1. 推动UC全人群HER2检测常规化,构建精准治疗新格局
RC48-C016研究成功达到预设的双主要终点,与传统含铂化疗相比,DV+T方案显著延长了中位PFS期和OS期,大幅提高客观缓解率,并展现出更优的安全性和耐受性。作为全球首个在HER2表达mUC一线治疗中证实DV+T方案显著优于含铂化疗的3期试验,该研究结果预计将重塑中国临床实践格局,成为HER2表达mUC患者新的标准一线治疗方案。
需要指出的是,本研究首次将精准治疗获益人群从HER2高表达(IHC 2+/3+)拓展至HER2表达(IHC 1+/2+/3+)的全谱系人群,实现了HER2靶向治疗从“高表达”向“广谱表达”时代的跨越。随着HER2检测在临床实践中的常规化与全覆盖实施,预计近80%的UC患者将有机会接受该精准治疗方案,从而显著提升总体治疗获益。同时,该研究为HER2-ADC联合免疫治疗在更早分期UC患者中的应用探索奠定了坚实基础。
2. 当前局限与未来展望
RC48-C016研究是HER2-ADC在尿路上皮癌领域首次公布数据的3期临床试验,标志着HER2靶向治疗迈入新阶段。然而,本研究仍有一定局限性:
首先,本试验的所有入组患者均为中国人群,其结果在全球不同地区及种族中的适用性尚待验证。要实现该方案在全球尿路上皮癌精准诊疗中的广泛应用,仍需通过全球多中心研究进一步评估不同人群中HER2表达特性、联合方案疗效与安全性的一致性。
其次,由于一线治疗后的免疫维持治疗(如阿维鲁单抗的相关适应证)尚未在中国获批,因此本研究对照组未纳入 “含铂化疗+免疫维持” 这一国际标准治疗模式。此差异可能对OS结果的跨国可比性产生一定影响。
展望未来,维迪西妥单抗国际3期临床试验DV001的结果备受期待。若其在全球患者中再次验证RC48-C016研究的卓越疗效与良好安全性,将进一步巩固DV+T联合方案在HER2表达mUC治疗中的核心地位。可以预见,HER2-ADC联合免疫治疗模式有望成为全球尿路上皮癌精准治疗的新支柱,为更广泛的人群带来生存获益。
主任医师,医学博士,博士生导师
北京大学肿瘤医院黑色素瘤与肉瘤内科主任,泌尿肿瘤内科主任
中国临床肿瘤学会(CSCO)副理事长兼秘书长
国际黑色素瘤协会(MWS)副主席
国家癌症中心国家肿瘤质控中心黑色素瘤专委会主任委员
CSCO黑色素瘤专家委员会前任主任委员
CSCO肾癌专家委员会副主任委员
CSCO免疫治疗专委会副主任委员
CSCO尿路上皮癌专委会副主任委员
CSCO前列腺癌专委会副主任委员
CFDA国家药品注册评审专家
国家卫生健康委合理用药专家委员会委员(抗肿瘤用药专业组)
主任医师,教授,博士生导师
北京大学肿瘤医院泌尿肿瘤内科副主任
中国抗癌协会泌尿生殖肿瘤整合康复专业委员会副主任委员
中国抗癌协会泌尿系统肿瘤专业委员会常委
中国临床肿瘤学会(CSCO)理事
中国临床肿瘤学会肾癌专家委员会常委兼秘书长
中国临床肿瘤学会尿路上皮癌专家委员会常委
中华医学会泌尿外科学分会临床研究学组副组长
国家肿瘤质控中心膀胱癌质控专家委员会委员
北京肿瘤防治研究会泌尿肿瘤分委会候任主任委员
北京医学会肿瘤分会常委
每一项临床研究都倾注着研究团队的心血结晶。学习过后,您是否有所收获?或有疑问想与主创团队分享?请在评论区留言,期待与您交流!

查看更多