查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





人工智能赋能乳腺癌个体化治疗专刊
Cancer Biology & Medicine
据统计,乳腺癌已成为全球女性发病率最高的恶性肿瘤,每年新发病例超过230万。面对这一沉重的疾病负担,乳腺癌诊疗领域正以前所未有的速度演进——精准医学不断深入临床实践,人工智能逐步赋能诊疗决策,国内外学者的研究步伐也在持续加快。在这一背景下,Cancer Biology & Medicine与中国人民解放军总医院江泽飞教授联合打造“人工智能赋能乳腺癌个体化治疗”专刊,旨在汇聚顶尖专家的智慧,系统呈现乳腺癌诊疗领域的新进展、新思考和新突破。
三阴性乳腺癌(TNBC)具有高度异质性,其中腔面雄激素受体型(LAR)约占10%–20%,表现为低增殖与高转移潜能,并对化疗和免疫治疗反应有限,是临床上亟待突破的“难治亚型”。尽管既往研究尝试以雄激素受体为靶点,但疗效有限,提示仍存在关键驱动机制尚未被识别。本期专刊中,复旦大学肿瘤医院团队基于该中心TNBC多组学队列,系统整合基因组、转录组及功能实验,发现LAR亚型存在两类具有明确转化潜力的治疗靶点:一是ERBB2激酶区突变驱动的信号激活,二是细胞衰老相关的免疫抑制微环境。研究者进一步通过类器官和动物模型验证,提出针对该亚型的精准治疗新策略。

Cite

Zhao Y, Wang H, Wang Y, Jiang Y, Hu X, Shao Z.Integrative multi-omic analysis identified ERBB2 mutations and senescencedriven immune suppression as dual therapeutic targets in LAR triple-negativebreast cancer. Cancer Biol Med. 2026; 23: 374-391. doi: 10.20892/j.issn.2095-3941.2025.0691
内容介绍
三阴性乳腺癌长期以来被当作一种“同质化”疾病治疗,但事实上它包含多个分子亚型。其中LAR亚型尤为特殊:患者多为绝经后女性,肿瘤Ki-67指数很低,呈现“惰性”表型,但淋巴结转移率却高达54%,且对标准新辅助化疗和免疫检查点抑制剂响应甚微。这种“表里不一”的特性提示,LAR亚型背后隐藏着独特的驱动机制。
本研究依托复旦大学附属肿瘤医院FUSCC-TNBC队列(81例LAR vs. 279例非LAR),通过全外显子测序、转录组测序及系统的功能实验,最终锁定两大治疗靶点。
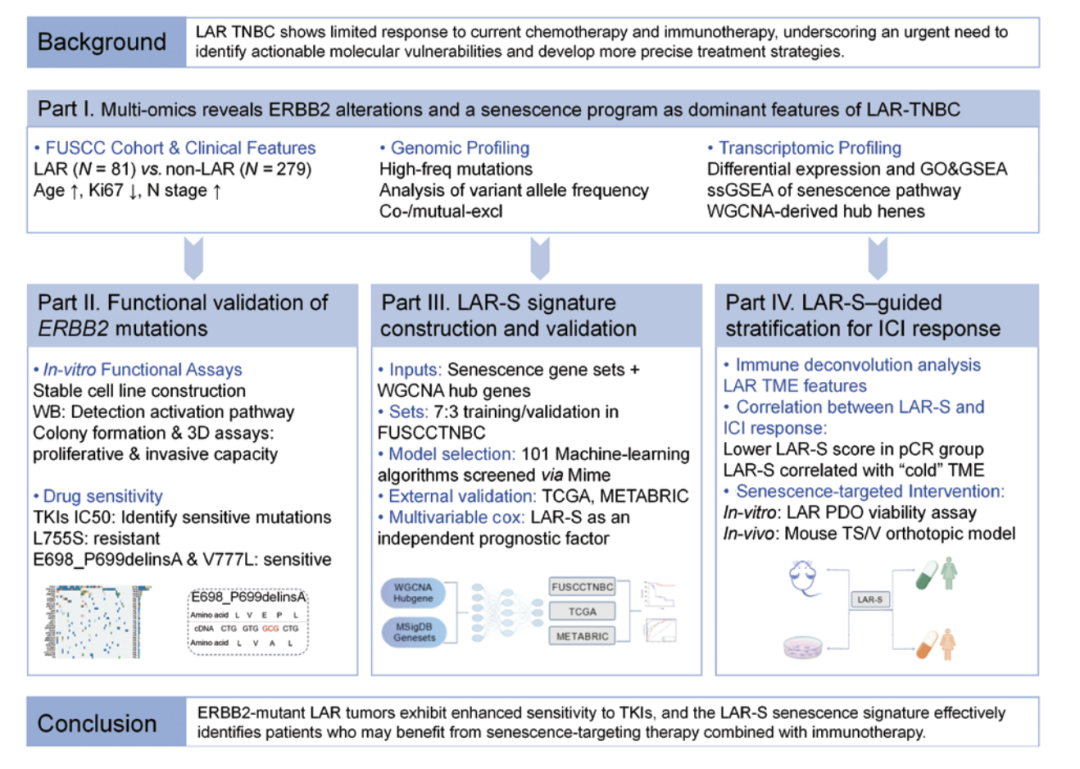
研究流程图
1. LAR亚型中ERBB2突变富集,提示新的精准治疗入口
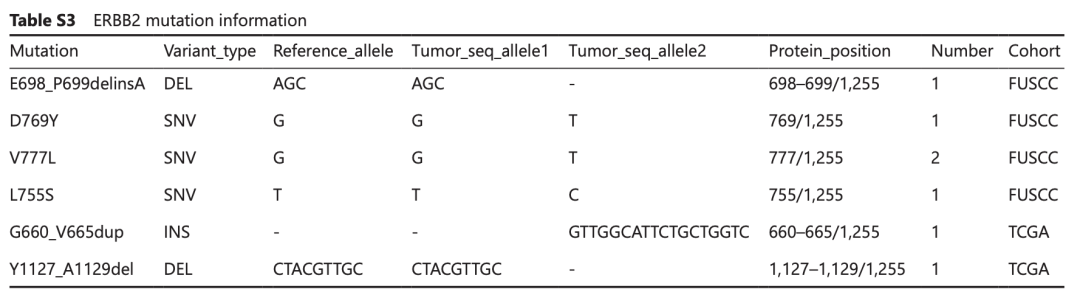
多组学分析显示,LAR亚型中PIK3CA、PTEN及ERBB2突变显著富集,其中ERBB2突变几乎特异性出现在LAR亚型中(约9%),而在非LAR亚型中基本缺失。与经典HER2扩增型乳腺癌不同,这类突变多位于激酶结构域,属于非扩增型驱动事件。
进一步功能实验表明,这些ERBB2突变并非“旁观者”,这些激活突变在LAR型肿瘤的恶性进展中发挥了关键的驱动作用,通过激活HER2-PI3K-AKT及MAPK等信号通路,促进细胞增殖和克隆形成能力。同时,不同突变位点对靶向药物呈现差异化敏感性。例如,V777L及E698_P699delinsA突变对奈拉替尼高度敏感,而L755S则表现为对拉帕替尼耐药。
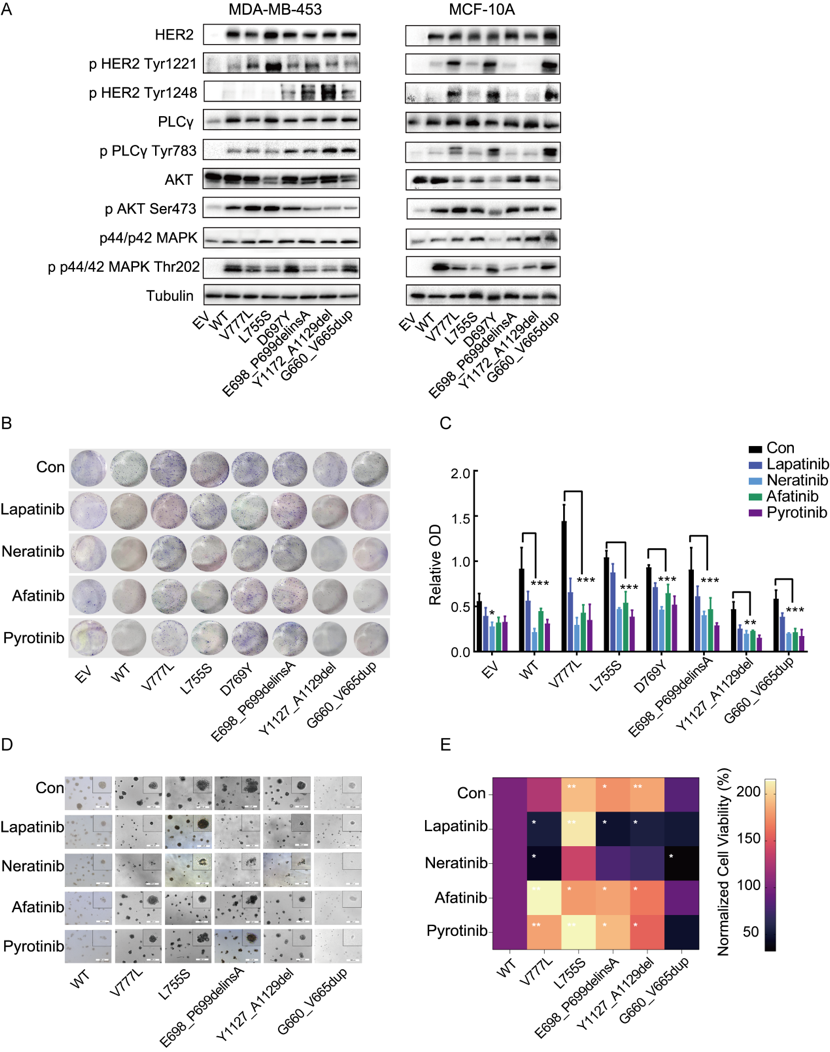
LAR相关ERBB2突变的功能验证及靶向治疗
(A)Western blot分析稳定表达空载体(EV)、野生型(WT)或ERBB2突变的MDA-MB-453和MCF-10A细胞系中HER2-PI3K-AKT通路的激活情况。
(B)表达EV、WT ERBB2或ERBB2突变的MDA-MB-453细胞集落形成实验的代表性图像,评估其致癌转化潜能。
(C)定量分析集落形成数的柱状图。数据来自三次独立实验,以均值±SD表示。
(D)携带不同ERBB2构建体的MCF-10A细胞在三维(3D)球体培养中的代表性图像,细胞经溶媒(DMSO)或一组HER2酪氨酸激酶抑制剂(TKI)(拉帕替尼、奈拉替尼、阿法替尼、吡咯替尼)处理。
(E)TKI处理下3D球体培养的相对细胞活力热图。EV:空载体;WT:野生型;TKI:酪氨酸激酶抑制剂。
这一结果具有重要的临床意义:在传统定义为HER2阴性的TNBC中,通过检测ERBB2突变,可识别一部分潜在受益于HER2-TKI靶向治疗的患者,补充了传统病理分型的局限,为精准治疗提供新的入口。
2. LAR亚型中衰老相关免疫抑制是免疫治疗低效的关键原因
除基因突变外,研究团队进一步揭示LAR亚型具有显著的细胞衰老特征。转录组分析显示,该亚型显著富集细胞衰老相关通路,并伴随多种SASP因子(如IL-6、IL-8等)上调,GSEA和ssGSEA均显示,LAR型肿瘤的固有的雄激素受体响应和脂质代谢活跃,其细胞衰老等通路活性显著高于非LAR型。
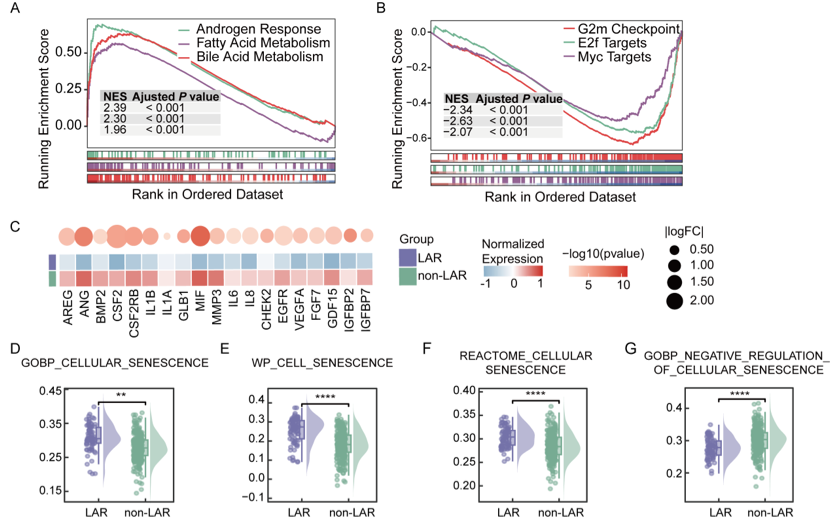
转录组分析揭示LAR亚型具有独特的细胞衰老特征
(A、B)LAR亚型与非LAR亚型相比,代表性标志性通路的GSEA富集图:(A)上调通路;(B)下调通路。显著通路的判定基于FDR q< 0.25。
(C)SASP基因的表达分析。左图:热图展示SASP基因在LAR和非LAR样本中的归一化表达水平;右图:气泡图展示每个SASP基因的log2FC。差异表达基因(DEG)的定义标准为 |log2FC| > 1 且 FDR校正后P < 0.05。
(D–G)箱线图比较LAR与非LAR亚型之间衰老相关基因集的ssGSEA富集分数:(D)GO BP:细胞衰老;(E)WikiPathways:细胞衰老;(F)Reactome:细胞衰老;(G)GO BP:细胞衰老的负向调控(均来自MSigDB)。
进一步免疫浸润分析显示,LAR亚型呈现典型“免疫冷”表型:CD8+ T细胞、NK细胞等效应细胞显著减少。在I-SPY2免疫治疗队列中,衰老特征较高的患者病理完全缓解(pCR)率更低,提示衰老驱动的免疫抑制是免疫治疗耐药的重要机制。进一步分析发现,衰老相关基因特征与T细胞活化、IFN-γ信号等免疫通路呈负相关。
基于上述机制,研究进一步提出一个关键假设:如果解除衰老状态,是否可以恢复免疫治疗敏感性?在患者源性类器官(PDO)模型中,使用衰老调节剂逆转衰老状态,可显著抑制LAR肿瘤生长;在小鼠模型中,单独使用抗PD-1或衰老调节药物效果有限,但联合治疗可显著抑制肿瘤生长,效果明显优于单药。从机制上看,这一策略可降低SASP相关炎症信号,减少免疫抑制细胞,并恢复CD8+ T细胞浸润,从而将“免疫冷肿瘤”转化为“免疫热肿瘤”。
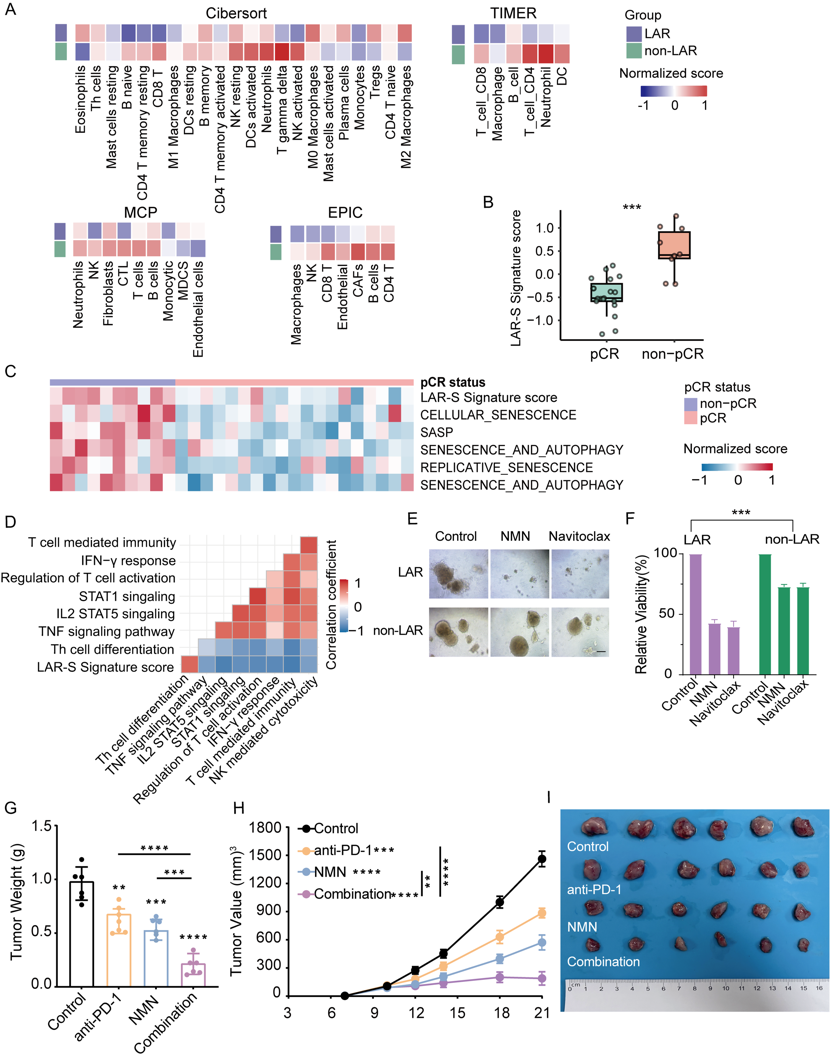
LAR-S特征与免疫抑制表型相关,并提示对抗PD-1疗法的敏感性
(A)基于CIBERSORT、EPIC、MCP和TIMER算法,比较FUSCC-TNBC队列中LAR与非LAR亚型之间肿瘤微环境中免疫细胞浸润的相对丰度。
(B)I-SPY 2队列中, pCR组与非pCR组患者LAR-S评分比较。
(C)I-SPY 2队列中,按pCR与非pCR分层的衰老相关特征ssGSEA评分。
(D)pCR患者组中LAR-S评分与免疫通路特征之间的相关系数。
(E)药物处理后第7天PDO的代表性图像。
(F)LAR型PDO经衰老抑制剂治疗后的治疗反应,以相对细胞活力表示。
(G)LAR移植瘤的终点瘤重,治疗包括溶媒对照、NMN、PD-1抗体或联合治疗。
(H)小鼠LAR移植瘤的肿瘤生长曲线。
(I)小鼠LAR移植瘤的代表性肿瘤图像。
对于无ERBB2突变的LAR患者,NMN(已作为膳食补充剂在人体中开展研究)联合免疫检查点抑制剂,提供了一种“老药新用”+“免疫增敏”的可行方案,为该类患者提供了新型精准治疗策略。
小结
本研究通过多组学整合和系统功能验证,本研究立足于临床难治性LAR型三阴性乳腺癌,通过多组学分析与体内外实验,明确了该亚型在基因组突变和免疫微环境层面的两大核心特征,并在此基础上识别出两大治疗突破口:
ERBB2突变亚群:约9%的LAR患者携带可靶向的激酶域突变,对奈拉替尼等TKI敏感,ERBB2突变为部分患者提供了可直接应用的精准靶向治疗路径,提示在HER2阴性人群中开展突变筛查具有现实意义。
衰老驱动的免疫抑制亚群:研究首次将“细胞衰老”作为LAR亚型的核心生物学特征,揭示其通过SASP介导免疫抑制,从而导致免疫治疗低效。联合使用衰老调节剂NMN与PD-1抗体,可在临床前模型中显著逆转免疫抑制、协同抑制肿瘤生长。
整体而言,该研究丰富了三阴性乳腺癌精准分型与治疗的理论基础,从机制到干预策略建立了完整的转化链条,为LAR型TNBC这一难治亚型提供了新的治疗方向,这一“双靶点、双策略”的精准分层治疗思路,有望改善LAR型TNBC患者的长期生存,并为其他衰老相关实体瘤的治疗提供借鉴。
通信作者
邵志敏 教授
复旦大学附属肿瘤医院
主任医师 医学博士 博士生导师
复旦大学附属肿瘤医院 肿瘤研究所所长
复旦大学肿瘤医院 乳腺癌研究所所长
亚洲乳腺癌协会主席
中国抗癌协会乳腺癌专业委员会主任委员
中国抗癌协会乳腺癌专业委员会主任委员
中华医学会肿瘤分会常委
上海市乳腺疾病防治委员会副主任委员
上海抗癌协会乳腺癌专业委员会主任委员
胡欣 教授
复旦大学附属肿瘤医院
研究员 医学博士 博士生导师
复旦大学附属肿瘤医院 精准肿瘤中心执行副主任
复旦大学附属肿瘤医院 肿瘤研究所所长助理
上海市抗癌协会遗传性消化道肿瘤专业委员会副主委
中国抗癌协会肿瘤精准治疗专委会委员
上海市抗癌协会乳腺癌专业委员会委员
上海市医学会肿瘤靶分子专科分会委员
上海市抗癌协会检验医学专业委员会委员
来源:Cancer Biology Medicine
查看更多