查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





11月9~13日,一年一度的美国肝病研究学会(AASLD)年会在美国旧金山如期召开,来自世界各地的肝脏病学领域学者们对新技术和新进展进行了深入交流与探讨。会上公布了一系列最新临床试验(late-breaking clinical trials),其中由美国学者发布的一项关于HCV感染患者抗病毒治疗新方案的研究,已发广泛热议,本文特邀四川大学华西医院感染疾病中心唐红教授对该研究进行点评。

目前,丙型肝炎病毒(HCV)感染患者的抗病毒治疗已经进入直接抗病毒药物(DAA)时代,相较于以前的聚乙二醇干扰素联合利巴韦林(PR)方案,DAA方案具有安全性更好、持续病毒学应答(SVR)率更高、疗效不受宿主白介素-28(IL-28)单核苷酸多态性(SNP)影响等诸多优势,但也存在一些不足,包括治疗费用较高、部分地区药物可及性受限、与其他药物出现药物间相互作用(DDI)、存在治疗失败可能性等问题。尤其出现治疗失败后,无论是治疗前预存或是由治疗诱导产生的耐药相关置换(RAS)都使得患者再治疗成为新的挑战。
NS5A抑制剂+索磷布韦(SOF)±利巴韦林(RBV)的方案是 DAA初治患者的常见用药方案,该方案靶 向HCV NAS5A和NS5B两个靶点,能强效抗病毒,部分患者甚至加用RBV以期缩短疗程或者增加疗效。对于该方案治疗失败的HCV感染患者,可供选择的再治疗方案有限。每日一次固定剂量的HCV NS3/4A蛋白酶抑制剂格卡瑞韦(glecaprevir,300 mg)和NS5A抑制剂派仑他韦(pibrentasvir,120 mg)(G/P)联合治疗,被美国食品与药物管理局(FDA)批准用于之前应用包含NS5A抑制剂的方案治疗失败、未用过NS3/4A蛋白酶抑制剂治疗的基因1型(GT1)HCV感染患者的再治疗。
本届AASLD年会上,美国学者交流的一项研究表明,NS5A抑制剂+SOF±RBC治疗失败的HCV GT1感染患者应用G/P方案治疗16周,耐受性良好,可以获得较高的SVR率。
该项研究纳入 NS5A抑制剂+SOF±RBV经治的HCV GT1患者,根据 GT1的基因亚型(1b或非1b亚型)进行分层,随机分组和给药如下:将无肝硬化(NC)患者按照2:1比例,分为A、B两组,分别应用G/P方案治疗12周(NC-12)和16周(NC-16);将代偿期肝硬化(CC)患者按1:1比例,分为C组和D组,分别应用G/P+RBV方案治疗12周(CC-12+R)和 G/P方案治疗16周(CC-16)。研究对所有基线和研究过程中发生病毒学失败的标本进行深度测序,检测NS3和NS5A耐药,主要研究终点为治疗结束后12周时的持续病毒学应答(SVR12)。177例接收治疗的受试者中,多数(81%)受试者为男性,80%为GT1a HCV感染,44%为黑人。目前,147例(83%)患者已经达到治疗结束后4周,132例(75%)患者达到治疗结束后12周。
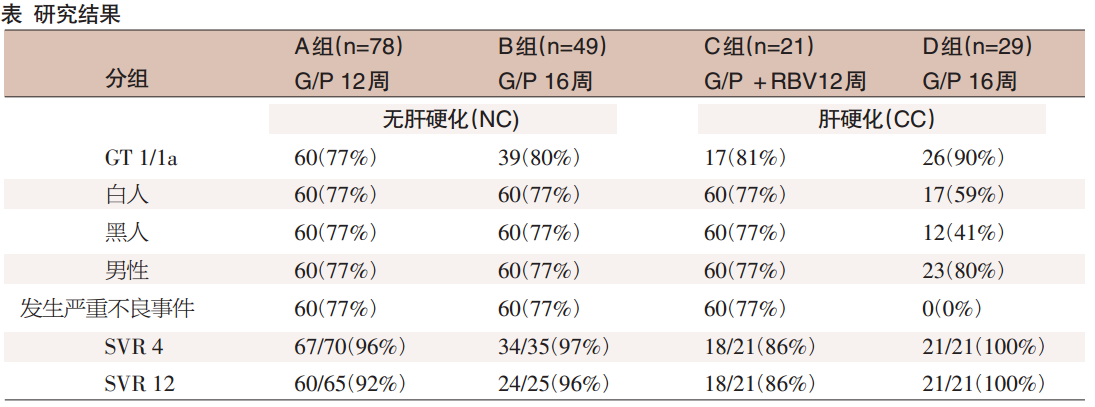
对有治疗结束后12周数据的132例患者分析结果显示,NC-12、NC-16、CC-12+R和CC-16组的SVR12率分别为92%、96%、86%和100%(表)。共有9例受试者治疗失败,包括NC-12组5例(4例复发,1例突破)、NC-16组1例(复发)和CC-12+R组3例(均为病毒学突破,并导致停药)。无患者由于不良事件停药,报告最常见的不良事件为疲乏(25%)、头痛(22%)和恶心(10%)。8例患者发生严重不良事件,其中1例发生肝细胞癌导致死亡,但均与治疗无关。
这项依然在进行中的研究目前获得了较为满意的研究结果。最终的有效性和安全性数据将在终期研究结果中披露。该项研究为NS5A抑制剂+SOF±RBV治疗失败的HCV感染患者提供了一个安全有效的再治疗方案。
在研究所纳入的这一特殊人群中,该方案有效的原因可能为:患者未用过NS3/4A蛋白酶抑制剂,不存在由药物诱导产生的RAS,而glecaprevir为第二代蛋白酶抑制剂,具有高耐药屏障和抗病毒活性。同时,方案中另一药物pibrentasvir也为第二代NS5A抑制剂,相较于第一代,该药耐药屏障更高,并有极强的抗病毒活性。因此,两药的联合能使再治疗呈现较为满意的疗效。除G/P方案外,SOF/维帕他韦(VEL)/伏西瑞韦(VOX)也可作为再治疗的选择之一。
本研究也存在一些不足,例如,这些仅仅是中期研究的结果,该研究设计中缺乏其他再治疗方案的对照,蛋白酶抑制剂的加入也使得该方案无法适用于肝硬化失代偿病人的再治疗。
来源中国医学论坛报社,转载请联系授权!
查看更多