查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





当地时间9月27日,2019欧洲肿瘤内科学会(ESMO)年会在西班牙巴塞罗那拉开帷幕。今年大会的主题为“将科学研究转化为对癌症患者更好的治疗(translating science into better cancer patient care)”,强调肿瘤领域研究的核心价值在于其转化为治疗手段的潜力。本报特邀中山大学肿瘤防治中心陈功教授,解读本届ESMO年会结直肠癌领域新进展。

陈功教授
2019年9月29日,ESMO年会进入第三天,本届年会结直肠癌领域的第二重要的内容-壁报讨论在下午结束,组委会从一共近1200篇投稿摘要中筛选了10篇最重要的进行了讨论点评,一共分三部分,大部分摘要都体现了精准医学在临床实践中的应用,给人印象最深的当属第一部分的三个有关HER2扩增的研究,让人隐约能预见mCRC治疗的下一个精准医学时代可能将会是“HER时代”,不管怎样,本次ESMO年会,我已经开始嗅到“她”的味道。
2019ESMO年会结直肠癌领域壁报讨论专场(Poster Discussion)议程
- 时间:2019-09-29,15:00-16:15
- 地点:Cordoba Auditorium (Hall 7)
- 内容:
第一部分:LBA35, LAB36, 526PD, 527PD
a) LBA35 – HERACLES-8研究:帕妥珠单抗联合T-DM1治疗HER2阳性mCRC的II期研究(Phase II study of pertuzumab and trastuzumab-emtansine (T-DM1) in patients with HER2-positive metastatic colorectal cancer: The HERACLES-B (HER2 Amplification for Colo-rectaL cancer Enhanced Stratification, cohort B) trial)
b) LBA36 – CAPTEM研究最终结果:卡培他滨联合替莫唑胺(CAPTEM)对比FOLFIRI治疗RAS突变、MGMT甲基化mCRC的II期研究(Randomized phase II study of CAPTEM versus FOLFIRI in RAS mutated, MGMT methylated metastatic colorectal cancer (mCRC): Final analysis, tumour biomarkers and methylated ctDNA)
c) 526PD – TRIUMPH研究:曲妥珠单抗联合帕妥珠单抗治疗肿瘤组织或ctDNA中HER2扩增mCRC的II期试验:GOZILA子研究(Primary efficacy of a phase II trial of trastuzumab (T) and pertuzumab (P) in patients (pts) with metastatic colorectal cancer (mCRC) with HER2 (ERBB2) amplification (amp) in tumour tissue or circulating tumour DNA (ctDNA): A GOZILA sub-study)
d) 527PD – MOUNTAINEER研究初步结果:曲妥珠单抗联合tucatinib(突卡替尼,即ONT-380,一种HER2高选择性口服小分子激酶抑制剂)治疗HER2扩增mCRC的试验(Trastuzumab and tucatinib for the treatment of HER2 amplified metastatic colorectal cancer (mCRC): Initial results from the MOUNTAINEER trial)
第二部分:528PD, 529PD, 530PD, 531PD
a) 528PD - CCTG CO.26研究更新:克隆性和DNA修复突变对MSS型mCRC患者血浆肿瘤突变负荷(pTMB)及免疫治疗疗效的影响(Impact of clonality and DNA repair mutations on plasma tumour mutation burden (pTMB) and immunotherapy efficacy in microsatellite stable (MSS) metastatic colorectal cancer (mCRC) in CCTG CO.26)
b) 529PD – 甲基化ctDNA对mCRC疗效的早期预测价值(Early identification of treatment effect by methylated circulating tumour DNA in metastatic colorectal cancer)
c) 530PD – 结直肠癌患者中移行扩增分子标签与EGFR单抗疗效的关系(Association between transit-amplifying signature and outcomes of patients treated with anti-epidermal growth factor receptor (EGFR) therapy in colorectal cancer)
d) 531PD - Sequential RAS mutation testing in cfDNA in RAS wild type (wt) metastatic colorectal cancer (mCRC) patients (pt) treated with panitumumab (P) and chemotherapy (CT) in first-line (1L): PERSEIDA study
第三部分:532PD, 533PD
a) 532PD – FOxTROT研究中的病理学分析(Pre-operative FOLFOX chemotherapy in advanced colon cancer: Pathology analysis of the FOxTROT trial)
b) 533PD – BACCI-卡培他滨联合贝伐单抗+/-阿拓珠单抗(atezolizumab)治疗难治性mCRC的随机双盲安慰剂对照多中心II期研究:一项ACCRU网络研究(BACCI: A phase II randomized, double-blind, multicenter, placebo-controlled study of capecitabine (C) bevacizumab (B) plus atezolizumab (A) or placebo (P) in refractory metastatic colorectal cancer (mCRC): An ACCRU network study)
首先,让我们先来看看HER2相关的3个研究:
研究一:LBA35 – HERACLES-B研究:帕妥珠单抗联合T-DM1治疗HER2阳性mCRC的II期研究
a) 研究背景及信息

总所周知,HER2是和EGFR相同的激酶受体信号传导通路家族成员,在乳腺癌中被成功用在晚期和辅助治疗中的靶点。随后,抗HER2的治疗也被成功应用于晚期胃癌。HER2在结直肠癌中的表达是很罕见的(总体大约3%左右),但在RAS/BRAF野生型肿瘤中的过表达率要更高(据报道为5%~14%)。没有证据表明HER2过表达具有预后价值。然而,初步的研究结果提示HER2过表达可能是EGFR靶向药物耐药的疗效预测标志物。
来自意大利的HERACLES-B研究可谓是HERACLES研究的升级版,后者入组RAS野生型、HER2扩增阳性的mCRC患者,末线治疗中联合使用曲妥珠单抗和拉帕替尼,取得了30%的ORR和70%的疾病控制率,在精准医学时代将mCRC的治疗又向前推进了一步。2019年NCCN指南也首次推荐在HER2扩增阳性的mCRC末线治疗中增加“曲妥珠单抗+拉帕替尼”的治疗方案。

升级版的HERACLES-B研究有哪些改变呢?
首先,目标人群与HERACLES基本没有改变,依然是RAS野生型、既往所有标准治疗失败(含EGFR单抗)的mCRC患者,唯一不同是B研究增加了BRAF野生的条件。
其次,HER2扩增的确认也基本差不多,IHC+++,如果是IHC++则需要FISH或SISH确认。更新的是B研究中使用了NGS来同时确认HER2扩增以及RAS状态。
第三,也是最重要的,当然是治疗方案的升级,B研究使用的是帕妥珠单抗+T-DM1,更加强烈、先进的抗HER2靶向治疗。
T-DM1(即ado-trastuzumab-emtansine,商品名KADCYLA),是曲妥珠单抗(T,赫赛汀)与化疗药物DM1(伊马替林)共轭的药物,可以说是靶向与化疗的合体。其作用机制是T先与癌细胞表面的HER2受体结合后,进入细胞内。随后在癌细胞内分解并释放化疗药DM1,进而在癌细胞内发挥杀伤作用。T-DM1的作用机理体现了其精准攻击癌细胞的特点,其中曲妥珠单抗充当制导装置,将具有细胞毒性的DM1传递到HER2阳性的癌细胞上。T-DM1已经用于HER2阳性乳腺癌的治疗。
帕妥珠单抗是第一个被称作“HER二聚化抑制剂”的单克隆抗体。通过结合HER2,阻滞了HER2与其它HER受体的杂二聚,从而减缓了肿瘤的生长。其作用机制与曲妥珠单抗不同,互为补充,通过抑制同源二聚体、异源二聚体形成,进而从源头阻断HER2下游信号传导。目前在乳腺癌批准与曲妥珠单抗联合使用,产生更高效的抗HER2效应。
b) 人群基本信息与疗效
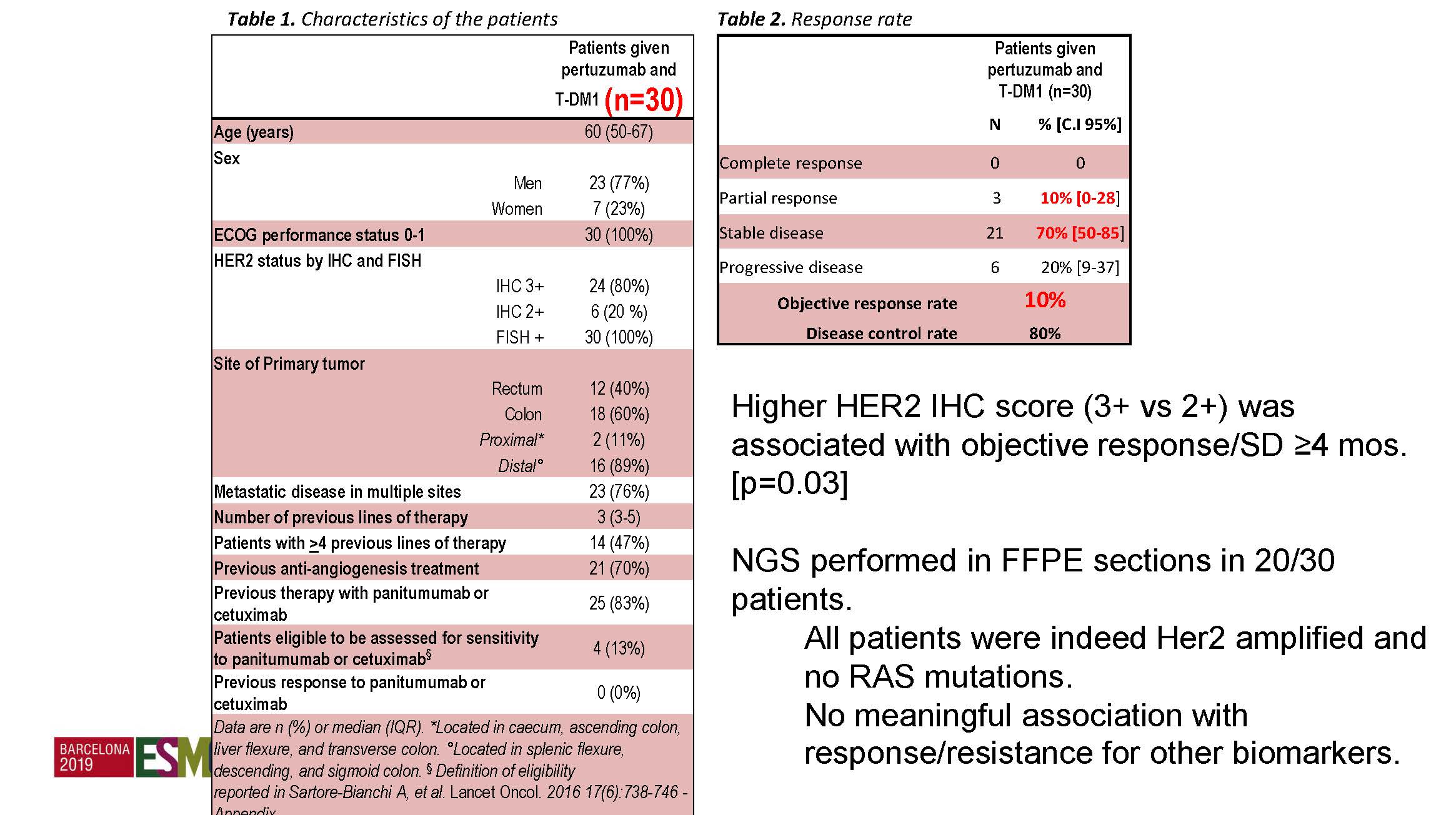
研究入组了30例难治性mCRC患者,83%的患者接受了EGFR单抗治疗,但没有ORR;70%接受了抗VEGF的治疗。经过全新抗HER2治疗后,最终全组患者的ORR为10%,但没有达到设计的主要终点(ORR 30%),4个月的疾病控制率80%。
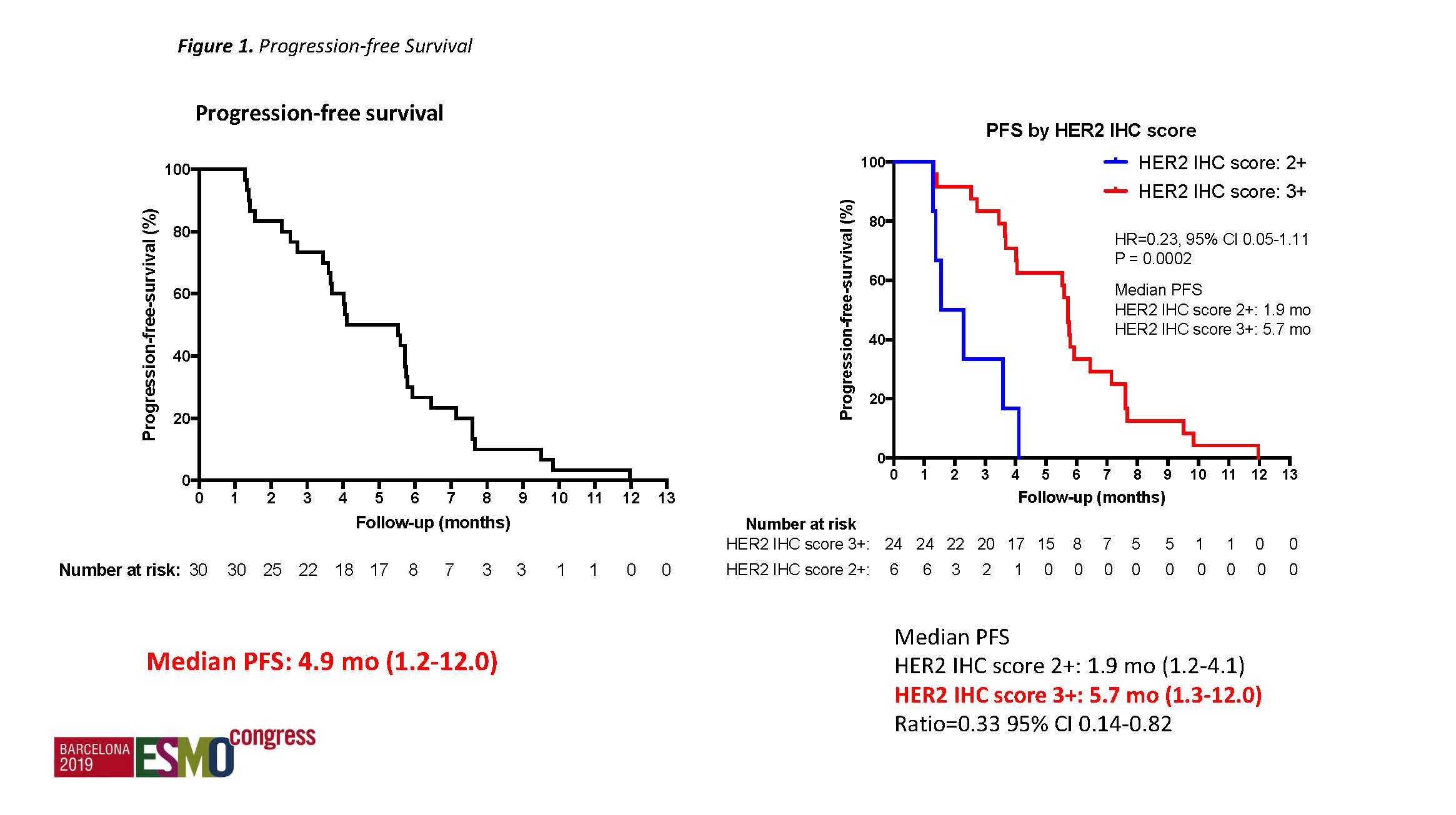
全组PFS为4.9个月,进一步的分析发现HER2 IHC高评分(3 vs 2)与更好的疗效有关,PFS 5.7对比1.9个月, HR=0.23, P=0.0002.
c) 研究解读

讨论嘉宾认为尽管研究并未达到主要研究终点,为阴性研究,但这种新型的抗HER2治疗展现了强大的治疗前景,其带来的PFS获益与之前的HERACLES研究(4.2月)和MyPathway研究(5.3月)类似,而且安全性很好。
研究二:526PD – TRIUMPH研究:曲妥珠单抗联合帕妥珠单抗治疗肿瘤组织或ctDNA中HER2扩增mCRC的II期试验:GOZILA子研究
a) 研究背景及信息

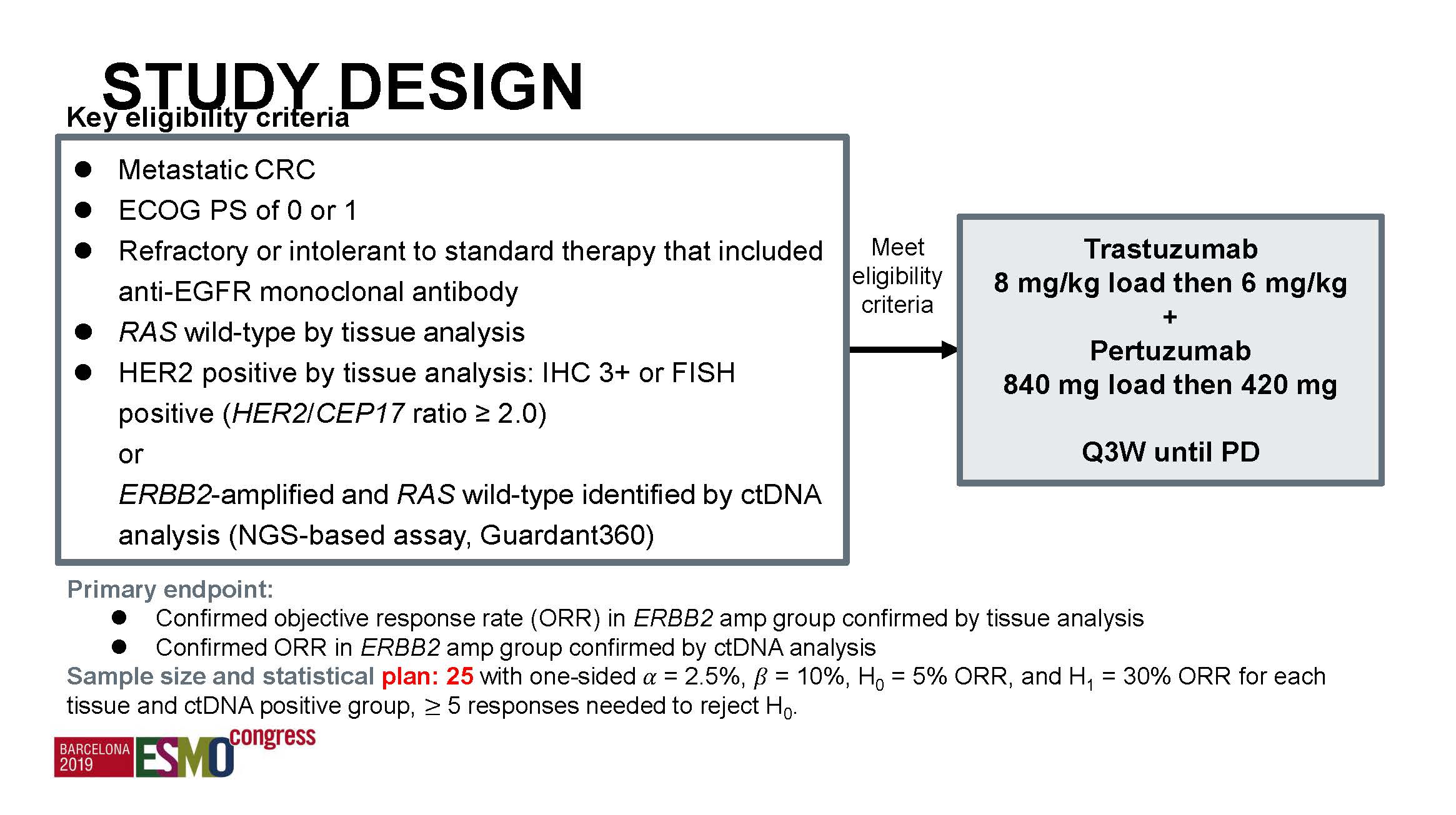
TRIUMPH研究的人群基本相同,但只入组HER2 IHC+++患者,或NGS检测HER2扩增人群,其他特征类似。治疗上与MyPathway一样,采用曲妥珠单抗联合帕妥珠单抗。主要终点ORR。
b) 疗效结果

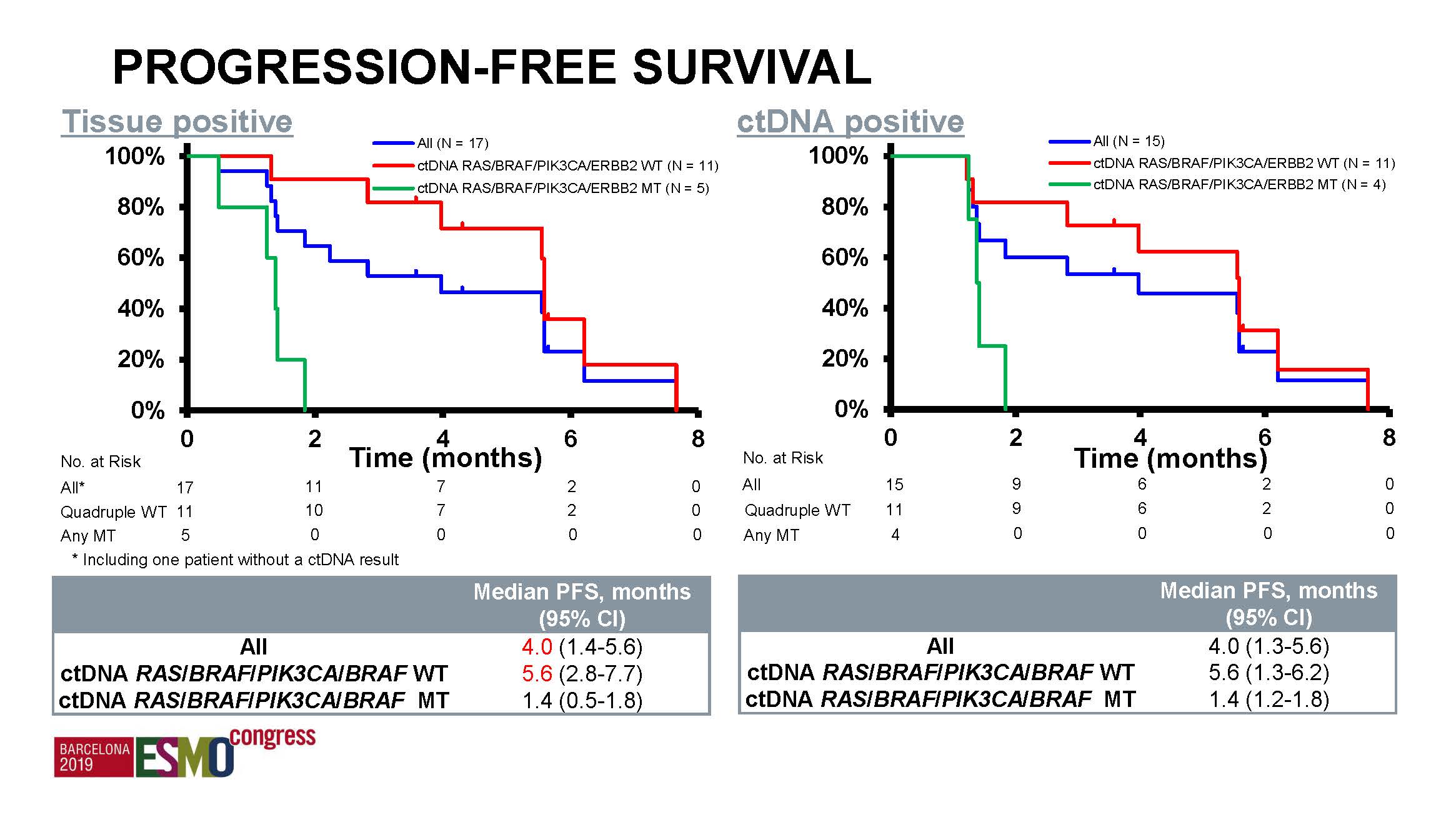
一共入组19例患者,其中18例可疗效评价;在组织HER2阳性的17例中6例获得ORR,ctDNA检测HER2扩增阳性的15例中,5例获得ORR。总体PFS为4.0月。
c) 研究解读

研究达到了主要终点,再次证实曲妥珠单抗联合帕妥珠单抗的HER2双抗治疗的抗瘤活性。结合IHC+++和ctDNA可能更好的筛选优势人群。
研究三:527PD – MOUNTAINEER研究初步结果:曲妥珠单抗联合tucatinib(突卡替尼,即ONT-380,一种HER2高选择性口服小分子激酶抑制剂)治疗HER2扩增mCRC的试验
a)研究背景及信息
a) 研究背景及信息

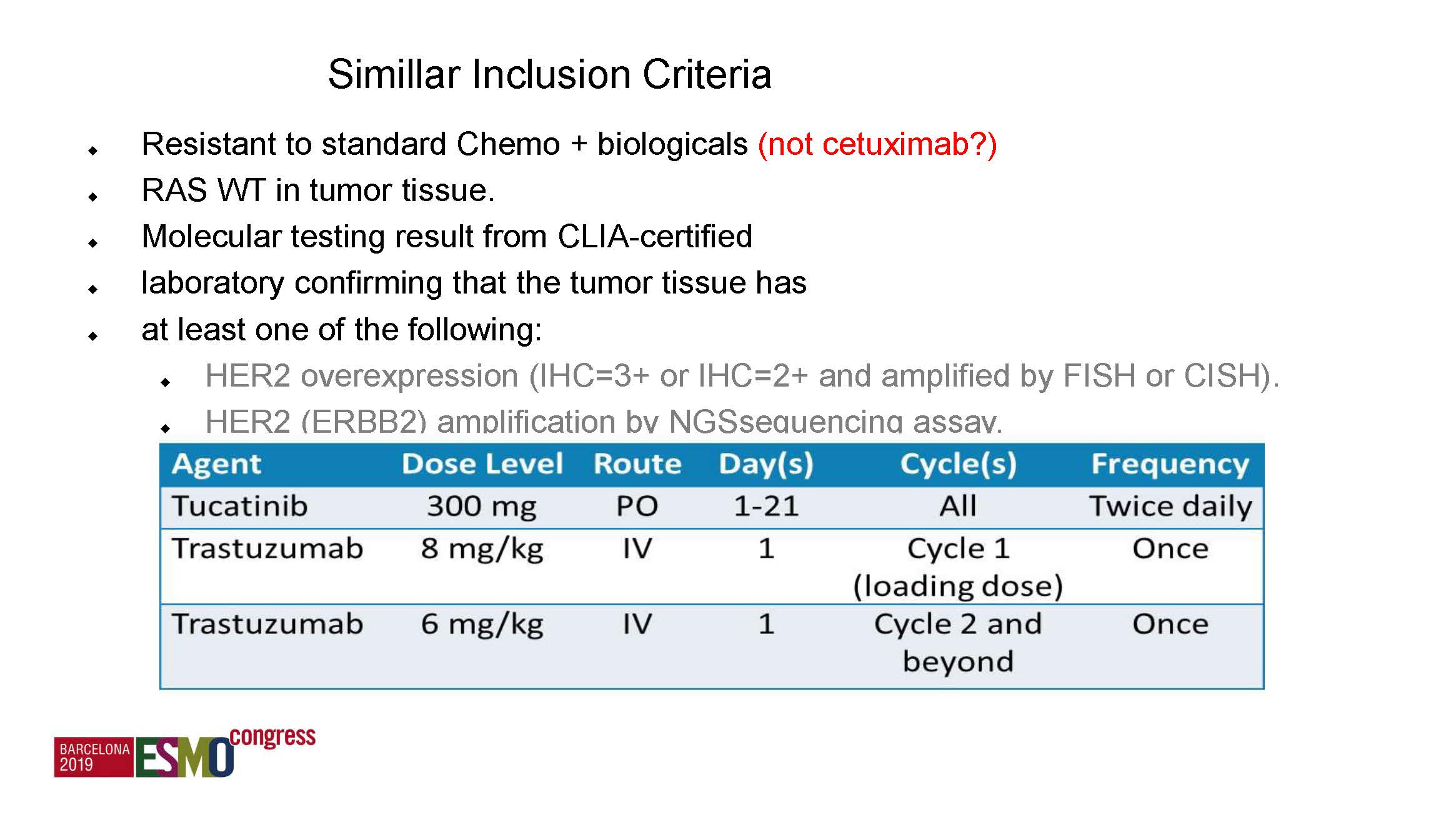
人群的入组标准和HER2判断标准均与前两个研究类似。治疗上采用曲妥珠单抗联合突卡替尼,后者是Cascadian Therapeutics公司研发的口服型小分子TKI,对HER2的抑制具有高度选择性,不会对EGFR产生作用,也就避免了EGFR抑制剂的常见毒性。
b) 疗效结果
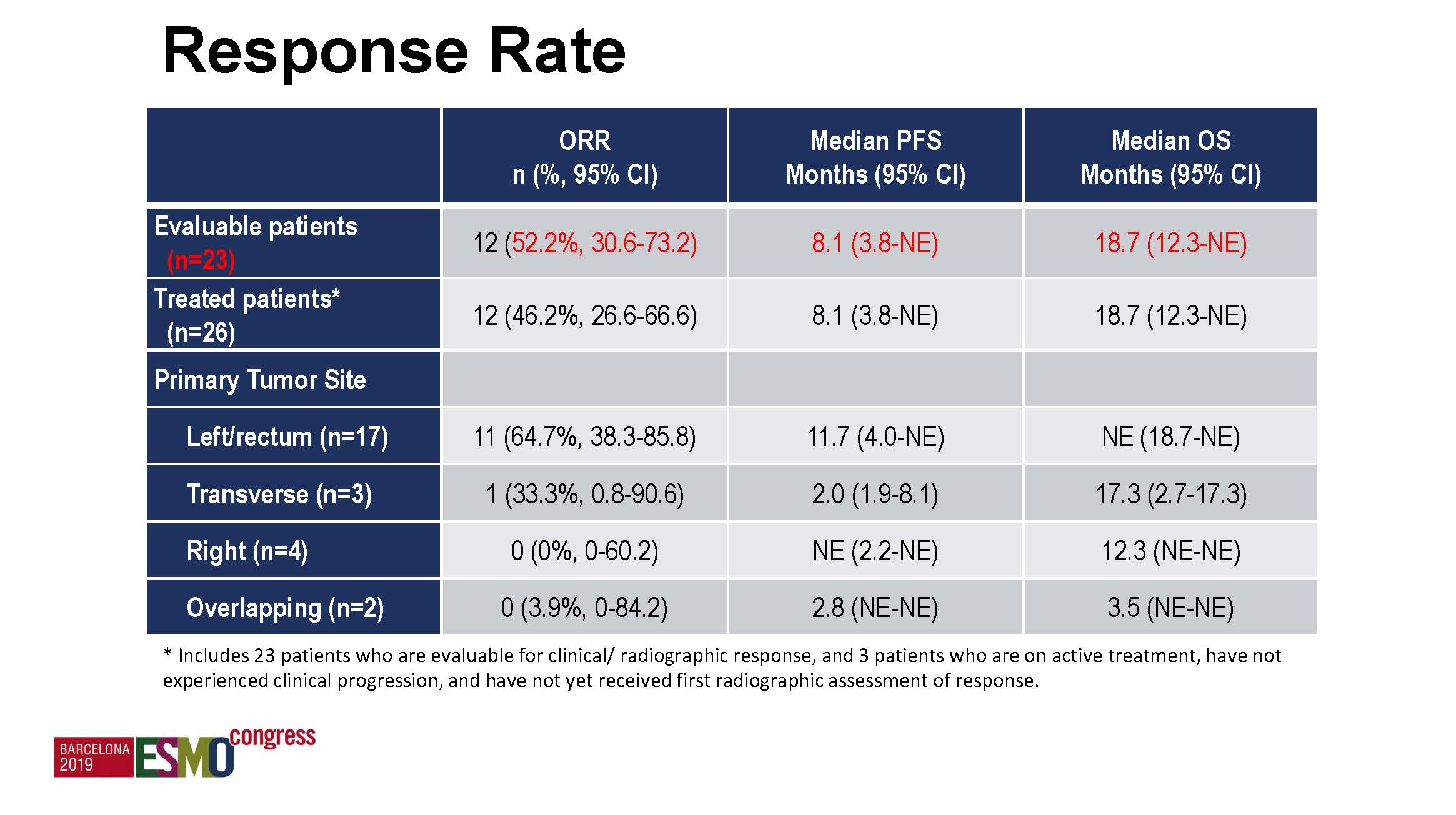
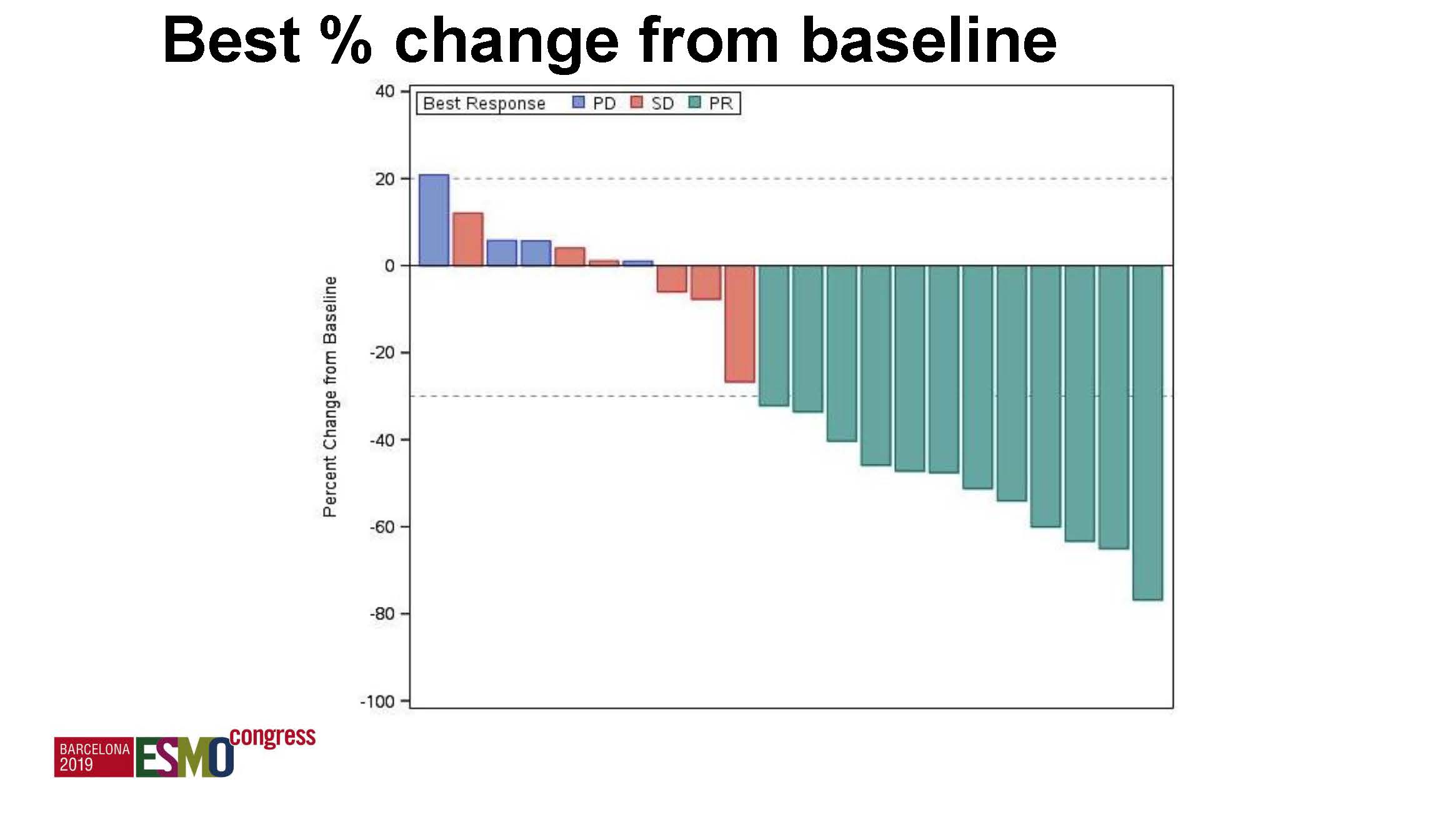
入组26例患者,23例为可评价人群,12例取得ORR(46.2%,ITT人群),中位PFS8.1月,中位OS 18.7月。
c) 安全性结果
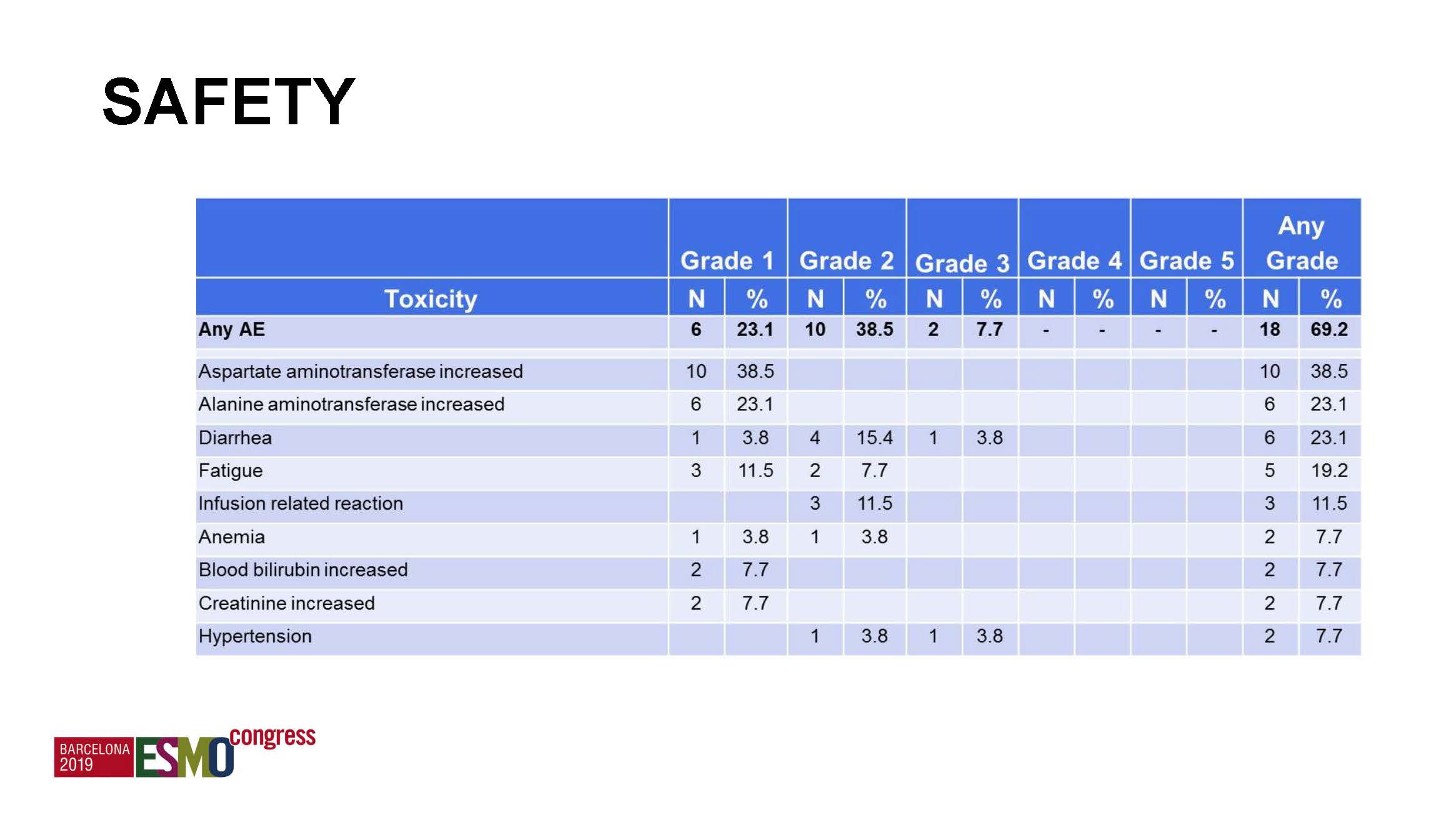
最常见的毒性是肝损害(AST/ALT升高),但主要是容易处理的I/II度。
d) 研究解读

该研究的ORR是mCRC抗HER2治疗所有研究中目前所见最高的,虽然不同试验间的比较需要很谨慎,但这么令人鼓舞的结果,提示该种新型抗HER2治疗模式具有强大的潜力。
临床启示
本次ESMO大会上集中展示的这几个mCRC末线治疗中针对HER2扩增的患者给予不同模式的抗HER2治疗,均取得了令人鼓舞的疗效,为陷入绝境中的晚期患者带来了新的希望,是精准医学推动临床实践、“异病同治”理念的典范,也改变了指南,2019 V2版NCCN指南最早做出反应,标准治疗失败的mCRC患者如果HER2扩增阳性推荐抗HER2治疗,曲妥珠单抗联合拉帕替尼或帕妥珠单抗。而这些信息也改变了我们的临床实践。
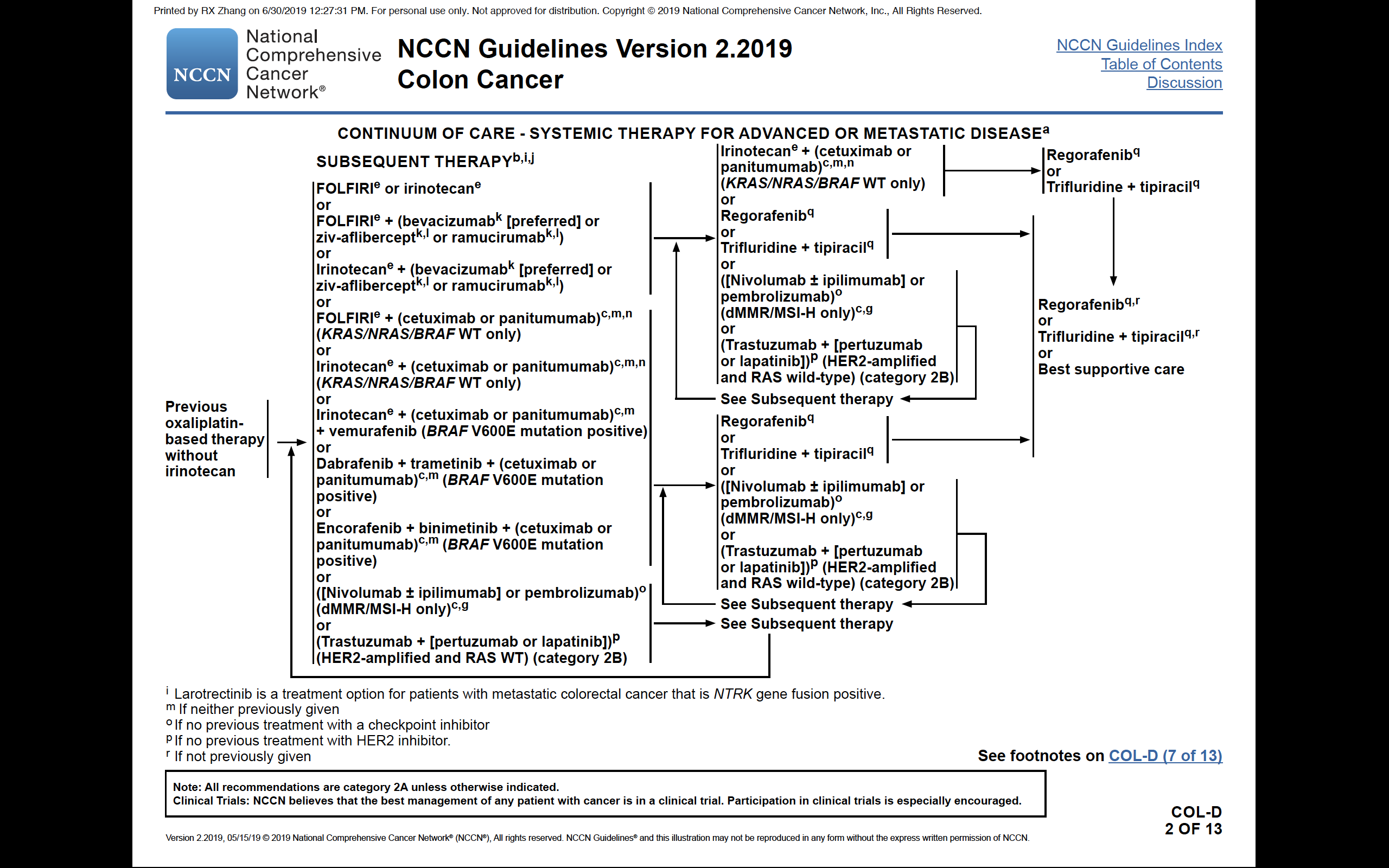
例如这个患者是我们医院治疗的一个实际病例,乙状结肠癌伴多发肝转移、盆腔种植、腹膜后淋巴结转移,RAS/BRAF野生,HER2扩增,ctDNA检测基线HER2拷贝数为4.7%,初始治疗为FOLFOX+西妥昔单抗,进展后更换为抗HER2治疗,单纯从肿瘤标志物CEA、CA199的变化即可看出,HER2拷贝数与疗效的关系。随着HER2拷贝数增加,EGFR单抗的逐渐耐药,而更换为抗HER2治疗后,患者明显获益。


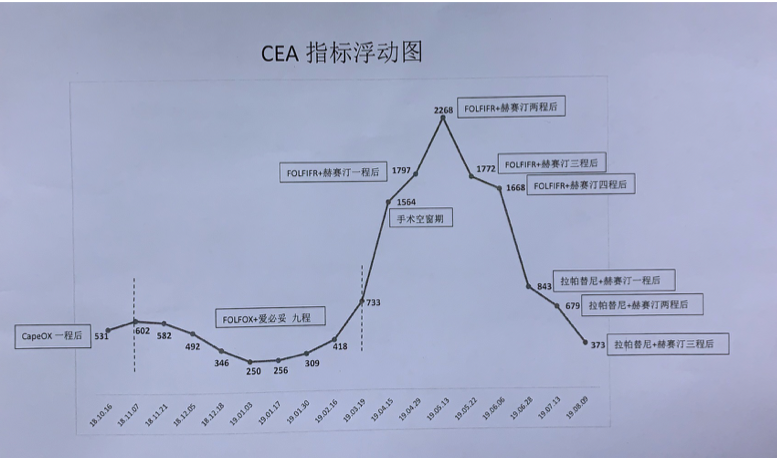
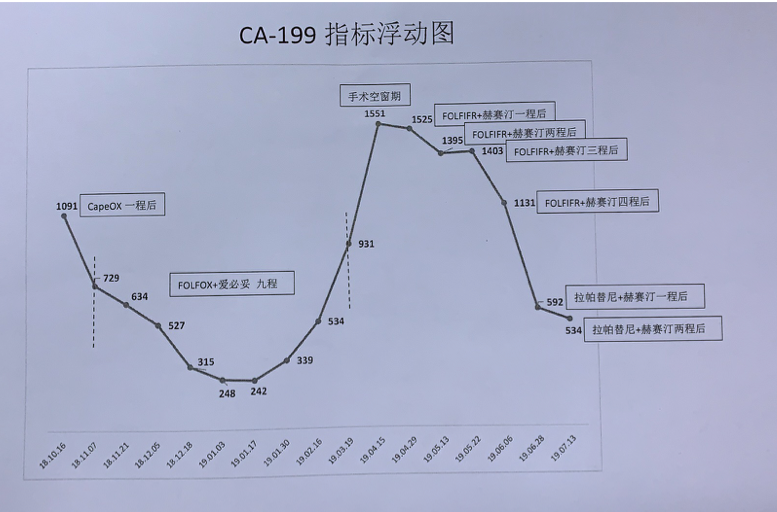
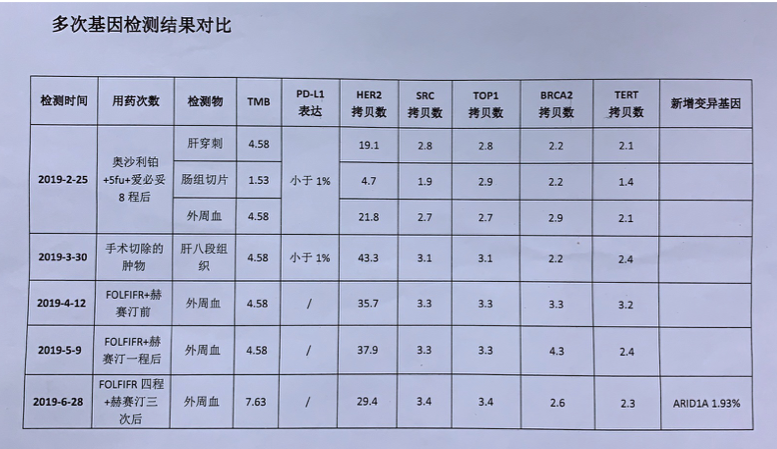
2019年的NCCN指南首次明确推荐应将EGFR单抗在一线治疗中的使用不仅限于RAS野生型左半mCRC,还增加了BRAF野生型的限制,即RAS/BRAF双野生左半,相信很快也会加入HER2扩增拷贝数的限制条件了,那些伴有HER2扩增的患者,也不太可能从单纯抗EGFR治疗中获益,但具体的HER2拷贝数截断值是多少、联合抗EGFR和抗HER2会否增加疗效,仍然是未知数。
不管怎样,基于NGS检测特殊可作用靶点突变的精准医学实践,已经在mCRC治疗领域开始开花结果,针对MSI-H人群的检查点抑制剂免疫治疗、针对BRAF突变的VIC、BEACON模式已经开启,接下来,该是抗HER2的治疗时代了。
mCRC精准医学时代,我已经嗅到了“她(HER)”的味道,你说呢?
供稿 | 陈功(中山大学肿瘤防治中心)发自西班牙巴塞罗那
编辑 | 刘婷(中国医学论坛报)
查看更多