查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





强直性脊柱炎(AS)是一种主要累及中轴关节的慢性炎症性疾病,常导致进行性、不可逆的结构损伤、功能衰退及生活质量下降1,3。其病因尚未完全明确,人类白细胞抗原B27(HLA-B27)为重要的关键易感基因,中国人群患病率为0.2%~0.5%,以男性多见4,5。目前,临床以非甾体抗炎药(NSAIDs)为一线治疗,肿瘤坏死因子α抑制剂(TNFi)既往长期作为NSAIDs应答不佳或不能耐受患者的治疗选择6,7,然而临床实践显示,约40%的AS患者对TNFi不耐受或应答不足3。国际指南推荐,白细胞介素-17A(IL-17A)抑制剂可用于治疗TNFi应答不足或不耐受的AS患者8。但在中国TNFi经治的活动性AS患者中,IL-17A抑制剂高质量Ⅲ期临床证据仍有限,尤其缺乏本土大样本随机对照研究数据8。赛立奇单抗作为国内首个全人源IgG4结构原研IL-17A抑制剂在既往接受过TNFi以及未接受过TNFi的AS患者中均显示出良好的疗效1,2,为中国此类患者提供了重要的探索性循证依据。本期我们特邀赛立奇单抗Ⅲ期研究的研究者之一,来自山东大学齐鲁医院的李洁教授对赛立奇单抗在TNFi经治人群的疗效进行深度解读与点评,以期为临床实践提供参考。
本项事后分析源于一项Ⅲ期、随机、双盲、安慰剂对照、多中心临床试验(NCT05881785)。
研究对象:
既往接受过TNFi治疗的中国活动性AS患者。
研究分组:
患者按1:1:1比例随机分配:
赛立奇单抗100 mg组;
赛立奇单抗200 mg组;
安慰剂组。
治疗16周后,安慰剂组受试者进入维持期,并按1:1比例重新随机分配至赛立奇单抗100mg组或200mg组。
主要研究终点:
第16周国际脊柱关节炎评估协会20%应答率(ASAS20)。
研究结果(图1):
在既往接受过TNFi治疗的患者中:
第16周ASAS20应答率:赛立奇单抗100mg组、200mg组分别为71.4%和83.3%,均高于安慰剂组(35.9%)(均P<0.001);
第16周ASAS40应答率:赛立奇单抗100mg组为46%(P<0.001),200 mg组为40%(P<0.01),均高于安慰剂组的18.8%;
赛立奇单抗100mg组与200mg组在疾病活动度、躯体功能、炎症水平、生活质量、健康状况及整体功能等方面的改善持续至第32周。
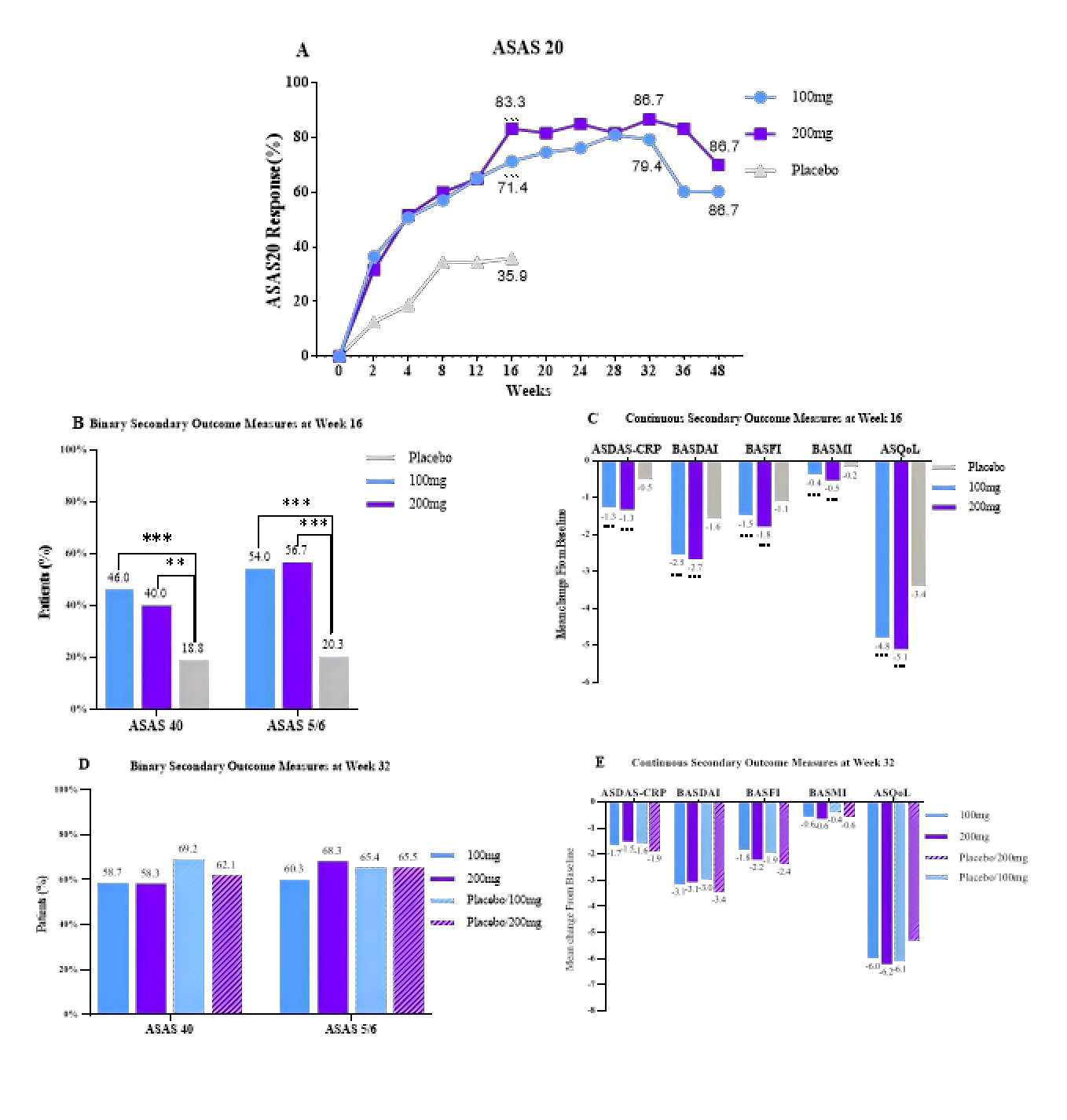
图1 主要终点ASAS20(0-48周,末次给药后28周)及次要终点短期疗效(16周)与长期疗效(32周)。
注:ASAS:国际脊柱关节炎评估协会;ASDAS-CRP:基于C反应蛋白的强直性脊柱炎疾病活动评分;BASDAI:巴斯强直性脊柱炎疾病活动指数;BASMI:巴斯强直性脊柱炎测量学指数;BASFI:巴斯强直性脊柱炎功能指数;ASQoL:强直性脊柱炎生活质量问卷。***P<0.001,**P<0.01,*P<0.05。
NCT05881785研究亚组分析结果2
未接受过TNFi以及既往接受过TNFi患者的疗效特征:
赛立奇单抗100mg组:既往接受过TNFi治疗与未接受过TNFi治疗的患者第16周ASAS20应答率相近,经治亚组在数值上更高(71.4% vs 62%,P>0.05)。
第16周,赛立奇单抗200mg组显示出类似的疗效特征,既往接受过TNFi治疗的患者ASAS20应答率数值更高(83.3% vs 68.1%,P>0.05)。同时,赛立奇单抗200mg组的应答率数值均高于100mg组。
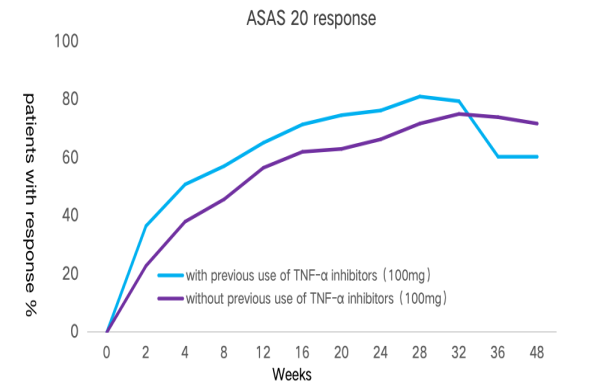
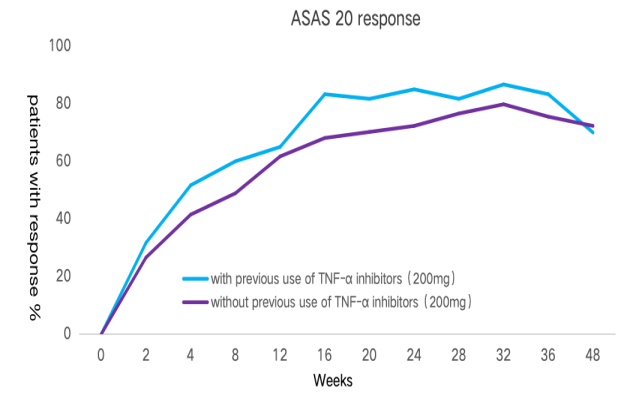
图2 赛立奇单抗100mg(左图)和赛立奇单抗200(右图)在既往TNFi经治以及未接受TNFi治疗患者0-48周ASAS20应答率。
验证IL-17A抑制剂在TNFi经治人群中的治疗价值,支持异靶点转换治疗路径
AS的炎症通路涉及多个关键细胞因子,TNFi与IL-17A在疾病的炎症驱动、骨代谢异常等过程中均发挥作用,且二者在病理环节中存在相对独立的效应环节6。基于这一机制特点,当TNFi治疗未能实现理想疾病控制时,转换至IL-17A抑制剂在机制层面具备合理性。本次事后分析结果显示,在既往接受TNFi治疗的患者中,赛立奇单抗治疗组在16周时达到主要终点及次要终点的患者比例更高,且相关疗效趋势可维持至32周,提示IL-17A抑制剂可为该类患者带来稳定的疾病控制效果。
该结果与国际同类研究的结论方向一致,验证了赛立奇单抗在TNFi应答不足或不耐受中国人群能够带来积极的疾病应答,缓解强直性脊柱炎带来的疼痛、晨僵症状,带来显著的生活质量提升。
为临床个体化用药与长期疾病管理提供可参考的本土化信息
本次事后分析纳入了赛立奇单抗100 mg与200 mg两个剂量组,结果显示两种剂量均能达成预设疗效目标,可为临床剂量选择提供参考。研究未开展剂量组间的统计学比较,因此暂不支持剂量优劣判断,但两种剂量均表现出持续的治疗效应,同时在用药期间,赛立奇单抗200mg剂量组ASAS20的应答率数值上优于赛立奇单抗100mg剂量组,提示临床可结合患者疾病特征、治疗目标及耐受情况进行个体化选择。这一信息对于长期管理和患者个体化管理尤为重要,AS作为慢性炎症性疾病,需要持续、稳定的治疗以维持疾病控制,剂量选择的灵活性有助于为不同疾病特征的患者带来更好的疾病应答。
在长期疾病管理方面,本研究提供了最长32周的疗效观察数据,显示赛立奇单抗治疗后患者的疾病活动度、躯体功能、生活质量等相关指标可保持稳定。现有证据提示,生物制剂治疗的持续性与患者长期功能预后密切相关,稳定的疾病控制是延缓结构进展的重要前提5。该分析的长期观察结果为临床评估赛立奇单抗在TNFi经治患者中的维持治疗价值提供了依据,也为制定长期随访与治疗调整策略提供了本土化参考。
赛立奇单抗100 mg和200 mg剂量在TNFi经治患者中第16周即显示显著疗效,且疗效持续至第32周,各项指标进一步改善,且32周内疗效稳定。上述结果表明,赛立奇单抗可作为中国TNFi经治、活动性AS患者的有效循证治疗选择。

医学博士
山东大学齐鲁医院风湿科副主任医师
山东省医学会风湿病学分会委员
山东省医师协会风湿病学分会常务委员
一、剂量选择强调个体化,为临床决策提供现实依据
本研究提示赛立奇单抗100 mg与200 mg剂量均可达预设疗效终点,200mg组相较100mg组16周ASAS20应答率虽然没有统计学差异,但数值上更优,为临床提供了灵活选择空间。临床实践中可综合考虑患者疾病活动度、体重、耐受性及治疗成本等因素进行剂量选择。由于目前国内外指南对于不同人群IL-17A抑制剂推荐给药剂量仍未明确,导致临床实践中对于TNF经治患者的用药方案不一。一项在美国开展的真实世界研究中,53.8%的患者使用了翻倍剂量的IL-17A抑制剂9,这一结果提示,对于一部分AS患者,使用翻倍剂量的IL-17A抑制剂可能是更优的治疗选择,对于IL-17A抑制剂的个体化给药剂量仍需进一步探索和优化。
二、TNFi治疗史可能影响IL-17A抑制剂的用药策略
TNFi是最早获批用于治疗活动性AS患者的生物制剂,但40%患者存在TNFi应答不佳或者不耐受。对于既往接受过TNFi的AS患者,有文献提示IL-17A抑制剂的疗效不及既往未接受过TNFi的患者10。在临床实践中也往往能够发现TNFα经治的患者使用IL-17A抑制剂后疾病活动度的改善不理想。在赛立奇单抗的事后分析中,赛立奇单抗不仅在总人群的疗效积极,在TNFi经治患者中的16周ASAS20应答率相较于未接受过TNFi的患者数值更高,这一研究结果是否能够在真实世界中得到验证令人期待。
三、强化长期管理策略,重视持续疗效与安全性监测
基于生物制剂持续治疗与长期功能预后的密切关系,临床在长期管理中应定期评估ASDAS-CRP、BASFI及生活质量指标,达到治疗目标者维持治疗可能有更大获益,避免不规律用药或过早停药。在赛立奇单抗的事后分析数据中,赛立奇单抗32周各疗效指标维度数值均优于16周的疗效数据,这意味着,AS患者在使用IL-17A抑制剂的过程中通过延长用药时间,能够持续降低疾病活动度,让患者得到疾病的长效控制。
参考文献:
[1] Liang J, et al. Efficacy of Xeligekimab in TNFi-experienced Active Ankylosing Spondylitis: Phase III Post Hoc Analysis. APLAR 2025; Poster No.199.
[2] Gu J, et al. Efficacy of xeligekimab in adults with ankylosing spondylitis: subgroup analysis from a randomized, double-blind, placebo-controlled phase 3 trial. APLAR 2025; Poster No.185.
[3] Sieper J, Deodhar A, Marzo-Ortega H, et al. Secukinumab efficacy in anti-TNF-naive and anti-TNF-experienced subjects with active ankylosing spondylitis: results from the MEASURE 2 Study. Ann Rheum Dis. 2017;76(3):571-592.
[4] Song Y, Chen H. Predictors of Health-Related Quality of Life in Patients with Ankylosing Spondylitis in Southwest China. Patient Prefer Adherence. 2021;15:1887-1894. Published 2021 Aug 28.
[5] Ji X, Wang Y, Ma Y, et al. Improvement of Disease Management and Cost Effectiveness in Chinese Patients with Ankylosing Spondylitis Using a Smart-Phone Management System: A Prospective Cohort Study. Biomed Res Int. 2019;2019:2171475. Published 2019 Feb 25.
[6] Bilici R, Alp GT, Çelikdelen SÖ, Öztürk MA, Kekilli M. TNF ınhibitor resistance in ankylosing spondylitis: is Helicobacter pylori the overlooked culprit?. Clin Rheumatol. 2025;44(8):3201-3207.
[7] Wang J, Lou W, Li Y, Jiang Y, Jiang X, Yang L. Progress in targeted therapy for ankylosing spondylitis: A review. Medicine (Baltimore). 2024;103(48):e40742.
[8] Atzeni F, Carriero A, Boccassini L, D'Angelo S. Anti-IL-17 Agents in the Treatment of Axial Spondyloarthritis. Immunotargets Ther. 2021;10:141-153. Published 2021 May 3.
[9] Joshi R, Latremouille-Viau D, Meiselbach MK, et al. Characterization of Patients with Ankylosing Spondylitis Receiving Secukinumab and Reasons for Initiating Treatment: A US Physician Survey and Retrospective Medical Chart Review. Drugs Real World Outcomes. 2019 Mar;6(1):1-9.
[10] Michelsen B, Lindström U, Codreanu C, et al. Drug retention, inactive disease and response rates in 1860 patients with axial spondyloarthritis initiating secukinumab treatment: routine care data from 13 registries in the EuroSpA collaboration. RMD Open. 2020 Sep;6(3):e001280.
本资料仅供医疗卫生专业人员医学科学交流,不用于推广目的。
审校专家 | 马蕾 刘岩
点评专家 | 李洁
查看更多