查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





血管组 董漪
记忆犹新的是2016年ISC 期间我曾经写过《脑室出血该怎么治疗?再来点Tpa也许也不错,可减少致残率。ISC大会上汇报了: Tpa治疗脑室内出血,而且血肿越大,疗效越好。如果能清除90%的患者。因此,在Danial Hanley时隔MISTIE III的欣喜消息。
MISTIE III旨在探索微创脑室引流血肿清除术能否降低脑出血患者的死亡率,通过Tpa可溶解大部分血块,使得残存血块小于15ml,因此使得脑出血患者的生存功能。
MISTIE III是一项三期、开放、盲法终点评估研究,在美国、加拿大、欧洲、亚洲、澳洲的78家医院进行。纳入18岁以上非创伤性幕上出血30ml以上的脑出血患者。通过电脑随机数字进行中心随机入组分配(四个/组或者六个/组)。干预为基于影像指导下的MISTIE 治疗(每8小时10mg tPA,最多给药9次),对照组为标准内科治疗。主要终点为良好预后,即基于基线情况(脑出血量、年龄、格拉斯哥昏迷评分、脑室内出血量、血块部位)校正后,365天时的改良RANKIN 评分0-3分。统计方法采用了改良的意向性分析。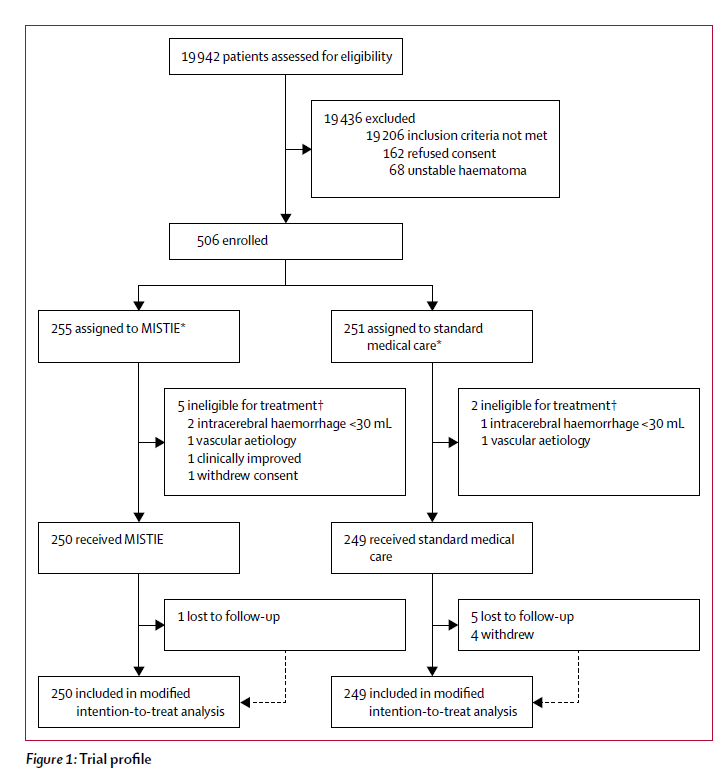
本研究纳入了2013年12月30日至2017年8月15日期间506例脑出血患者,255例随机至MISTIE组,251例随机至标准治疗组。共计499例患者接受了随机分配的治疗,并纳入改良意向性分析。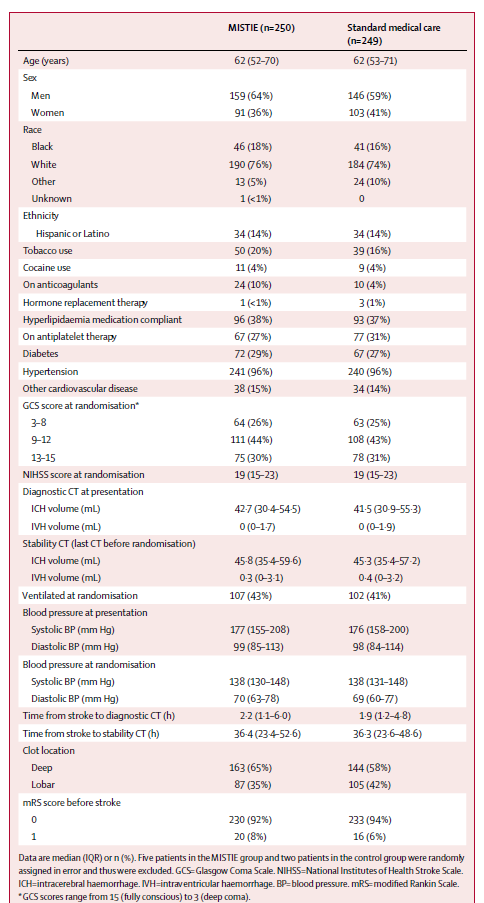

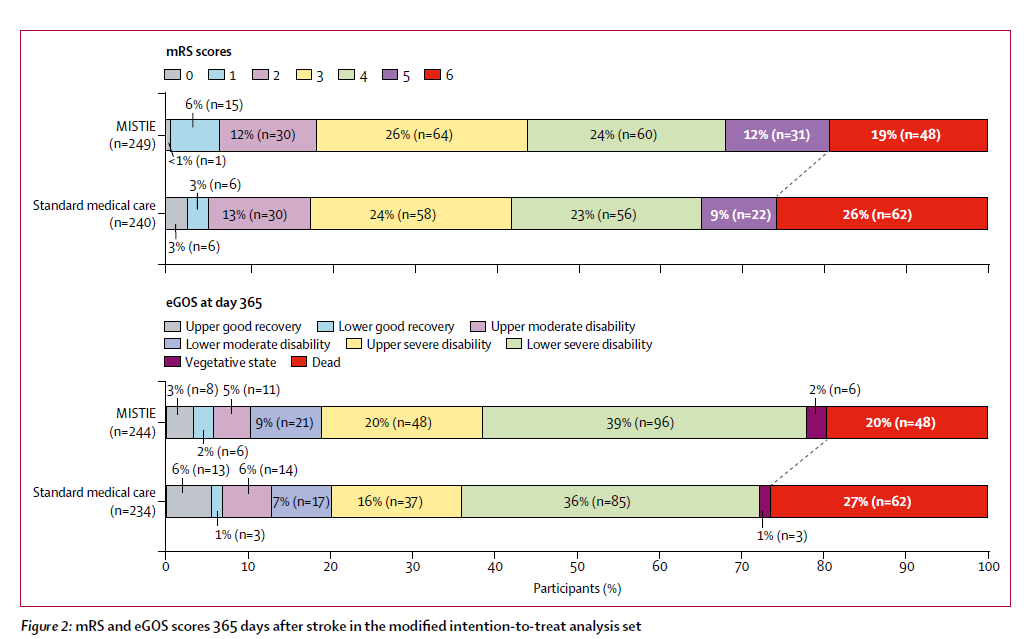
经过365天随访,MISTIE组45%的患者以及对照组41%的患者达到了经基线情况校正后的良好结局(mRS 0-3分)(校正后差异4% [95% CI –4 to 12]; p=0·33)。
敏感性有序逻辑回归分析模型发现MISTIE组的优势比:mRS 5分为0·60(p=0·03), :mRS4分为0·84 (p=0·42), :mRS 3分为0·87 (p=0·49), and :mRS 2分为0·82 (p=0·44)。
 7天内死亡率 MISTE组为2/255(1%),对照组10/251(4%),两组存在显著差异 (p=0·02) 。30天内死亡率 MISTE组为24/255(9%),对照组37/251(15%),两组存在不存在显著差异(p=0·07)。两组间安全性类似。
7天内死亡率 MISTE组为2/255(1%),对照组10/251(4%),两组存在显著差异 (p=0·02) 。30天内死亡率 MISTE组为24/255(9%),对照组37/251(15%),两组存在不存在显著差异(p=0·07)。两组间安全性类似。
30天内并发症率 MISTIE组为75/255(30%),对照组84/251(33%),两组存在显著差异 (p=0·012) 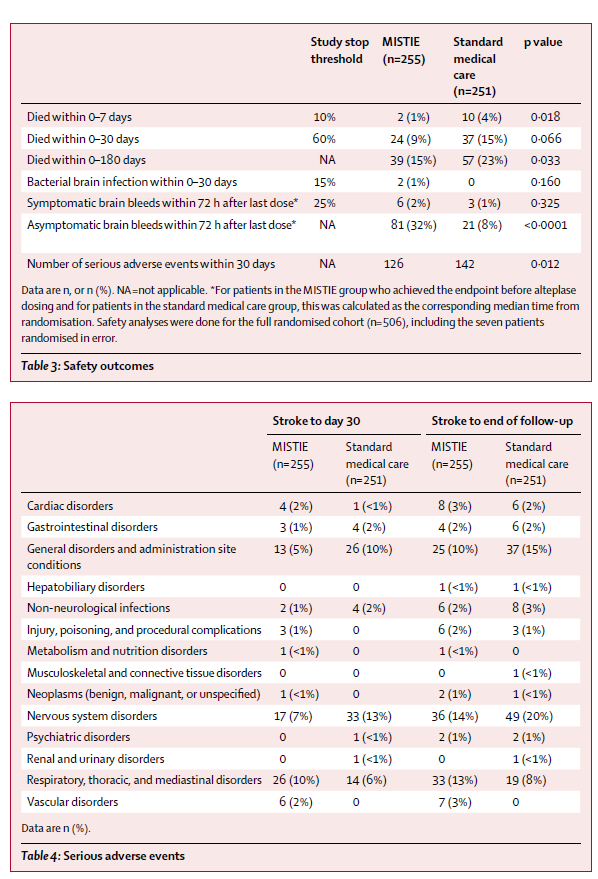
因此,本研究证实虽然MISTIE治疗并不能改善365天时患者达到良好预后的比例,但这样的手术方式是安全的。
Reference
Daniel F Hanley*, Richard E Thompson*, Michael Rosenblum, Gayane Yenokyan*, Karen Lane*, Nichol McBee*, Steven W Mayo*,et al.Efficacy and safety of minimally invasive surgery with
thrombolysis in intracerebral haemorrhage evacuation (MISTIE III): a randomised, controlled, open-label, blinded endpoint phase 3 trial. Lancet. February 7, 2019
感谢虞雁南及斯坦福大学图书馆的支持
查看更多