查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





近年来,随着免疫治疗的兴起,非小细胞肺癌(NSCLC)的治疗格局发生了翻天覆地的变化。
目前对于驱动基因阴性可手术NSCLC,免疫治疗奠定了其治疗地位,并涌现了三种围手术免疫治疗模式:包括单纯免疫新辅助(“餐前点心”模式)、单纯免疫辅助(“餐后甜点模式”)和免疫新辅助+术后免疫辅助巩固(“三明治”模式)。基于CheckMate-816研究的结果,FDA两年前批准了PD-1单抗-纳武利尤单抗用于可手术NSCLC的新辅助治疗。
随后,可手术NSCLC领域涌现了多项围手术期免疫治疗的随机对照研究,这些研究在CheckMate-816术前应用免疫治疗的基础上不同程度地引入了术后辅助免疫治疗措施,以期进一步降低复发和转移的风险。其中包括KEYNOTE-671、Neotorch、AEGEAN、NADIM Ⅱ、CheckMate 77T以及RATIONALE-315等。这些围手术期研究均显示出了延长的无事件生存期(EFS)的结果。
但是,对于已经接受了新辅助免疫检查点抑制剂的患者,术后继续该治疗能带来多少额外的疗效获益?治疗相关不良反应(TRAE)又会增加多少?哪些患者能豁免这些额外的辅助免疫?这些问题因为缺乏头对头比较的研究而引起广泛争议。

近日,中山大学肿瘤防治中心张力/洪少东团队在《美国医学会杂志》(JAMA)子刊JAMA Network Open(IF=13.8)公布了一项对比免疫“餐前点心”模式和免疫“三明治”模式的研究,为这些学术界热切关心的问题提供了初步答案,为指导后续临床实践和临床试验设计提供了研究数据。
张力教授及洪少东副主任医师为该研究通讯作者,周溢鑫副主任医师、李岸霖硕士研究生、余慧博士研究生、王钰虹医师为共同第一作者。该研究得到了国家自然科学基金、广东省自然科学基金杰出青年项目等资助。
这项研究总共纳入了5项临床研究(截止至2023-7-31),包括KEYNOTE-671、Neotorch、AEGEAN、NADIM Ⅱ和CheckMate 816。研究总共对2385名患者的数据进行了分析。
在免疫“三明治”模式的研究中,患者接受了3至4个周期的新辅助PD-(L)1单抗联合含铂化疗,并在术后接受了一年(NADIM Ⅱ为半年)的辅助PD-(L)1单抗治疗。经过7.8个月至23.9个月的中位随访时间,免疫“三明治”模式的两年生存率为80.9%-85.0%,而免疫“餐前点心”模式(即CheckMate-816模式)的两年生存率为82.7%。
研究进一步通过间接分析方法对比了免疫“三明治”模式与免疫“餐前点心”模式的疗效及安全性。结果显示,两者在五事件生存(EFS)期方面的治疗效果相当(HR=0.90, 95% CI 0.63~1.30; P=0.588)。这一相似性在大多数亚组中均保持一致,包括年龄、性别、地区、ECOG PS、疾病分期和组织学类型。
值得注意的是,对于未达到病理完全缓解(pCR)的患者,额外辅助治疗可能有助于改善EFS的趋势(HR=0.82, 95% CI 0.56-1.21; P=0.323)。然而,在非吸烟者中、PD-L1 TPS(肿瘤比例评分)表达≥50%的患者中,以及使用卡铂的患者中的特定亚组里,额外辅助治疗可能损害EFS获益。
在总生存(OS)方面,尽管围手术期模式与新辅助模式均显著降低了死亡风险(与单独化疗相比),但间接分析进一步显示,两种模式之间在OS方面并无显著差异(HR 1.18, 95% CI 0.73-1.90; P=0.511)。这表明,在降低死亡风险方面,两种模式的效果相似。
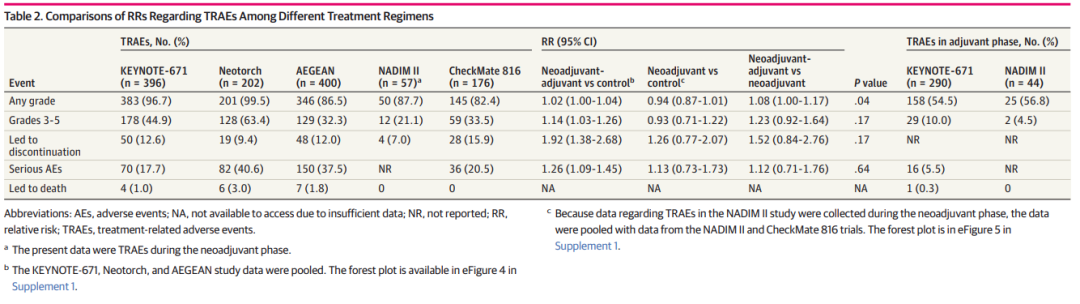
在安全性方面,围手术期模式任意级别和3~5级治疗相关不良反应(TRAE)的发生率分别为86.5%~99.5%和32.3%~63.4%。KEYNOTE-671和NADIM Ⅱ研究报道的辅助免疫治疗阶段新出现的任意等级的TRAE发生率分别为54.5%和56.8%,3~5级TRAE发生率分别为10.0%和4.5%。
进一步,通过间接对比,免疫“餐前点心”基础上额外增加免疫辅助治疗,增加了8%任意等级TRAE的发生风险(RR=1.08,1.00至1.17,P=0.038),且3-5级TRAE发生风险也有增加的趋势(RR=1.23,0.92至1.64,P=0.167)。
此外,免疫“三明治”模式中,导致死亡的TRAE发生率在1.0%至3.0%之间,而在免疫“餐前点心”模式中并未报告与治疗相关的死亡事件。
基于该研究结果,对于可手术的NSCLC患者,在接受新辅助PD-(L)1单抗并根治性手术后,额外的辅助免疫治疗是否能进一步增加患者预后暂无定论。
该研究结果揭示,对于NSCLC围手术期免疫治疗,似乎“less is more”。在头对头比较的临床研究验证结果出来之前,医生在制定临床决策时,必须综合考虑患者的生物标志物、对先前治疗的疗效及耐受性、患者的治疗积极性以及免疫毒性的易感性等因素,审慎关注额外辅助免疫治疗所带来的潜在风险和有限获益。
未来需要基于高维度多组学研究,对可手术NSCLC患者个性化免疫治疗策略提供依据。
查看更多