查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





滤泡性淋巴瘤(FL)作为最常见的惰性非霍奇金淋巴瘤之一,一线治疗后复发率居高不下,约 20%-30% 患者存在早期进展(POD24),二线及以上(2L+)治疗长期面临 “缓解浅、持续短、耐药快” 的临床困局。
全球多中心Ⅲ期 EPCORE FL-1 研究的顶刊结果,为 2L+ FL 治疗带来颠覆性突破:Epcoritamab(艾可瑞妥单抗)联合来那度胺(R²)方案,以显著的疗效优势、独特的作用机制、可控的安全性及固定疗程设计,全面超越传统标准治疗,有望重新定义 2L+ FL 的治疗范式。
EPCORE FL-1 是一项在全球 30 个国家 189 个中心开展的开放标签、随机对照Ⅲ期研究(NCT05409066),共纳入 488 例接受过至少一线化学免疫治疗的复发 / 难治性(R/R)FL 患者,按 1:1 随机分配至 Epcoritamab+R² 组(243 例)和 R² 单药组(245 例)。
研究核心终点为独立审查委员会(IRC)评估的中位无进展生存期(PFS)和总缓解率(ORR),关键次要终点包括 CR 率、缓解持续时间(DoR)、至下次抗淋巴瘤治疗时间(TTNT)及安全性。中位随访 14.8 个月的意向性治疗(ITT)人群分析结果,发表于《柳叶刀》并在 2025 年 ASH 年会同步公布。
所有关键疗效数据均严格引自 EPCORE FL-1 的《柳叶刀》全文(参考文献1)
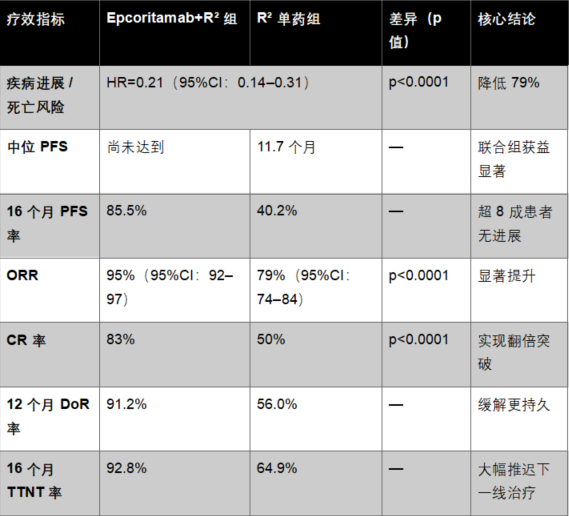
亚组获益全覆盖:无论是否存在 POD24、CD20 单抗耐药、双重难治(抗 CD20 + 烷化剂)、高肿瘤负荷或 FLIPI 高危等特征,Epcoritamab+R² 的疗效优势均与整体人群一致,真正实现 “广谱获益”,填补了高危难治人群的治疗空白。

优势一:机制革新,绕开耐药,精准 T 细胞重定向杀伤
Epcoritamab 是采用 DuoBody 技术研发的 CD3×CD20 双特异性抗体,Fc端部分效应子功能被设计沉默,不依赖 ADCC/CDC 效应,彻底绕开传统 CD20 单抗的耐药通路。其通过 “双靶点桥接” 机制,一端结合肿瘤细胞表面的 CD20(即使低表达),另一端招募 T 细胞并激活,释放穿孔素与颗粒酶直接裂解肿瘤细胞。
这一机制优势在临床中得到直接验证:EPCORE FL-1 研究中,CD20 耐药 / 低表达亚组的患者,接受 Epcoritamab+R² 治疗的获益与整体人群完全一致,解决了 2L+ FL 的核心耐药难题。

基于 Blood 杂志发表的 Ⅰb/Ⅱ期研究结果(文献2),EPCORE FL-1 采用最长 12 个周期(约 1 年)的固定疗程设计,无需长期维持治疗。这种模式既实现了 83% 的高 CR 率,又减少了长期药物暴露带来的毒性,兼顾疗效与患者生活质量。
同时,Epcoritamab 为皮下注射制剂,无需静脉输注,将来可能在门诊即可完成给药,大幅减少患者住院时间与往返医院的成本,显著提升治疗依从性。

优势三:安全性可控,免疫相关毒性温和易管理
安全性数据严格遵循 EPCORE FL-1 原文及 FDA 说明书(文献3),整体不良反应与各单药已知安全特征一致,无新安全信号:
1. 血液学毒性:最常见的 3 级及以上不良反应为中性粒细胞减少(联合组 69% vs 单药组 42%),通过常规支持治疗可快速缓解,粒缺伴发热发生率仅 6%,远低于传统化疗方案;
2. 免疫相关毒性:细胞因子释放综合征(CRS)多为 1–2 级,中位缓解时间仅 24 小时,仅 26% 的患者需使用托珠单抗干预;免疫细胞相关神经毒性综合征(ICANS)发生率极低,仅1例1级病例,3天内缓解,无严重 ICANS 报告;
感染风险:通过规范的肺孢子菌肺炎和疱疹病毒预防,仅观察到1例肺孢子菌肺炎感染,安全性可控。

优势四:覆盖高危人群,填补临床未满足需求
2L+ FL 中,POD24、双重难治、高肿瘤负荷等高危人群预后极差,传统方案疗效有限。EPCORE FL-1 研究证实,Epcoritamab+R² 在这些亚组中仍能带来显著获益:POD24 患者疾病进展风险大幅度降低,双重难治患者 CR 率与整体人群持平,彻底打破了高危人群的治疗瓶颈。
在此之前,2L+ FL 的标准治疗以 R² 方案为主,但该方案难以实现深度缓解,多数患者快速复发,耐药后只能依赖化疗、CAR-T 等毒性较大或经济负担沉重的治疗手段。
EPCORE FL-1 的研究结果,彻底打破了这一僵局:Epcoritamab+R² 方案成为目前首个在随机Ⅲ期研究中,证实较标准治疗显著改善 2L+ FL 患者 PFS、ORR 和 CR 率的 CD3×CD20 双特异性抗体联合方案。其“机制革新、疗效碾压、安全可控、潜在的门诊便捷性”的核心优势,重新定义了 2L+ FL 的治疗标准,让“深度缓解、长期控病”成为可能。
目前,Epcoritamab 已在美国、欧盟、日本等 65 个以上国家和地区获批淋巴瘤相关适应症,全球临床应用经验不断积累。尽管其在国内的上市申请暂未获批,但 EPCORE FL-1 的惊艳数据,已为其在中国的临床应用奠定了坚实基础,未来有望快速获批,惠及国内广大 2L+ FL 患者。
EPCORE FL-1 研究的成功,标志着 2L + 滤泡性淋巴瘤治疗正式进入“双抗联合无化疗”的全新时代。Epcoritamab 凭借独特的 T 细胞重定向机制,绕开耐药壁垒;以固定疗程实现深度持久缓解,兼顾疗效与安全性;更通过对高危人群的全面覆盖,填补了临床未满足需求。
相信在不久的将来,随着 Epcoritamab 在国内的获批与临床应用,将彻底改写 2L+ FL 的治疗格局,为更多复发 / 难治性滤泡性淋巴瘤患者带来长期生存的希望,让“惰性淋巴瘤,也能实现长期控病”不再是奢望。
参考文献
1 Falchi, Lorenzo, et al. "Epcoritamab, lenalidomide, and rituximab versus lenalidomide and rituximab for relapsed or refractory follicular lymphoma (EPCORE FL-1): a global, open-label, randomised, phase 3 trial." The Lancet 407.10524 (2026): 161-173.
2 Falchi L, Sureda A, Leppä S, et al. Fixed-duration epcoritamab plus R² drives favorable outcomes in relapsed or refractory follicular lymphoma[J]. Blood, 2025, 146(22): 2629-2640. DOI: 10.1182/blood.2025029909.
3 FDA. EPKINLY™ (epcoritamab-bysp) injection prescribing information[EB/OL]. 2023.
来源:会议来稿
查看更多