查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过






乳腺癌是全球女性最常见的恶性肿瘤之一。尽管临床已经形成较成熟的分型体系,但即使属于同一分型,不同患者的治疗反应和预后仍存在明显差异。这提示,乳腺癌在传统分型之外,可能还存在更深层次的生物学差异。
近年来研究表明,染色质可及性变化以及转录因子调控网络重塑,是肿瘤获得侵袭能力和转移能力的重要基础。但由于缺乏能够稳定保留患者肿瘤特征的研究模型,乳腺癌在表观遗传层面的系统研究仍较为有限。
2026年3月16日,复旦大学附属肿瘤医院郭小毛、俞晓立、陈飞、沈敏洪团队合作在《Cell Stem Cell》发表研究论文Paired patient-derived organoids reveal transcription factor-driven epigenetic remodeling in breast cancer metastasis。研究团队通过建立乳腺癌患者来源类器官(PDOs)生物库,并结合多组学分析,系统描绘了乳腺癌进展过程中的表观遗传变化图谱,识别出四种不同的乳腺癌表观遗传状态,并进一步发现驱动淋巴结转移的关键转录因子网络。
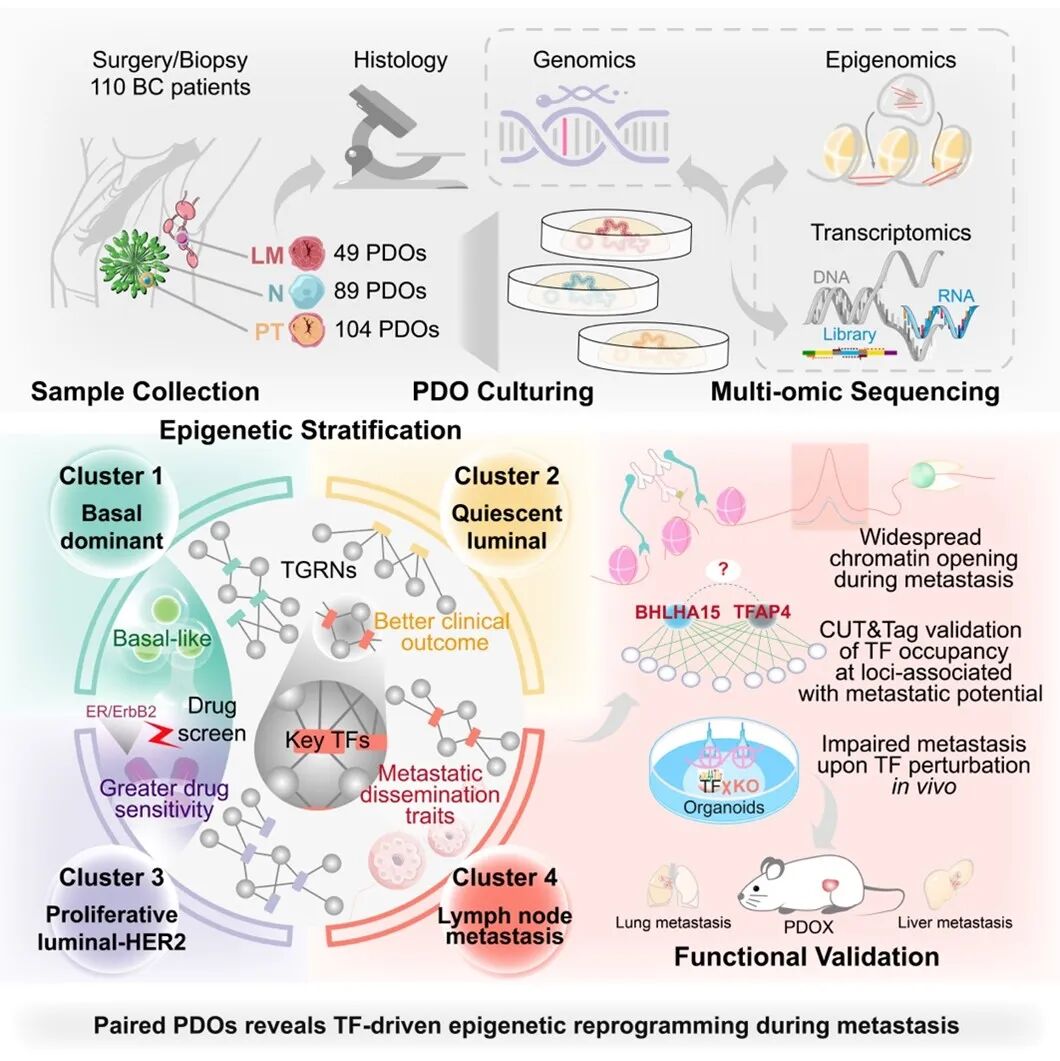
图形摘要
建立乳腺癌类器官生物库,为研究肿瘤进展提供新模型
研究团队建立了来源于原发肿瘤、癌旁正常组织及淋巴结转移灶的配对乳腺癌患者来源类器官(PDOs)生物库。多项验证结果显示,这些类器官能够较好保留患者肿瘤的关键特征:肿瘤PDOs呈现实性、囊性和葡萄状等多种形态,而正常乳腺组织PDOs则更加均一。H&E染色及免疫组化进一步证实,PDOs 在ER、PR、HER2、Ki-67等关键标志物表达方面与来源组织高度一致。该类器官模型为研究乳腺癌发生发展及转移机制提供了重要实验平台。
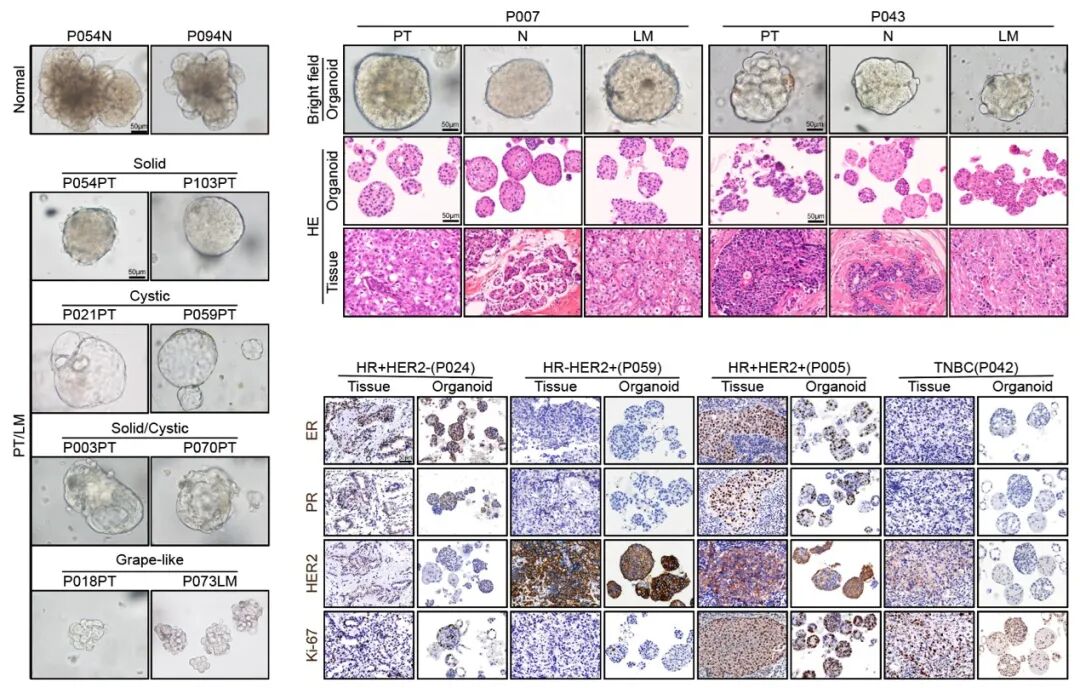
乳腺癌类器官组织病理学特征
发现4种乳腺癌表观遗传状态,揭示新的肿瘤异质性维度
在此基础上,研究团队整合染色质可及性与转录组等多组学数据,识别出 4种不同的乳腺癌表观遗传状态。其中:
Cluster1为基底样主导状态,侵袭性较强;
Cluster2更接近正常乳腺上皮状态,增殖活性较低;
Cluster3为高增殖的 luminal-HER2 相关状态,激素应答和细胞周期通路活跃;
Cluster4主要来源于淋巴结转移灶,富集ECM重塑和EMT等转移相关通路。
研究提示,乳腺癌除了传统分型之外,还存在一套反映肿瘤动态演化的表观遗传状态体系。
不同表观状态对应不同预后与治疗敏感性
研究团队在多个独立乳腺癌患者队列中进一步验证发现,前三种主要来源于原发灶的表观遗传状态均可稳定识别,并与临床结局密切相关。其中Cluster2患者预后最好,而Cluster1和Cluster3与更高复发风险相关,Cluster1还与更差总体生存相关。
同时,基于PDOs的药物筛选显示,Cluster3对内分泌治疗、HER2靶向治疗及部分CDK4/6抑制剂更为敏感。这一结果提示,表观遗传状态有望成为传统分型之外的新型治疗分层依据。
锁定驱动乳腺癌淋巴结转移的关键转录因子
在四种状态中,研究团队重点关注Cluster 4(淋巴结转移相关状态)。通过整合ATAC-seq和RNA-seq数据,研究人员构建了转录因子调控网络,并筛选出一组关键转录因子,包括:MEF2A、NR2F1、NR2F2、NFATC4、ZNF148、TFAP4 和 BHLHA15。其中TFAP4与BHLHA15表现出最强的协同调控特征。进一步的CUT&Tag、CRISPR敲除及动物实验表明:当TFAP4或BHLHA15被敲除后,EMT和细胞外基质重塑等转移相关程序明显下降,肺和肝转移负担显著降低。这表明,这些转录因子在乳腺癌淋巴结转移过程中发挥关键驱动作用,并有望成为未来抗转移治疗的重要靶点。
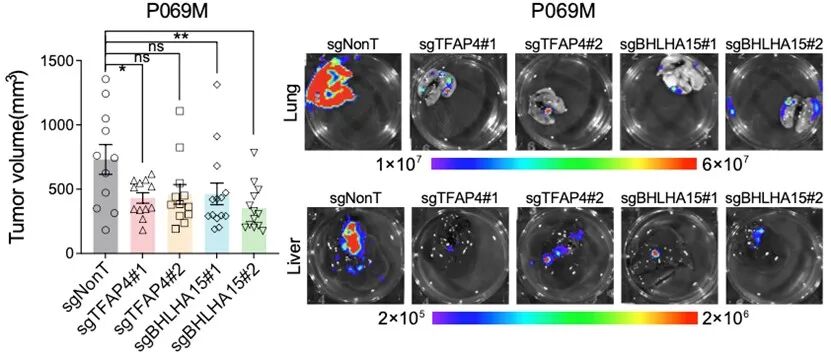
TFAP4/BHLHA15 敲除抑制乳腺肿瘤体内生长
研究意义与未来展望
本研究通过建立乳腺癌 PDO 生物库并开展系统性多组学分析,描绘了乳腺癌进展过程中的表观遗传变化图谱,提出了四种具有不同生物学特征的表观遗传状态。研究不仅深化了对乳腺癌异质性和转移机制的认识,也为患者分层和精准治疗提供了新的思路。
研究团队表示,未来将进一步依托 PDO 模型,探索建立新辅助放疗分层体系并解析局部晚期乳腺癌放疗抵抗的分子机制,为乳腺癌患者精准治疗策略的优化提供新的研究基础。

复旦大学附属肿瘤医院陈飞、俞晓立、郭小毛、沈敏洪教授为论文的共同通讯作者,复旦大学肿瘤医院博士后饶欣欣、王静雯为论文的共同第一作者。该研究得到了复旦大学附属肿瘤医院吴炅书记、邵志敏主任、江一舟副院长、徐彦辉教授、许蜜蝶教授、章真教授、唐爽教授以及同济大学张勇教授的大力支持。研究工作获得国家重大慢性非传染性疾病防控研究专项、国家自然科学基金等项目资助。
来源 | 复旦大学附属肿瘤医院
查看更多