查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





脑海绵状血管畸形(CCM)是中枢神经系统常见的出血性血管异常之一,是青壮年脑卒中和癫痫的重要致病因素。尽管其临床危害明确,但长期以来,散发性CCM “从何而来、为何进展”始终未明,近年来该疾病遗传机制的突破,开启了这一疾病从体细胞突变发生、发展到出血致病的系列机制研究。
近日,首都医科大学宣武医院神经外科洪韬教授、张鸿祺教授团队于Brain杂志发表了题为"Angiogenic switching in cerebral cavernous malformations driven by MAP3K3-PIK3CA synergy"的研究论文。该研究揭示MAP3K3与PIK3CA突变协同激活PI3K–AKT–mTOR通路,诱导CCM中类似肿瘤的血管生成开关,并验证了PI3Kα抑制剂Alpelisib在CCM中的治疗潜力。

在2026年的最新研究中,团队将研究焦点锁定在疾病进展的“临界点”,提出并系统验证了CCM中的血管生成关键开关。研究发现,MAP3K3与PIK3CA突变并非简单叠加效应,而是通过协同激活MAPK–PI3K信号网络,使脑血管内皮细胞跨越维持稳态的阈值,从相对静息状态跃迁为持续异常血管生成状态。一旦这一“开关”被打开,病灶便不再是局灶性异常,而进入持续扩张、结构失稳和反复出血的自我放大通道。这一发现在机制层面解释了临床中长期存在的现象:为什么部分CCM病灶在早期相对稳定,而一旦进展便难以逆转;为什么不同患者之间出血风险存在巨大差异。
研究构建了内皮细胞特异性的Map3k3I441M突变、Pik3caH1047R突变及两者叠加突变转基因同窝对照小鼠,利用Cdh5(PAC)–CreERT2系统在出生后诱导突变表达。通过体视镜、micro-计算机体层摄影(CT)三维成像、组织学及免疫荧光评估病灶形态和信号通路激活。研究对动物模型行单细胞核糖核酸(RNA)测序及bulk RNA测序,还分析了12例人类CCM单细胞数据以验证发现的临床相关性。机制验证方面,通过腺相关病毒(AAV)载体在成年Pik3ca GOF小鼠中递送MAP3K3I441M或VEGFA,观察MAP3K3 GOF与PIK3CA GOF的协同作用。最后,在治疗探索上采用PI3Kα抑制剂Alpelisib来干预小鼠模型及患者来源CCM类器官(图1)。
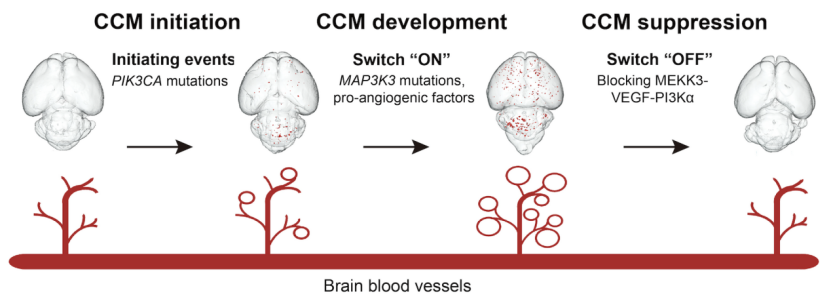
图1 PIK3CA突变可启动CCM的发生,但病灶的生长还需要额外的触发因素,如MAP3K3突变或促血管生成因子水平升高。PI3Kα抑制剂Alpelisib在临床前模型中可阻CCM的形成,并逆转促血管生成信号通路的激活。
本研究系统地阐明了MAP3K3与PIK3CA突变的协同致病机制。两种突变并非简单的效应叠加,而是有着明确的功能分工与协同作用。成年时期MAP3K3基因突变或VEGFA表达增加均可作为Pik3caH1047R突变基础上的“二次打击”因素,促进单纯Pik3caH1047R突变产生的静脉发育异常(DVA)发展为典型的CCM病变。在临床转化层面,研究明确了PI3Kα作为可干预的核心靶点,Alpelisib在小鼠模型和患者来源类器官中均显示出显著疗效,为这一长期依赖外科手术的疾病提供了药物治疗的新方向。
本研究是该团队CCM系列研究的延续。2021年团队在Brain发表封面论文,首次明确MAP3K3和PIK3CA突变是散发性CCM的核心遗传驱动因素;2023年再次在Brain报道MAP3K3激活突变可独立诱发CCM,并建立了高度还原人类疾病特征的动物模型。2026年的发表研究在前期工作基础上,完成了从突变发现、机制解析到治疗策略探索的完整研究链条,为CCM的精准治疗奠定了重要基础。
来源 宣医图书馆
查看更多