查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





免疫治疗目前已经成为晚期非小细胞肺癌(NSCLC)的一线标准治疗。治疗过程中发生寡转移,尤其是淋巴结进展,提示可能出现了免疫耐药。本期我们将分享一例晚期非小细胞肺癌寡转移患者一线接受替雷利珠单抗联合局部巩固放疗后病灶持续缓解,无进展生存期(PFS)达36个月。由此可见,寡转移患者继续原免疫治疗方案(IO TBP),同时联合局部放疗可提升长期生存获益。
王立峰 教授
南京大学医学院附属鼓楼医院
医学博士,主任医师,教授
南京大学医学院附属鼓楼医院肿瘤中心副主任
南京大学医学院附属鼓楼医院肺癌亚专业负责人
中国抗癌协会国际医疗交流分会常委
CSCO非小细胞肺癌专家委员会委员
中国生物工程学会肿瘤靶向治疗分会常委
中国肿瘤药物临床研究专委会 委员
中国医疗保健国际交流促进会胸部肿瘤学分会 常委
江苏省抗癌协会化疗专业委员会副主任委员
江苏省整合医学研究会肺癌专委会副主任委员
江苏省医师协会肿瘤化疗与生物治疗医师分会常委
江苏省生物技术协会肿瘤精准医学诊疗专业委员会常委
德国莱比锡圣乔治医院肿瘤中心、意大利锡耶纳大学医院(AOUS)免疫肿瘤科高级访问学者
美国梅奥医院(MAYO CLINIC)癌症中心临床访问医生
美国约翰霍普金斯医院临床访问医生
吕昕 教授
南京鼓楼医院
南京鼓楼医院主治医师
熟悉常见恶性肿瘤的诊治,现主要从事肺癌精准诊断、靶向治疗、免疫治疗、肺癌精准立体定向放疗及综合治疗相关领域的研究
熟练掌握常规及复杂情况下的CT引导下精准肺穿刺活检术
参与多项国内外临床研究,并曾参与ESMO等国际重要学术会议交流
一般情况:患者,男性,65岁,既往无吸烟史。
主诉:患者于2021年2月因“头晕伴左侧肢体乏力”至脑科医院查头颅MRI提示颅内占位考虑转移,至我院就诊。
既往史:无。
胸腹部CT提示右肺下叶占位,大小约5.2cm×4.3cm,邻近支气管局部闭塞,纵隔及右肺门内肿大淋巴结,考虑肺癌可能性大。非小细胞肺癌相关抗原21-1 17.90ng/ml,显著升高。ECT-全身骨显像未见明显异常。头颅MRI提示右侧额、顶叶占位,考虑转移瘤可能。
胸部CT及头颅MRI
右肺穿刺活检病理结果:非小细胞癌,低分化,难以进一步分型。免疫组化:癌细胞表达P63(散在+),P40(散在+),NapsinA(-),TTF-1(-); VENTANA anti-ALK(D5F3)肿瘤细胞(-) ;对照组织:阳性对照(+),阴性对照(-)。本例活检组织呈实性片状分布伴较多坏死,结合免疫表型以腺癌可能性大。NGS检测:未检测到驱动基因突变。tTMB:21.1突变/MB,高表达。PD-L1表达:阴性,TPS<1%(Dako 22C3)。
右肺腺癌 Ⅳ期伴脑转移,无驱动基因突变,TMB高表达,PD-L1阴性,ECOG评分2分。
治疗过程:患者于2021-02-26行颅内病灶立体定向放疗(PTV 50Gy/10f),并于2021-03-15、2021-04-09接受2周期“白蛋白紫杉醇+卡铂+替雷利珠单抗”治疗,首次疗效评价PR,肺部及颅内病灶明显缩小,肢体乏力症状缓解。
2021-02
2021-04
胸部CT及头颅MRI
继续2周期“白蛋白紫杉醇+卡铂+替雷利珠单抗”治疗,肺部病灶稳定,颅内病灶持续缓解。
2021-04
2021-06
胸部CT及头颅MRI
联合治疗结束后,调整为“白蛋白紫杉醇+替雷利珠单抗”维持治疗2周期,病情持续稳定。
2021-06
2021-08
胸部CT及头颅MRI
2021-06-03出现II°肝损及手脚远端肢体麻木,2021-08-03开始调整改行替雷利珠单抗单药维持治疗。
完善PET-CT:检查右肺占位伴葡萄糖代谢增高;主肺动脉窗一枚淋巴结葡萄糖代谢增高;结合病史,符合右下肺肺癌伴淋巴结转移。
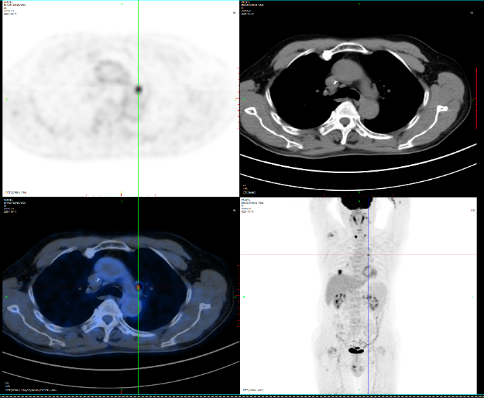
2021-11-11开始行肺部病灶巩固性放疗,右下肺病灶+主动脉旁淋巴结(PTV 5Gy×10f),后继续替雷利珠单抗单药维持治疗。放疗后肺部病灶有所缩小,放疗后4月左右出现射野范围内炎症,给予甲强龙40mg静脉滴注×7d,后逐步减量,1月后复查未见明显吸收,3月后炎症范围有所吸收,继续替雷利珠单抗维持治疗。
胸部CT
患者至2023-03替雷利珠单抗治疗满2年,目前随访复查肺内病情稳定,一线PFS 36个月。
免疫联合化疗目前已经成为驱动基因阴性晚期NSCLC患者的标准一线治疗方案,中位无进展生存期(mPFS)约8-10个月。一线治疗效果对患者的整体生存具有关键的影响。有研究表明转移性NSCLC一线系统治疗后,大多数的进展事件,包括颅内和颅外,仅发生在基线时已经存在的病灶,而非新的病灶[1]。局部巩固治疗可以通过根治性放疗或手术来控制所有已知病灶,从而改善患者的PFS。相比广泛转移患者,有限的远处转移患者(寡转移)具有更惰性的表型,或可从局部巩固治疗中获益。
2016年一项对比晚期寡转移NSCLC一线治疗未发生进展的患者,接受局部巩固(所有病灶放疗±手术)序贯维持治疗和单纯维持/观察治疗的多中心随机Ⅱ期研究结果公布,中位随访18.7个月,局部巩固治疗组mPFS为11.9个月,显著高于单纯维持/观察组3.9个月(HR 0.35,p=0.005),同时推迟了新发病灶出现的时间6.2个月,中位总生存(OS)延长超过2年(41.2个月vs 17.0个月,HR 0.40, p=0.017),两组间的毒性没有显著差异[2-3]。该研究首次证实,对于转移灶数量有限的患者,局部巩固治疗可以延长一线系统治疗的PFS,延缓新的转移扩散,进而延长患者的OS。2019年Bauml等人开展了一项单臂Ⅱ期研究,51例寡转移(转移灶≤4)患者接受了全部病灶的局部消融治疗(Local ablative therapy, LAT)后序贯帕博利珠单抗,获得了19.1个月的mPFS,显著超越了6.6个月的历史数据,也超过了既往研究报道中仅行全病灶消融治疗的14.4个月[4]。免疫治疗时代,合并寡转移患者在系统药物治疗有效的前提下,加入放疗等局部巩固治疗,可实现强强联合,提高患者的免疫应答。
本次病例报道中,患者接受颅内SBRT和一线替雷利珠单抗联合化疗2周期后,肺部和颅内病灶明显缩小,达到PR,随后4周期替雷利珠单抗联合化疗,肺部病灶持续稳定,补充PET CT显示主肺动脉旁淋巴结转移,该情况下选择进行肺部及淋巴结的巩固性放疗,序贯替雷利珠单抗维持治疗满两年,肿块消融呈纤维化改变,达到临床治愈状态,患者一线治疗至今PFS超过36个月,显著超越了历史数据,免疫加局部放疗极大地延缓了免疫耐药,延长了患者的生存期,目前该模式已经在我们肺癌亚专业组常规开展。
免疫治疗与放疗的联合应用是肺癌治疗领域的研究热点之一。无论单病灶或多病灶放免联合治疗耐受性尚可,且可获得较好的疾病缓解率和生存。但由于转移性患者情况较为复杂,仍需严谨的随机对照试验研究,以明确获益群体、放疗剂量、放疗时机和安全性管理等问题,以实现放疗和免疫治疗联用的效应最大化,从而为晚期NSCLC患者提供最优的治疗指导。
参考文献
[1] Rusthoven KE, er al. Is there a role for consolidative stereotactic body radiation therapy following first-line systemic therapy for metastatic lung cancer? A patterns-of-failure analysis. Acta Oncol. 2009; 48(4):578–583.
[2] Gomez DR, et al. Local consolidative therapy versus maintenance therapy or observation for patients with oligometastatic non-small-cell lung cancer without progression after first-line systemic therapy: a multicentre, randomised, controlled, phase 2 study. Lancet Oncol. 2016 Dec;17(12):1672-1682.
[3] Gomez DR, et al. Local Consolidative Therapy Vs. Maintenance Therapy or Observation for Patients With Oligometastatic Non-Small-Cell Lung Cancer: Long-Term Results of a Multi-Institutional, Phase II, Randomized Study. J Clin Oncol. 2019 Jun 20;37(18):1558-1565.
[4] Bauml JM, et al. Pembrolizumab After Completion of Locally Ablative Therapy for Oligometastatic Non-Small Cell Lung Cancer: A Phase 2 Trial. JAMA Oncol. 2019 Sep 1;5(9):1283-1290.
本文由中国医学论坛报社整理和编辑
查看更多