查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





研究名称:Adagrasib对比多西他赛治疗KRAS G12C突变非小细胞肺癌(KRYSTAL-12):一项随机、开放标签、III期试验[Adagrasib versus docetaxel in KRASG12C-mutated non-small-cell lung cancer (KRYSTAL-12): a randomised, open-label, phase 3 trial]
发表期刊:《柳叶刀》(The Lancet, IF=88.5)
通讯作者:莫树锦
主要作者单位:香港中文大学
对于经治的KRAS G12C突变晚期非小细胞肺癌,后线标准治疗多西他赛疗效有限且毒性显著。KRYSTAL-12研究作为确证性III期试验,证实靶向药物adagrasib相比化疗可显著延长无进展生存期,提高客观缓解率并控制症状负担,为这一既往“不可成药”靶点的人群确立了更优的治疗选择。
KRYSTAL-12研究是一项随机、开放标签、III期试验,旨在评估adagrasib对比多西他赛在既往经治的KRASG12C突变晚期或转移性NSCLC患者中的效果。该研究共纳入453例经铂类化疗+抗PD-1/PD-L1治疗进展的KRASG12C突变晚期NSCLC患者(ECOG 0~1,稳定脑转移允许入组)。
入组患者以2:1随机分配接受adagrasib或多西他赛治疗。主要研究终点是由盲法独立审查委员会(BICR)根据RECIST v1.1评估的PFS期。次要研究终点包括BICR评估的ORR、缓解持续时间(DOR)、OS期、1年OS率和安全性。
关键研究结果
中位随访时间为7.2个月,adagrasib组的中位PFS期为5.5个月(95%CI 4.5-6.7),多西他赛组为3.8个月(95%CI 2.7-4.7),HR=0.58(95%CI 0.45-0.76),P<0.0001。Adagrasib组的PFS期在所有亚组中均优于多西他赛组,包括有脑转移的患者。
Adagrasib组的ORR为32%(95%CI 26.7-37.5),多西他赛组为9%(95%CI 5.1-15.0),OR=4.68(95%CI 2.56-8.56),P<0.0001。Adagrasib组有3例完全缓解,93例部分缓解;多西他赛组有14例部分缓解。
Adagrasib组的中位DOR为8.3个月(95%CI 6.1-10.4),多西他赛组为5.4个月(95%CI 2.9-8.5)。
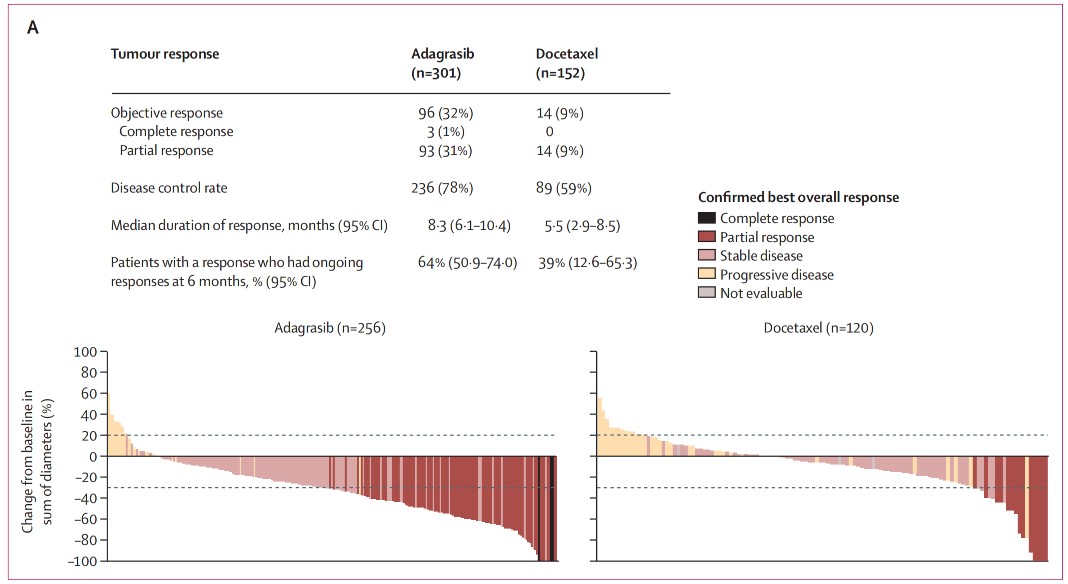
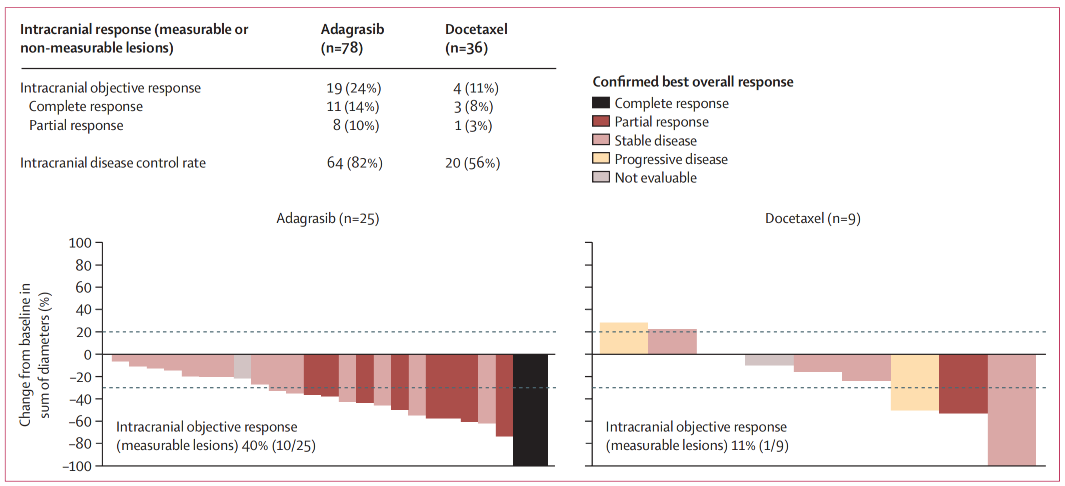
在有基线脑转移的患者中,adagrasib组的颅内ORR为24%(95%CI 15.3-35.4),多西他赛组为11%(95%CI 3.1-26.1)。在有可测量CNS靶病灶的患者中,adagrasib组的颅内ORR为40%(10/25),多西他赛组为11%(1/9)。
基于肺癌症状量表(LCSS)评估,adagrasib组患者症状恶化的风险低于多西他赛组,中位时间至LCSS恶化分别为3.0个月和1.5个月,HR=0.57(95%CI 0.45-0.74)。
Adagrasib组和多西他赛组分别有94%和86%的患者报告了任何级别的治疗相关不良事件(TRAEs)。Adagrasib组最常见的TRAEs为腹泻(53%)、呕吐(35%)和恶心(34%),多为1级。多西他赛组最常见的TRAEs为腹泻(31%)、贫血(30%)和乏力(27%)。
两组中分别有47%和46%的患者报告了3级及以上的TRAEs。Adagrasib组最常见的3级及以上TRAEs为ALT升高(8%)和AST升高(6%);多西他赛组为中性粒细胞减少(11%)、中性粒细胞减少症(10%)和乏力(10%)。Adagrasib组有4例治疗相关死亡(癫痫、肝衰竭、肝缺血和原因不明各1例),多西他赛组有1例治疗相关死亡(败血症)。
KRAS是人类癌症中最常见的癌基因之一,其中KRASG12C突变在肺腺癌患者中约占14%,但在亚洲NSCLC患者中仅约4%。KRASG12C突变的NSCLC是一种难以治疗的肺癌亚型,既往在化疗或免疫治疗进展后治疗选择有限。
Adagrasib是一种口服的小分子KRASG12C抑制剂,它能够不可逆且选择性地结合KRASG12C的非活性GDP结合态。在Ⅱ期KRYSTAL-1研究中,Adagrasib已显示出对KRASG12C突变的晚期NSCLC患者的临床活性,ORR达到43%,中位PFS期为6.5个月,中位总生存(OS)期为12.6个月。
在I/II期KRYSTAL-1研究的汇总队列中,Adagrasib的中位OS期达到14.1个月,2年OS率为31%,长期安全性特征可控。并且在稳定、经治脑转移及未经治脑转移NSCLC患者中显示出有前景的颅内活性。
基于以上结果,Adagrasib获得美国加速批准和欧盟附条件批准,同时被NCCN指南(2a类)、ESMO指南列为推荐方案,用于经治晚期KRASG12C突变NSCLC患者(包括脑转移)。
KRYSTAL-12研究的阳性结果,标志着KRAS G12C突变非小细胞肺癌的治疗正式迈入精准靶向时代。这是继CodeBreaK 200研究之后,第二个在III期层面证实KRAS G12C抑制剂优于标准二线化疗的里程碑式试验。Adagrasib凭借其独特的长半衰期和高脑穿透性等药理学优势,不仅在无进展生存期上实现了对化疗的显著超越,更在客观缓解率和缓解持续时间上展现出质的飞跃,32%的缓解率对化疗时代的个位数缓解率而言是颠覆性的进步。
全球诊疗格局来看,该研究为KRAS G12C突变患者提供了更高等级的确证性证据,进一步巩固了adagrasib作为这一分子亚群标准治疗的地位。尤其值得注意的是其颅内疗效数据,40%的颅内客观缓解率为伴脑转移这一常见且难治的人群带来了新的希望。基于KRYSTAL-1研究中adagrasib对未经治疗的脑转移患者同样有效的数据,未来研究的重点将转向前线治疗的探索,如联合免疫治疗或化疗,以进一步提升初始治疗的深度和持久性。同时,随着KRAS G12C抑制剂的广泛应用,深入理解并获得性耐药机制并开发新一代抑制剂或联合疗法,将是未来持续攻关的方向,最终目标是为患者构建更优的全病程管理策略。
KRYSTAL-12研究主要研究者之一的莫树锦教授曾在2024ASCO年会上公布了该研究的主要结果,并得到CSCO非小细胞肺癌诊疗指南的肯定。2025版CSCO诊疗指南认为KRYSTAL-12研究结果为既往经过化疗和免疫治疗后进展的KRASG12C突变NSCLC进一步提供了确证性依据。鉴于该药物目前尚未在国内获批上市,CSCO诊疗指南将其作为III级推荐方案,用于Ⅳ期KRASG12C突变型NSCLC的后线治疗。

香港中文大学医学院副院长(转化与创业)
李树芬医学基金会肿瘤学教授
美国临床肿瘤学会院士(FASCO)
美国临床肿瘤学会董事局成员(2018 年 6 月至 2022 年 5 月)
国际肺癌研究协会(IASLC)前任主席和现任财务主管
香港科学院院士
获 2015 年的邦妮·阿达里奥奖、2017 年的美国临床肿瘤学会(FASCO)院士奖以及 2017 年的保罗·邦恩科学奖
在国际同行评议期刊上发表了 220 多篇文章,包括 the New England Journal of Medicine、Science、Lancet 和 Journal of Clinical Oncology,并为多部社论和教科书撰稿
The Journal of Clinical Oncology 和其他国际期刊的胸部肿瘤学副主编
每一项临床研究都倾注着研究团队的心血结晶。学习过后,您是否有所收获?或有疑问想与主创团队分享?请在评论区留言,期待与您交流!

整理丨中国医学论坛报 胡岳
查看更多