查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





▼点击下图,查看更多ISC 2026重磅研究!
作者:复旦大学附属华山医院神经内科血管组 李嘉和 洪澜

2026年2月4日至2月6日,2026年国际卒中大会(ISC 2026)于美国新奥尔良召开。来自中国北京天坛医院的李姝雅教授代表LAIS研究者团队,在大会上发布了LAIS(Loberamisal for Acute Ischaemic Stroke)的Ⅲ期临床试验结果。

再灌注治疗仍然是急性缺血性卒中(AIS)早期管理基石,但其临床获益有限,相当比例的患者无法仅从再灌注策略中完全获益[1]。尽管神经保护策略有望改善卒中患者的临床预后,但其临床开发一直充满挑战。卒中治疗学术产业圆桌会议(STAIR)为多种神经保护疗法的研发提供了关键建议[2]。突触后致密蛋白95(PSD-95)抑制剂已显示出减轻缺血性脑损伤和发挥神经保护作用的潜力,尤其是在症状出现后3 h内给药时[3-5]。
除急性神经损伤外,卒中后抑郁和卒中后焦虑在第1年内影响约1/3的卒中幸存者,并与功能恢复不良和死亡率增加密切相关。然而,评估氟西汀等抗抑郁药的大规模临床试验未能证实其对卒中相关功能恢复的积极作用[6-8],突显了仅依靠抗抑郁药策略应对卒中后情绪障碍的挑战。
Loberamisal是一种双靶点神经保护剂,作用于PSD-95和含α2亚基的γ-氨基丁酸A型受体(α2GABA受体)活性通路。临床前研究表明,Loberamisal可降低神经兴奋性和神经炎症,同时发挥抗抑郁和抗焦虑作用[9]。在启动本项Ⅲ期试验前,研究团队开展了一项Ⅱ期剂量探索试验,该研究显示,在症状发作48 h内且基线美国国立卫生研究院卒中量表(NIHSS)评分为6~20分的AIS成人患者中,Loberamisal 40 mg组在疗效和安全性之间取得了最佳平衡,因此被选为Ⅲ期试验的剂量[10]。
基于此,来自首都医科大学附属北京天坛医院的王拥军院士和李姝雅教授团队开展了LAIS研究(Loberamisal for Acute Ischaemic Stroke)。这是一项在中国开展的多中心、随机、双盲、平行组、安慰剂对照的Ⅲ期临床试验,旨在评估发病48 h内的AIS患者中,静脉注射Loberamisal的有效性和安全性。李姝雅教授代表LAIS研究团队在ISC 2026大会上公布了此项研究的结果。

干预措施
符合条件的受试者按1: 1的比例随机分配,接受Loberamisal 40 mg或安慰剂治疗。研究药物为每日1次的1 h静脉输注,连续给药10 d。随机化根据症状发作至随机化的时间及研究中心进行分层。
年龄18~80岁
确认在症状发作48 h内的AIS
基线NIHSS评分7~20分
卒中前改良Rankin量表(mRS)评分≤1分
已接受或计划接受血管内机械取栓治疗
严重意识障碍(NIHSS 1a>1)
诊断为短暂性脑缺血发作(TIA)
目前正在使用抗抑郁药或抗焦虑药治疗
入组前使用过神经保护药物
主要终点:90 d时mRS评分为0~1分的患者比例
次要终点:① 90 d时mRS的滑动二分法分析;② 90 d时mRS总体分布情况;③ 第10 d与第30 d NIHSS评分较基线的变化;④ 第10 d与第30 d NIHSS较基线改善≥4分的比例;⑤ 90 d时Barthel指数≥95的比例。
严重不良事件(SAE)、重要不良事件、全因死亡率、疑似非预期严重不良反应(SUSARs)以及因不良事件导致的治疗中止。
蒙哥马利-阿斯伯格抑郁评定量表(MADRS)评估的抑郁情况
汉密尔顿焦虑量表(HAMA)评估的焦虑情况
计划总样本量为998例。统计分析遵循ICH-E9(R1)指南,缺失数据采用多重填补法处理。
三、研究结果

研究于2024年7月24日至2025年4月8日期间,在中国32个中心共入组并随机化了998例患者,排除1例未接受研究治疗的患者后,共有997例受试者纳入改良意向性治疗(mITT)分析。
两组基线特征均衡。中位年龄63岁,中位基线NIHSS评分为8分,从症状发作至治疗开始的中位时间为25 h。
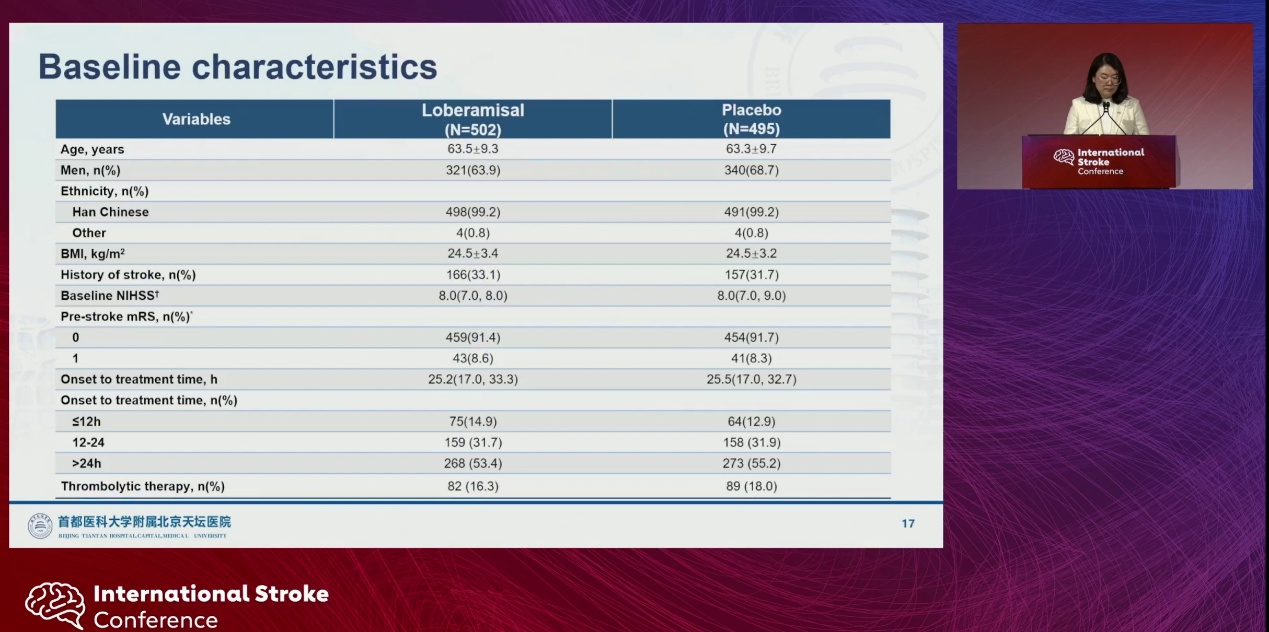
在90 d时,Loberamisal组有69.7%的患者达到mRS 0~1分,而安慰剂组为56.3%。Loberamisal组的相对风险比为1.24[95%置信区间(CI)1.22~1.36],绝对风险差为13.28%(95% CI 7.24~19.32),结果具有显著统计学意义。
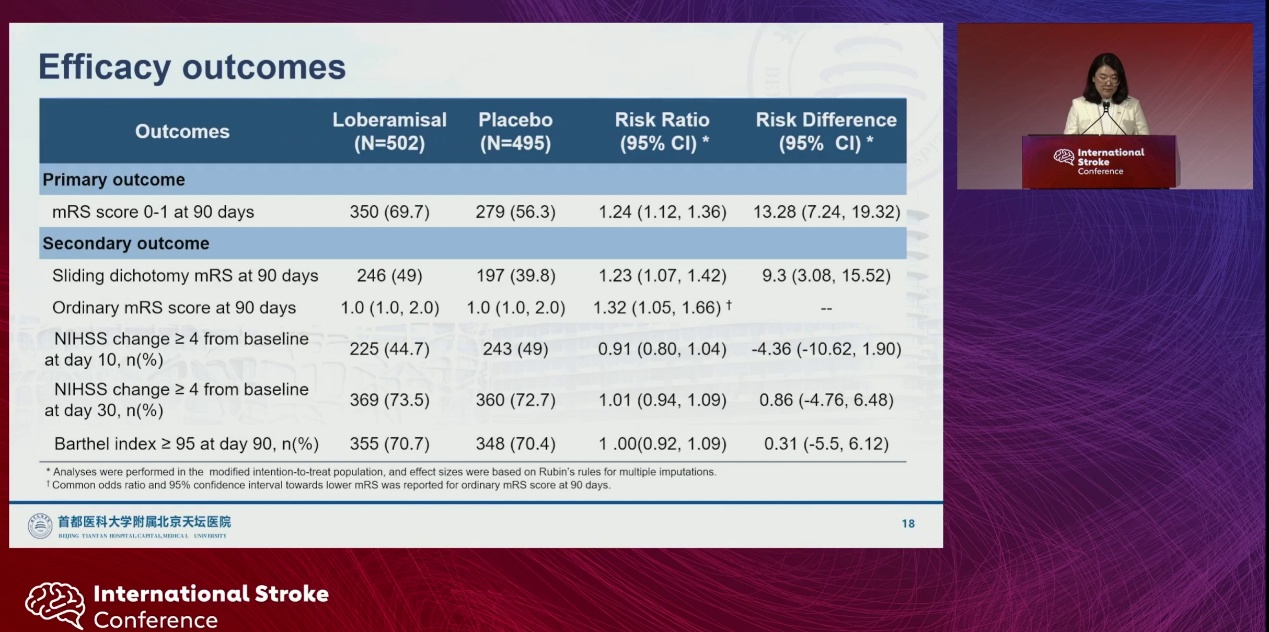
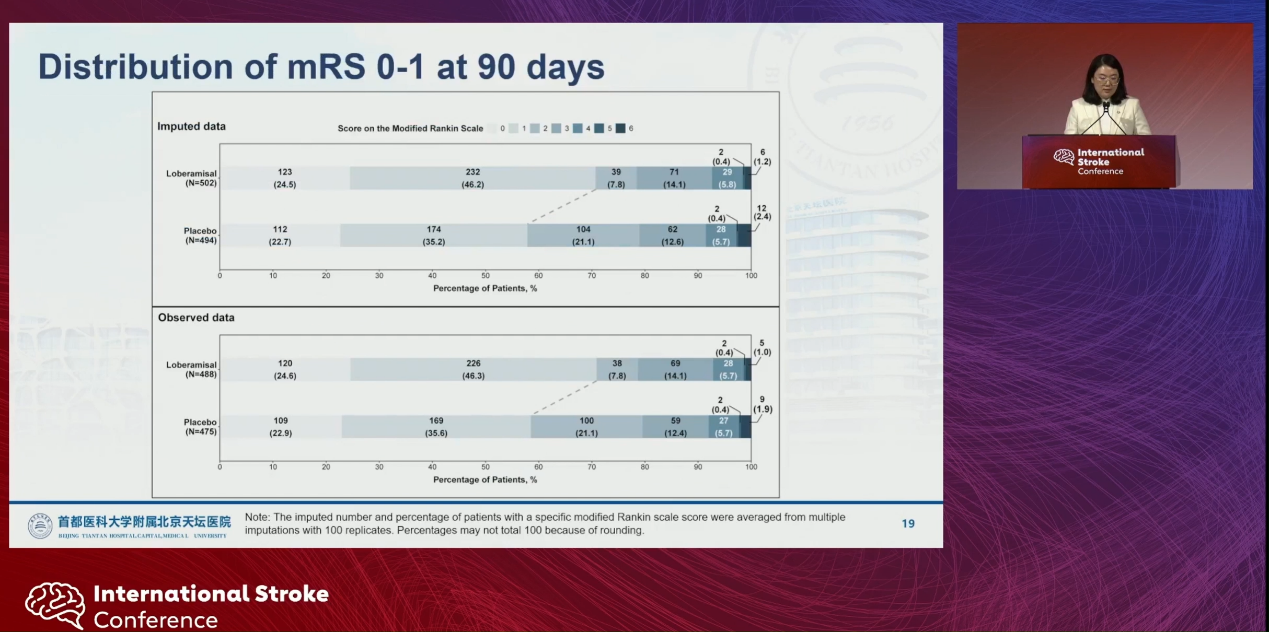
滑动二分法分析及mRS分布结果与主要终点一致。在NIHSS 改变及Barthel指数方面,两组差异未达到显著。
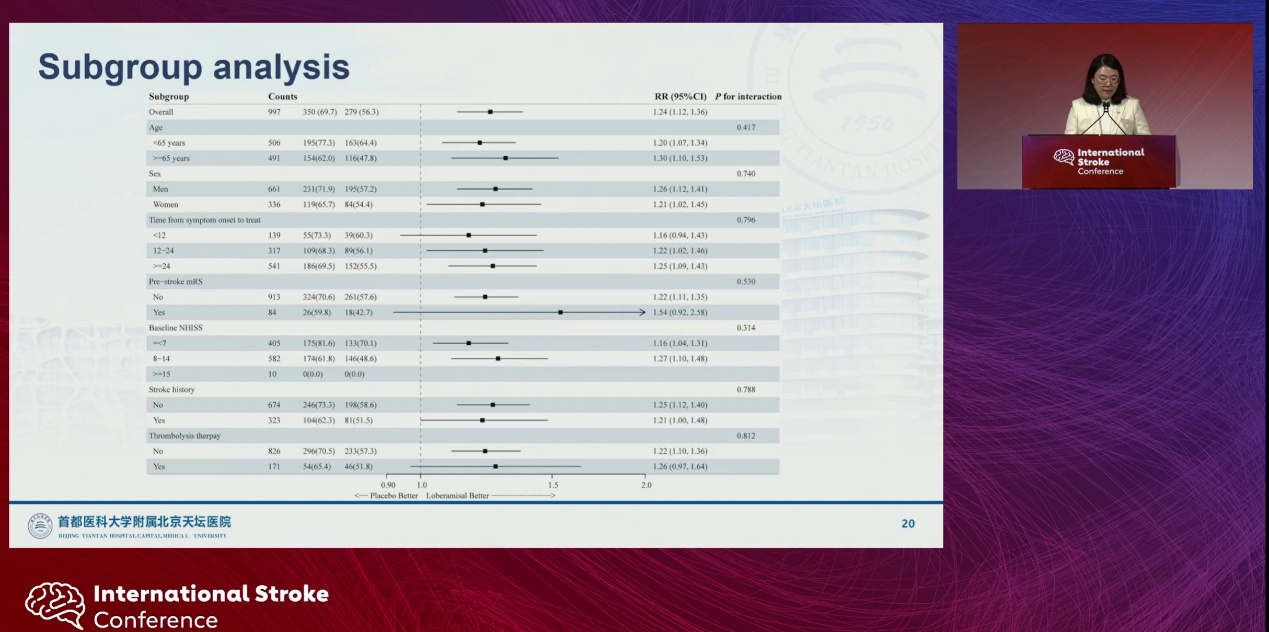
亚组分析未发现预设亚组间存在异质性。
Loberamisal组严重抑郁(8.6% 对13.1%,相对危险度0.65,95% CI 0.45~0.94)和中重度焦虑(中度焦虑:10.6% 对 14.7%, 相对危险度0.72,95% CI 0.51~0.998;重度抑郁:8.4% 对 12.3%,相对危险度0.68,95% CI 0.47~0.99)的风险较安慰剂组显著降低。
两组的总体安全性特征相当。数值上,Loberamisal组的SAE发生率(8.6% 对 10.7%,P=0.283)和全因死亡率(1.2 对 2.0%,P=0.300)略低于安慰剂组。试验期间未发生SUSARs。
四、研究结论

LAIS研究表明,对于起病48 h内的中重度AIS患者,Loberamisal治疗与90 d时优良功能预后(mRS 0~1)比例绝对增加13.28%相关,且具有良好的安全性。此外,Loberamisal还显示出降低卒中后严重抑郁和焦虑风险的潜力,验证了其双重神经保护及情绪调节机制。
尽管本试验的局限性(如排除血管内治疗患者)可能限制了结果对更广泛人群的普遍性,但这些发现有力支持了Loberamisal作为一种新型神经保护疗法在AIS治疗中的进一步研究与应用。
[1] FISHER M, SAVITZ S I. Pharmacological brain cytoprotection in acute ischaemic stroke - renewed hope in the reperfusion era [J]. Nat Rev Neurol, 2022, 18(4): 193-202.
[2] SAVITZ S I, BARON J-C, FISHER M. Stroke Treatment Academic Industry Roundtable X: Brain Cytoprotection Therapies in the Reperfusion Era [J]. Stroke, 2019, 50(4): 1026–31.
[3] HILL M D, GOYAL M, MENON B K, et al. Efficacy and safety of nerinetide for the treatment of acute ischaemic stroke (ESCAPE-NA1): a multicentre, double-blind, randomised controlled trial [J]. Lancet, 2020, 395(10227): 878-87.
[4] HILL M D, GOYAL M, DEMCHUK A M, et al. Efficacy and safety of nerinetide in acute ischaemic stroke in patients undergoing endovascular thrombectomy without previous thrombolysis (ESCAPE-NEXT): a multicentre, double-blind, randomised controlled trial [J]. Lancet, 2025, 405(10478): 560-70.
[5] CHRISTENSON J, HILL M D, SWARTZ R H, et al. Efficacy and safety of intravenous nerinetide initiated by paramedics in the field for acute cerebral ischaemia within 3 h of symptom onset (FRONTIER): a phase 2, multicentre, randomised, double-blind, placebo-controlled study [J]. Lancet, 2025, 405(10478): 571-82.
[6] Safety and efficacy of fluoxetine on functional recovery after acute stroke (EFFECTS): a randomised, double-blind, placebo-controlled trial [J]. Lancet Neurol, 2020, 19(8): 661-9.
[7] Safety and efficacy of fluoxetine on functional outcome after acute stroke (AFFINITY): a randomised, double-blind, placebo-controlled trial [J]. Lancet Neurol, 2020, 19(8): 651-60.
[8] Effects of fluoxetine on functional outcomes after acute stroke (FOCUS): a pragmatic, double-blind, randomised, controlled trial [J]. Lancet, 2018, 393(10168): 265-74.
[9] XU X, CHEN M, ZHU D. Reperfusion and cytoprotective agents are a mutually beneficial pair in ischaemic stroke therapy: an overview of pathophysiology, pharmacological targets and candidate drugs focusing on excitotoxicity and free radical [J]. Stroke Vasc Neurol, 2024, 9(4): 351-9.
[10] FENG B, LI H, XU S, et al. Loberamisal injection for the treatment of acute ischaemic stroke: a multicentre, randomised, double-blind, placebo-controlled phase II clinical trial [J]. Stroke Vasc Neurol, 2025.
查看更多