查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





作者:上海交通大学医学院附属仁济医院 谢亦乐 房静远 陈萦晅
PART.01
简要病史
现病史 患者男性,41岁,因“间断反酸3年”入院。患者自2020年起无明显诱因下出现间断反酸,无腹痛、恶心、呕吐、腹泻、便秘等不适,胃纳及体重无明显变化。2020年至2021年,患者先后于我院完善胃肠镜及胶囊内镜检查,示慢性萎缩性胃炎、多发胃、小肠、结肠息肉;此后间断服用抑酸剂、胃黏膜保护剂等药物对症治疗。现患者为明确病因,门诊拟“消化道多发息肉”收治入院。
既往史 患者2006年行听神经瘤切除术;2005年、2019年、2020年多次行舌根、喉部新生物息肉切除术。病理:黏膜慢性炎伴淋巴组织反应性增生,灶区不典型增生。2019年确诊桥本甲状腺炎(TGAb阳性,T3、T4、FT3、FT4无异常,未予药物治疗)。2023年1月甲状腺B超示弥漫性改变、甲状腺双侧叶多发占位-考虑增生性结节(TI-RADS3类)。2020年行多发性血管瘤切除术7次;2020年确诊特发性震颤,未服药治疗。
个人史 无吸烟史,偶有饮酒,频率为每月1~2次,每次饮用2两白酒。
家族史及家庭情况 患者父母曾行肠镜检查示结肠息肉(未见书面报告,息肉是否多发尚不明确);奶奶曾确诊骨髓瘤,未行胃肠道相关检查;患者无兄弟姐妹,目前育有一子(15岁),身体康健。
PART.02
入院查体
T:36.8℃ P:87次/分 R:21次/分 BP:120/77 mmHg
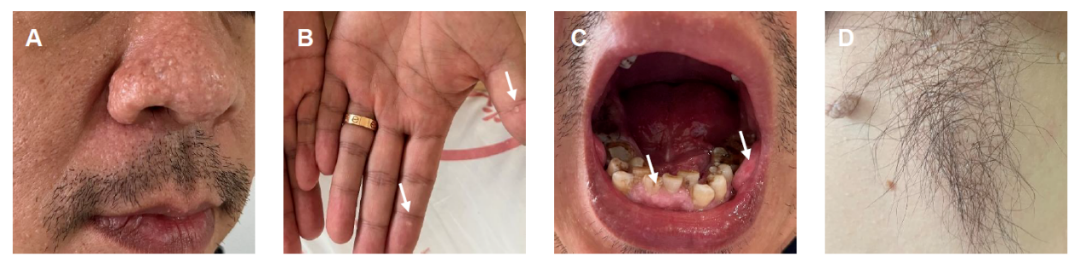
患者头围61cm,皮肤色素沉着,面部、颈部可见多发扁平或隆起米粒大小丘疹;鼻外形偏大,鼻头肥厚,鼻部多发丘疹(图A);双侧手掌可见丘疹(图B)。唇色红润,齿龈萎缩,齿列不齐,伴龋齿,双侧口腔内颊黏膜增厚肥大(图C);双侧腋下、颈部多发灰褐色带蒂皮赘,大小不一(图D);双侧腹部、前臂外侧、大腿外侧可触及多发质软、可移动的皮下肿块;双侧前臂内侧可见数条血管瘤手术瘢痕。腹部平坦,无腹部压痛,无腹部反跳痛,肝脾肋下未及,肠鸣音正常,移动性浊音阴性,双下肢无水肿。
PART.03
临床检查
01
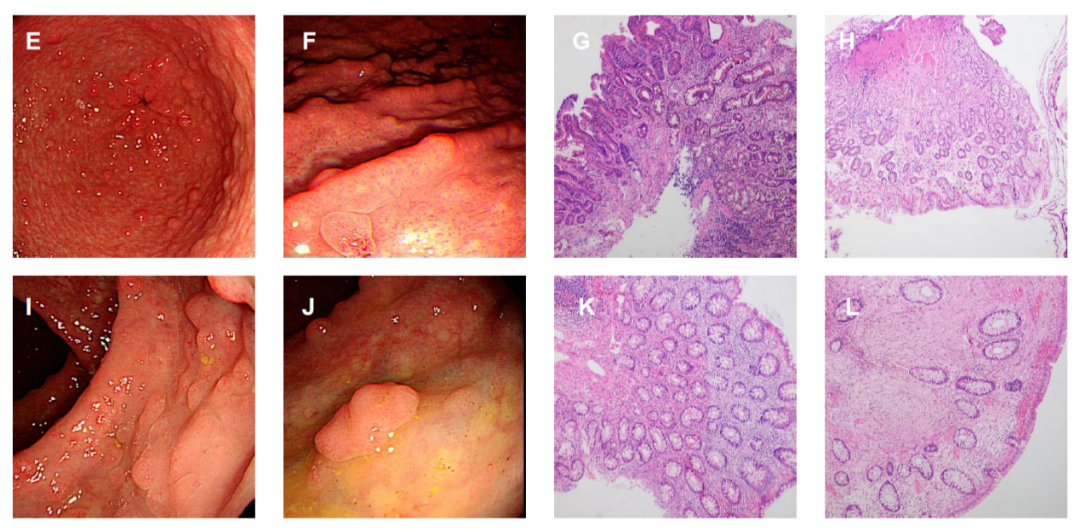
2020年8月 我院胃镜:胃体黏膜呈细颗粒状,可见多枚直径约0.2~0.4cm Is型及Isp型息肉,表面光滑或充血;胃角黏膜粗糙颗粒状;胃窦黏膜粗糙颗粒状,可见多枚直径约0.2~0.4cm Is型息肉,表面光滑或充血,红白相间,血管显露(图E-F);病理:慢性萎缩性胃炎。
02
2020年8月 我院肠镜:横结肠、降结肠、乙状结肠及直肠处可见多枚直径约0.2cm~0.8cm Is型或Isp型息肉(图I-J)。
03
2021年8月 我院胶囊内镜:小肠多发息肉(十二指肠、空肠上段、回肠下段多发小息肉,直径约0.4~0.5cm)。
04
2023年4月 外院胃镜:食管白斑、胃多发息肉、十二指肠多发息肉。病理:(十二指肠)管状腺瘤,(胃窦)炎性息肉(图G-H)。
05
2023年4月 外院肠镜:全结肠+直肠数十枚息肉样隆起,较大者0.8cm×0.8cm,乳头状,表面黏膜光整,基底部无蒂。病理:(升结肠)炎性息肉,(直肠)黏膜腺体慢性炎,无明显异常,固有层见多灶梭形细胞片状增生,免疫组化倾向神经纤维瘤(图K-L)。
06
2023年4月 外院小肠镜:回肠多发息肉,回肠末端见多发淋巴滤泡增生,回肠下段见数枚半球状隆起,大小约0.5cm×0.7cm。(EMR切除3枚)。病理:增生性息肉。
07
2023年5月 外院上腹平扫增强CT:肝脏未见明显异常;胆囊底部结节,息肉可能;右肾囊肿。
08
本次入院后血常规、生化、肝肾功能、肿瘤指标等未见明显异常。
PART.04
鉴别诊断
1、腺瘤性息肉综合征:主要包含家族性腺瘤性息肉病(FAP)、MUTYH相关息肉病(MAP)等。
FAP主要由腺瘤性息肉病(APC)基因突变引发,呈常染色体显性遗传,青少年时期在结直肠内出现大量腺瘤性息肉,恶变风险高。经典型FAP发病年龄更早,建议从10~12岁起开启结直肠癌筛查,必要时可进行预防性结直肠切除。
MAP 为常染色体隐性遗传,由MUTYH双等位基因胚系变异所致,发病年龄较FAP稍晚(多见于20~25岁后),息肉数量相对较少,以定期肠镜筛查为主要监测手段,当息肉进展超出内镜控制范围时推荐采取手术治疗。
2、错构瘤息肉综合征:涵盖黑斑-息肉综合征(PJS)、幼年性息肉综合征(JPS)、PTEN错构瘤肿瘤综合征(PHTS,包括Cowden综合征和Bannayan-Riley-Ruvalcaba综合征)、锯齿状息肉病综合征(SPS)、Cronkhite-Canada 综合征(CCS)等。
PJS为常染色体显性遗传,由 STK11 基因致病,核心表现为皮肤黏膜色素沉着(口周、手足为主)、胃肠道多发错构瘤性息肉(近段小肠最密集),伴肿瘤易感性;
JPS为常染色体显性遗传,与 SMAD4 或 BMPR1A 基因胚系突变相关,以胃肠道多发幼年性息肉(结肠最常见)为特征,易伴出血、贫血;
SPS以结肠多发大型锯齿状息肉为特征,确诊年龄多 50~60 岁,伴腺瘤或腺瘤家族史者需排查 MUTYH 突变;
CCS又称息肉-色素沉着-脱发-爪甲营养不良综合征,病因目前尚不清楚,散发性疾病,病因不明,多见于中老年人,除胃肠息肉外,还伴腹泻、色素沉着、脱发、爪甲异常、低蛋白血症等全身症状。
临床诊断需把握 “表型+基因”双核心:先通过息肉病理类型、伴随体征及家族史初步分型,再针对性检测STK11、SMAD4、PTEN等基因以明确诊断。
PART.05
罕见病诊断依据
结合患者的特殊外貌(大头、掌跖角化病、口腔黏膜乳头状瘤、面部皮肤丘疹、多发皮赘等)、相关器官病变(血管瘤、听神经瘤、甲状腺结节、桥本甲状腺炎)及多发性胃肠道息肉表现,考虑患者为Cowden综合征待排。
为进一步明确诊断,对本例患者进行了基因检测,结果显示PTEN基因c.635-1G>c(p.Asn212Ilefs)致病突变。综上该病例可确诊为“Cowden综合征”,其他诊断:胃、十二指肠、小肠、结肠多发息肉、食管白斑、双肾多发囊肿、胆囊底部息肉样病变、舌根部新生物、桥本甲状腺炎、甲状腺双侧叶多发占位(增生性结节可能)、听神经瘤个人史、血管瘤个人史、特发性震颤。
PART.06
诊疗及随访方案
目前仍缺乏针对Cowden综合征的特效治疗药物。管理核心为“对症治疗+肿瘤筛查+遗传干预”:① 内镜下息肉切除或手术治疗,缓解消化道症状;② 按亚型制定个性化筛查方案(Cowden综合征强化甲状腺、乳腺筛查);③ 遗传性亚型需开展家族遗传咨询与基因检测,明确亲属患病风险;④ 须同步纠正全身并发症,通过多学科协作改善预后。
根据以上原则,对该患者进行了疾病及健康宣教,建议其每年至少进行一次消化内镜检查,以及腹部、甲状腺和其他相关器官检查,以筛查恶性肿瘤。同时建议本例患者的儿子进行了基因检测,结果显示其子未携带 PTEN 突变。
PART.07
疾病介绍
胃肠道息肉综合征是一类由多种病因引发、具有多种临床表现的临床综合征,涵盖腺瘤性息肉综合征与错构瘤息肉综合征这两大类型。磷酸酶和张力蛋白同源物(PTEN)是关键的抑癌基因,其突变可引起PTEN错构瘤肿瘤综合征(PHTS),其中一型为Cowden综合征,是罕见的常染色体显性遗传的肿瘤综合征,患病率约为1/20万~1/25万。
Cowden综合征以累及所有胚层分化组织的多器官、多发性错构瘤为特征,同时伴有乳腺癌、甲状腺癌、子宫内膜癌、血管瘤高发风险。其主要表现集中在皮肤和胃肠道,以面部小丘疹、口腔黏膜乳头状瘤、肢端角化症及胃肠道多发性息肉为核心临床特征[Gastroenterology.2023;164(5):800-811]。临床医生有必要提高对Cowden综合征的认识,以确保准确识别患者。
该罕见病目前仍缺乏具体且敏感的治疗方法。国际Cowden联盟于2012年报告了368名PTEN胚系突变患者,发现乳腺癌、甲状腺癌、子宫内膜癌、结肠直肠癌、肾癌和黑色素瘤的标准化发病率升高[Clin Cancer Res.2012 Jan 15;18(2):400-7]。被诊断或高度怀疑患有Cowden综合征的患者应接受全面检查,定期筛查恶性肿瘤,并密切随访。确诊后,建议在35岁或更早的时候开始胃肠镜检查。若发现多发性息肉或腺瘤性息肉,应设定每年一次的监测间隔。多项研究提示,mTOR抑制剂雷帕霉素可阻断PHTS的血管病变生长(Cancer Discov. 2025 Jul 3;15(7):1350-1362),挽救PTEN突变疾病神经表型(Mol Psychiatry. 2025 Jul;30(7):3077-3089),促进晚期黏膜皮肤病变的快速消退(Cancer Res. 2008 Sep 1;68(17):7066-72)等。这些发现表明,mTOR抑制剂可能是Cowden综合征患者及其他涉及PTEN功能缺陷的肿瘤综合征的化学预防和治疗的合适选择。
点评与启示
消化科陈萦晅教授:本例患者兼具全消化道多发息肉、特殊外貌(大头、皮肤丘疹等)及多器官合并症(听神经瘤、血管瘤、桥本甲状腺炎等),与该病“多系统受累”的核心特征相符。诊疗团队的核心亮点在于跳出“局部治局部”的思维局限,以“一元论”思维整合多系统线索,关联特殊体征与既往病史提出遗传性综合征假设。通过“全消化道内镜定位与评估+基因检测确诊”的阶梯化方案,精准区分FAP、PJS等相似综合征,避免了误诊漏诊。该名患者多次于耳鼻咽喉、内分泌科、血管外科、消化科等就诊,对临床医生而言,一是需加强对罕见疾病的学习,例如本例患者具有特殊的“过目不忘”的外貌表现,需强化相关关联警惕性;二是精准采集家族史,通过全面体格检查捕捉特异性体征;三是需践行“对症治疗+肿瘤筛查+遗传咨询”的规范化管理。

中国科学院院士
中国医学科学院学术咨询委员会学部委员,中华医学会消化病学会候任主任委员。
上海交通大学讲席教授、上海交通大学医学院消化科学院院长,上海交通大学医学院附属仁济医院消化学科带头人、仁济医院消化病中心主任,上海市消化疾病研究所长,仁济医院安徽医院(国家区域医疗中心)执行院长。上海市消化内科临床医学中心主任、上海市消化内科临床质控中心主任。国家卫健委内科消化重点实验室主任。担任仁济医院副院长兼消化科主任十余年。
国家杰出青年科学基金获得者、教育部“长江学者”特聘教授、科技部重点研发专项首席、国家自然科学基金委创新研究群体带头人。

消化内科副主任,主任医师,博士生导师,二级教授
中华医学会消化病学分会消化道肿瘤协作组 组长
中华医学会消化病学分会胃肠微生态学组 委员
上海市医学会消化病学分会 副主任委员
中国医疗保健国际交流促进会消化病学分会 副主任委员
中国女医师协会消化病学专委会 副主任委员

消化内科,住院医师
版权说明:本文来源于中国医学论坛报“罕见病临床思辨”专栏,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。
查看更多