查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





▼点击下图,查看更多ISC 2026重磅研究!
作者:复旦大学附属华山医院神经内科血管组 范文锦 应云清

2026年2月4日至2月6日,2026年国际卒中大会(ISC 2026)于美国新奥尔良召开。来自新加坡国立大学的记忆、衰老与认知中心的Christopher Chen教授汇报了评估MLC1501在伴有运动功能障碍的卒中后受试者中有效性的研究的最新结果。

MLC601(NeuroAiD)与MLC901(NeuroAiD Ⅱ)是一类由多种植物成分组成的复方制剂,既往临床前研究显示其具有神经保护、抗炎及神经修复的多重作用[1]。临床试验及相关系统综述进一步证实,二者有助于改善缺血性卒中患者的功能结局与促进神经恢复,目前已在全球多个国家被用于卒中及创伤性脑损伤后的神经功能修复。
在此基础上,为优化长期治疗的可行性并提升临床转化潜力,研究者开发了第三代制剂MLC1501。该制剂在保留关键药理作用的前提下,将配方简化为黄芪、当归、川芎和远志四味中药,旨在:① 保持与母体化合物相当的关键药理特性;② 通过减少服药负担提升患者依从性;③ 优化生产工艺以促进市场可及性;④ 并支持更长期的治疗方案,从而为未来纳入临床指南与医疗保障体系创造条件。
基于对卒中恢复试验的最新见解,以及早期从MLC601的CHIMES[2]、CHIMES-E[3]研究和MLC901研究中所积累的关于基线卒中严重程度和治疗时间窗作用的认识[4,5],MAESTOSO研究(MLC1501 study Assessing Efficacy in post-STrOke Subjects with mOtor deficits)聚焦于卒中急性期后仍遗留具有临床意义运动功能障碍的缺血性卒中患者,旨在评估MLC1501在促进运动功能恢复方面的疗效与安全性。在ISC 2026大会上,来自新加坡国立大学的记忆、衰老与认知中心的Christopher Chen教授汇报了评估MLC1501在伴有运动功能障碍的卒中后受试者中有效性的研究的最新结果。

本研究为Ⅱ期、多中心、随机、双盲、安慰剂对照研究,旨在评估MLC1501在卒中急性期后促进运动功能恢复的有效性与安全性。计划纳入300名符合条件的缺血性卒中患者。
受试者按1:1:1的比例随机分配至三个治疗组:安慰剂组、MLC1501低剂量组、MLC1501高剂量组。治疗周期为24周(6个月),每日2次,每次4粒,口服或管饲给药。
疗效评估分别在第4周(电话随访)、第12周、第24周或研究结束时(以较早者为准)进行。所有受试者均接受标准的卒中二级预防治疗以及康复治疗。
男性或女性
年龄≥18岁,或符合所在国家要求的法定成年年龄
在入组前2~10 d内确诊为急性缺血性卒中(AIS),且具有相符的脑影像学检查结果
美国国立卫生研究院卒中量表(NIHSS)8~18分,NIHSS运动项目5A、5B、6A和/或6B合计得分≥3分
经医师判断适合进行积极康复治疗的患者
书面知情同意
改良Rankin量表(mRS)>1分。
对任何研究程序有禁忌证。
在静脉溶栓或血管内溶栓/取栓术后24 h内出现状况不稳定。
过去30 d内服用过任何草药或传统药物。
过去30 d内参加过其他临床药物研究或器械试验。
妊娠期或希望在研究期间继续哺乳的女性。育龄期女性如果同意严格禁欲或使用有效的避孕措施(全身作用的激素类避孕药除外),则可以入选。绝经/绝经后或已行手术绝育的女性在研究期间也不允许使用激素替代疗法。
对黄芪、川芎、远志、当归或豆科植物(如豆类、豌豆、蚕豆)、远志科植物(如远志、蛇根草)、伞形科植物(如大茴香、葛缕子、胡萝卜、芹菜、莳萝、欧芹、防风草)或皂树皮过敏。
有证据显示存在其他可能影响长期功能或导致残疾的显著脑缺血性病变。
有证据显示患有会影响研究评估和随访的晚期或严重疾病,例如癌症、肾衰竭、肝硬化、痴呆或精神疾病。
根据研究者的判断,存在:① 任何其他可能因参与本研究而危及患者安全;② 妨碍其完成研究规定程序的能力;③ 影响研究评估和随访;④ 影响研究结果有效性的医学、精神或认知状况。
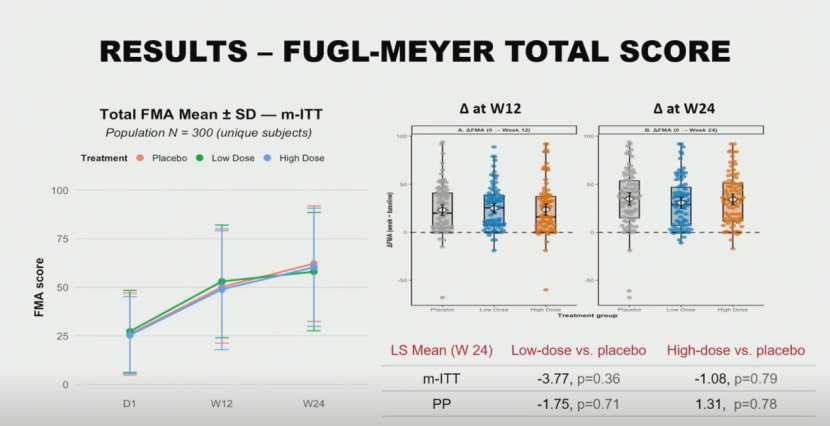
24周时Fugl-Meyer运动功能量表(FMA)评分较基线的变化。
12周时FMA总分较基线的平均变化。
12周和24周时FMA上肢和下肢评分较基线的平均变化。
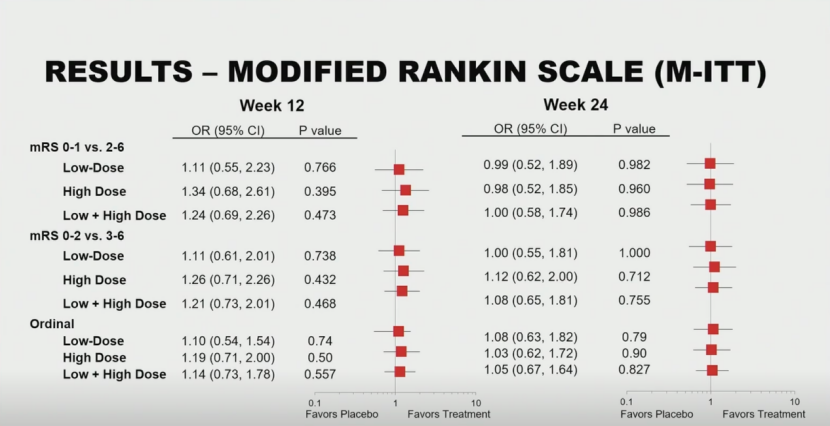
4周、12周和24周时mRS评分(0~1分 对 2~6分)的患者比例。
4周、12周和24周时患者报告结果测量信息系统-总体健康简表(PROMIS-10)评分较基线的平均变化。
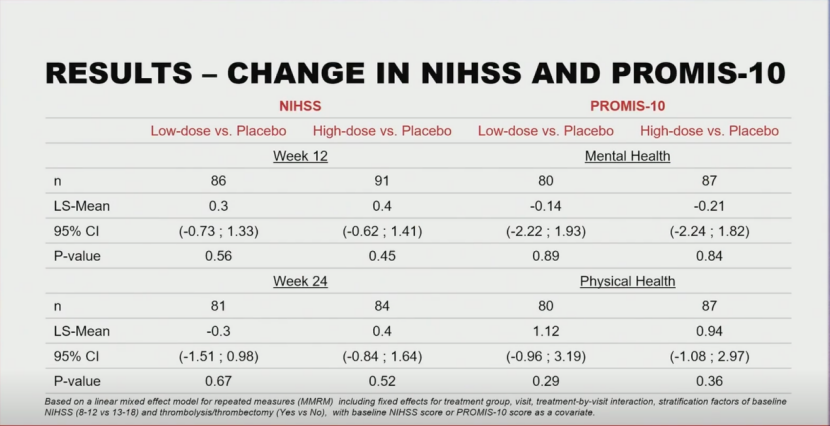
12周和24周时NIHSS评分较基线的平均变化。


各组受试者基线特征均衡可比:年龄或性别无显著差异,约15%的患者接受了血管再通治疗,平均NIHSS评分为11分,平均FMA评分为26分。
在安全性方面,不良事件(AE)、严重不良事件(SAE)及死亡人数在各组间无差异。
主要结局的统计结果为阴性,无论是高剂量组还是低剂量组,在Fugl-Meyer评分上与安慰剂组相比均无差异。
mITT分析集的统计结果相同,干预24周后,低剂量组与安慰剂组均数差为-3.77(P=0.36),高剂量组与安慰剂组的差异为-1.08(P=0.79),药物干预未能带来额外的运动功能获益。
24周时各组间实现功能独立(mRS 0~2分)的比例相当(低剂量组比值比1.00,P=1.000;高剂量组比值比1.12,P=0.712),mRS位移分析亦证实无显著差异。
NIHSS评分和PROMIS-10评分均未展现出统计学意义上的改善。
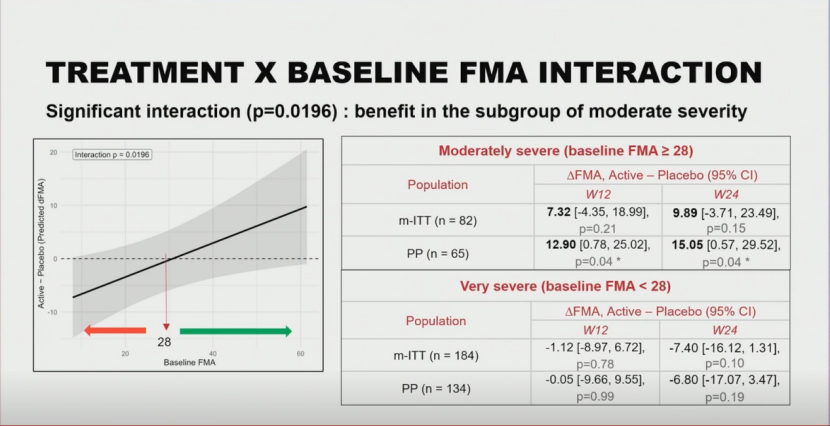
值得注意的是,研究团队进行了一项预设的交互作用分析。结果证实,基线病情严重程度显著影响了药物疗效:极重的运动功能障碍患者可能存在严重的皮质脊髓束中断,预后较差;而基线FMA≥28分的中重度患者则显示出获益信号。
特别是在依从性良好的PP人群中:治疗12周时,药物组与安慰剂组相比,FMA评分改善值的组间差异为12.90分[95%置信区间(CI)0.78~25.02, P=0.04];治疗24周时,组间差异进一步扩大至15.05分(95% CI 0.57~29.52, P=0.04)。
四、研究结论

MAESTOSO研究证实了MLC1501在缺血性卒中患者长达24周治疗中的安全性,但主要终点无显著差异,次要终点(mRS、NIHSS、PROMIS-10)的结果同样无显著差异,可能是由于配方的简化导致了一些有助于运动恢复的成分丢失。
基于此,未来Ⅲ期临床试验是否开展需要更慎重的考量。此外,治疗与基线病情严重程度之间存在交互作用。预设的亚组分析提示基线病情严重程度显著影响药物疗效,中度运动功能障碍患者(基线FMA≥28分)可能是该药物的潜在获益人群,这启发我们在未来卒中恢复试验中究竟应该纳入哪些患者,仍需仔细思考。
[1] Heurteaux C, Gandin C, Borsotto M, et al. Neuroprotective and neuroproliferative activities of NeuroAid (MLC601, MLC901), a chinese medicine, in vitro and in vivo[J]. Neuropharmacology, 2010, 58(7): 987-1001.
[2] Chen C L H, Young S H Y, Gan H H, et al. Chinese medicine neuroaid efficacy on stroke recovery: a double-blind, placebo-controlled, randomized study[J]. Stroke, 2013, 44(8): 2093-2100.
[3] Venketasubramanian N, Young S H, Tay S S, et al. CHInese medicine NeuroAiD efficacy on stroke recovery - extension study (CHIMES-E): a multicenter study of long-term efficacy[J]. Cerebrovascular Diseases (Basel, Switzerland), 2015, 39(5-6): 309-318.
[4] Chen C P L H, Esagunde R U, Escabillas C G, et al. Phase II randomised, double-blind, placebo-controlled trial to assess the efficacy and safety of MLC1501 in patients with stroke: the MLC1501 study assessing efficacy in post-STrOke subjects with mOtor deficits (MAESTOSO) study protocol[J]. Stroke and Vascular Neurology, 2025, 10(5): 657-664.
[5] Navarro J C, Chen C L, Lee C F, et al. Durability of the beneficial effect of MLC601 (NeuroAiDTM) on functional recovery among stroke patients from the Philippines in the CHIMES and CHIMES-E studies[J]. International Journal of Stroke: Official Journal of the International Stroke Society, 2017, 12(3): 285-291.
查看更多