查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





▼点击下图,查看更多ISC 2026重磅研究!
作者:复旦大学附属华山医院神经内科血管组 乐诗嘉 苏娅
2026年2月4日至2月6日,2026年国际卒中大会(ISC 2026)于美国新奥尔良召开。来自加拿大曼尼托巴大学的Jai Shankar教授发布了EMMA-Can研究的初步结果。该研究采用独特的三臂设计,通过对比前瞻性注册登记研究与随机对照试验(RCT),首次全面评估了脑膜中动脉栓塞术(EMMA)在真实世界临床实践中治疗慢性硬膜下血肿(CSDH)的有效性与安全性。
CSDH是神经外科最常见的疾病之一,传统治疗手段为外科钻孔引流术(SD)。然而,即使接受标准外科治疗,仍有高达1/3的患者出现血肿复发[1],给患者带来沉重负担。
近年来, EMMA作为一种微创辅助治疗方法逐渐兴起。该技术通过栓塞脑膜中动脉(MMA),阻断血肿外膜的新生血管供应,从而打断维持血肿形成的炎症性新血管循环[2]。多项RCT已经证实[3-5],在严格筛选的患者群体中,EMMA能有效降低CSDH复发率及严重不良事件发生率。
然而,临床实践中的患者往往具有更复杂的临床特征,可能不完全符合RCT的严格纳入标准,例如双侧血肿、未行外科引流、基线功能状态较差或伴有局灶性神经功能缺损等。因此,EMMA在真实世界临床实践中的有效性与安全性须进一步验证,EMMA-Can研究正是为填补这一循证医学空白而设计。
EMMA-Can研究采用创新的三臂设计,包括两个RCT臂(外科引流±EMMA)和一个前瞻性注册登记研究臂。这一设计的独特之处在于,前瞻性研究臂与RCT同步进行,采用完全相同的标准化手术方案、影像学评估和随访流程,从而确保数据的高度可比性。


改良Rankin量表(mRS)≤2分
单侧、有症状的原发性或复发性CSDH,头颅计算机体层摄影(CT)显示血肿厚度>10 mm
近2年内行头颈部CT血管造影(CTA)检查,证实EMMA血管入路可行
纳入在日常临床实践中接受EMMA治疗的CSDH患者,包括:① 不符合RCT纳入标准的患者;② 双侧CSDH患者;③ 未行外科引流的患者;④ 存在外科引流禁忌证的患者;⑤ 基线mRS评分较差的患者;⑥ 无局灶性神经功能缺损的患者。
无法从患者或其替代决策者处获得知情同意
双侧有症状的CSDH患者
CTA显示MMA分支与颈内动脉(ICA)分支之间存在持续交通
存在栓塞术禁忌证,如严重肾功能不全[肾小球滤过率(eGFR)<30 ml/(min·1.73m2)]或妊娠
预期寿命<6个月
已知对栓塞剂过敏
急性硬膜下血肿,CT扫描显示均匀高密度影
继发性CSDH,可能由潜在疾病引起,如血管病变、脑肿瘤、蛛网膜囊肿、自发性颅内低压或既往开颅手术史

主要有效性终点:入组后90 d内的影像学CSDH复发(由盲法独立神经放射科医师根据随访CT扫描进行判定)。

主要安全性终点:全因死亡率及严重不良事件。
研究于2021年5月至2025年9月期间完成患者入组,共纳入RCT患者192例,前瞻性注册登记研究患者110例。经排除后,RCT每臂各纳入93例可评估患者,注册登记研究纳入95例可评估患者。
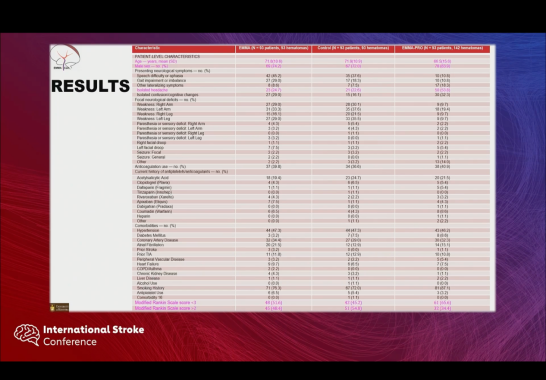
三组患者的基线特征总体均衡可比。EMMA组、对照组和EMMA-PRO组的平均年龄分别为71.8岁、71.9岁和66.5岁,男性比例分别为74.2%、72.0%和83.9%。
在血肿特征方面,EMMA组和对照组患者的平均血肿体积分别为132.2 ml和131.4 ml,平均血肿厚度分别为22.6 mm和23.9 mm,两组基线血肿负担相当。相比之下,EMMA-PRO组的平均血肿体积为89.5 ml,平均血肿厚度为17.4 mm,血肿负担相对较轻。
从占位效应来看,EMMA组和对照组中存在中线移位的患者比例分别为98.9%和97.8%,而EMMA-PRO组为81.7%。

(1)单侧血肿患者:EMMA显著降低复发风险
在90 d随访期内,EMMA组患者血肿复发率仅为14.0%,而对照组的复发率高达49.5%,两组差异具有高度统计学意义[比值比0.17,95%置信区间(CI)0.08~0.33,P<0.001]。
更令人振奋的是,前瞻性注册登记研究组的真实世界数据验证了这一疗效。尽管EMMA-PRO组纳入的单侧血肿患者(n=44)可能不完全符合RCT的入排标准,但其血肿复发率同样保持在较低水平(15.9%),与对照组(49.5%)相比具有显著差异(比值比0.19,95% CI 0.07~0.45,P<0.001),复发风险降低幅度与EMMA组相当。
(2)双侧血肿患者分析
EMMA-PRO组包含49例双侧CSDH患者,从血肿水平分析来看,共有98个血肿接受治疗,其复发率为16.3%,显著低于对照组的单侧血肿复发率49.5%(比值比0.15,95% CI 0.05~0.42,P<0.001),提示EMMA对双侧血肿同样有效。
从患者水平分析,双侧CSDH患者中任一侧血肿复发的比例为26.5%,仍显著低于对照组的49.5%(比值比0.37,95% CI 0.17~0.77,P=0.009)。这表明即使对于双侧血肿这一高危人群,EMMA治疗仍能使复发风险有效降低。

在安全性方面,三组间的严重不良事件发生率与全因死亡率均无统计学差异,显示EMMA在真实世界应用中具有良好的安全性。所有严重不良事件及死亡病例经中心化判定后,均未归因于EMMA操作本身。

四、研究结论与意义
EMMA-Can研究通过独特的三臂设计,首次系统性验证了EMMA在真实世界复杂患者群体中的疗效与安全性。
研究结果表明,EMMA作为外科引流的辅助治疗,不仅在RCT严格筛选的单侧CSDH患者中显著降低复发风险,在更复杂的患者群体中同样有效——包括双侧血肿患者、未行外科引流者、基线mRS评分较差者等RCT通常排除的人群,其复发率降低幅度与RCT干预组相当。这一发现为EMMA在真实世界的广泛应用提供了高级别循证医学证据,拓展了其适应证范围,为临床医生提供了更灵活的治疗选择。
[1] DUCRUET A F, GROBELNY B T, ZACHARIA B E, et al. The surgical management of chronic subdural hematoma [J]. Neurosurgical review, 2012, 35(2): 155-69.
[2] LINK T W, RAPOPORT B I, PAINE S M, et al. Middle meningeal artery embolization for chronic subdural hematoma: Endovascular technique and radiographic findings [J]. Interv Neuroradiol, 2018, 24(4): 455-62.
[3] DAVIES J M, KNOPMAN J, MOKIN M, et al. Adjunctive Middle Meningeal Artery Embolization for Subdural Hematoma [J]. N Engl J Med, 2024, 391(20): 1890-900.
[4] LIU J, NI W, ZUO Q, et al. Middle Meningeal Artery Embolization for Nonacute Subdural Hematoma [J]. N Engl J Med, 2024, 391(20): 1901-12.
[5] FIORELLA D, MONTEITH S J, HANEL R, et al. Embolization of the Middle Meningeal Artery for Chronic Subdural Hematoma [J]. N Engl J Med, 2025, 392(9): 855-64.
查看更多