查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过






岁聿云暮,华章将启。当2025年的时间卷轴缓缓收束,消化内镜及消化系疾病领域在临床研究与实践探索中留下了诸多坚实足迹,新技术的涌现、新理念的更迭以及循证医学证据的不断累积,正在深刻重塑着我们对疾病的认知与临床实践决策。
为了帮助广大临床医生系统梳理学科脉络,准确把握前沿进展,《中国医学论坛报》年度盘点栏目特别邀请了消化领域各亚专业的领军专家,对2025年度的临床研究进展进行深度回顾与总结。
胃肠动力障碍性疾病为临床常见病与多发病,涉及消化道平滑肌运动功能障碍、肠-脑互动异常等。临床包括以各种原因引起的动力障碍为主的疾病,如贲门失弛缓症(Achalasia,AC)、胃食管反流病(Gastroesophageal reflux disease, GERD)、胃轻瘫(Gastroparesis),以及可能涉及动力的疾病,如功能性消化不良(Functional,FD)、肠易激综合征(Irritable bowel syndrome,IBS)、功能性便秘(Functional constipation,FC)等肠-脑互动障碍。这一类的疾病给社会和个人都带来沉重的经济和医疗负担;同时针对其诊断及治疗,医学界也在竭力开发解决方案。
《中国医学论坛报》特邀中山大学附属第一医院肖英莲教授团队对2025年胃肠道动力相关疾病的重要临床进展进行盘点,从而为临床医生们开展临床实践操作提供指导。
肖英莲 教授

中山大学附属第一医院
主任医师 博士生导师
中山大学附属第一医院内科副主任,消化科副主任
中山大学附属第一医院南沙院区副院长
中华医学会消化病学分会委员
中华医学会消化病学分会胃肠动力学组组长
中国研究型医院协会神经胃肠动力专委会副主任委员
白求恩基金会消化专委会常委
亚洲神经胃肠动力学会常任理事
中国医药卫生基金会消化专委会常委

中山大学附属第一医院消化内科医师,助理研究员,博士后
第一作者身份在AJG、JTRM等杂志发表SCI论文8篇
过去一年,GERD 领域的前沿研究仍聚焦于 “精准诊断” 与 “疗效优化” 两个方面。在这一核心框架下,GERD 临床研究版图仍在持续拓展,涌现出较多新兴的探索方向,包括以喉咽症状为主诉的 GERD诊治策略、新兴 GERD 亚型的特征描述与管理策略探索。
对于以喉咽症状为主诉的 GERD诊治策略,既往存在定义模糊、喉咽症状与喉咽反流概念混淆、喉咽反流病诊断标准缺乏统一规范等问题,这直接导致了抑酸药物过度使用,且患者的临床获益有限。2025 年发布的《圣地亚哥共识 —— 喉咽反流症状和喉咽反流病》[1],由消化内科、耳鼻喉科、发音语言学等多领域的28名国际专家组成跨学科工作组联合制定,旨在规范喉咽症状(LPS)与喉咽反流病(LPRD) 的定义、诊断及管理流程。
该共识明确区分 “症状” 与 “疾病” 的定义:① LPS 特指咳嗽、声音嘶哑或音质改变、频繁清嗓、咽喉黏液过多(俗称 “痰多”)、咽喉疼痛或不适等系列症状,而癔球症、鼻后滴漏、口臭、嗳气等则未被纳入 LPS 范畴;② LPRD 的诊断需同时满足 “长期存在困扰性 LPS” 及 “存在客观反流证据” 两项核心条件。
诊断方面,该共识强调动态反流监测是 LPRD 诊断的关键参考依据及首选工具。对于 pH 阻抗监测结果,食管酸暴露时间(AET)>6% 可作为 GERD/LPRD 的确诊证据。喉镜与上消化道内镜检查对明确器质性病变具有重要临床价值,但需要注意喉镜检查可能导致反流相关过度诊断,而上消化道内镜检查则存在遗漏反流诊断的风险。
治疗层面,该共识提出应基于患者症状谱制定个体化管理方案,根据是否合并食管症状(烧心、反流、胸痛)采取不同的治疗路径(图 1)。同时,共识推荐以客观检查证据为导向实施精准治疗,以减少抑酸药物的过度使用。此外,共识强调病理生理学机制导向治疗的重要性,提出喉高反应性与过度警觉可能是 LPS 形成的关键病理生理机制,并推荐喉部再校准疗法(LRT)、神经调节剂和(或)认知行为疗法等靶向干预措施。关于抗反流手术在以喉咽症状为主诉 GERD 患者中的应用价值,目前仍存争议,但今年发表的一项系统综述与荟萃分析结果显示,腹腔镜下抗反流手术可显著缓解 GERD 相关咳嗽症状[2]。
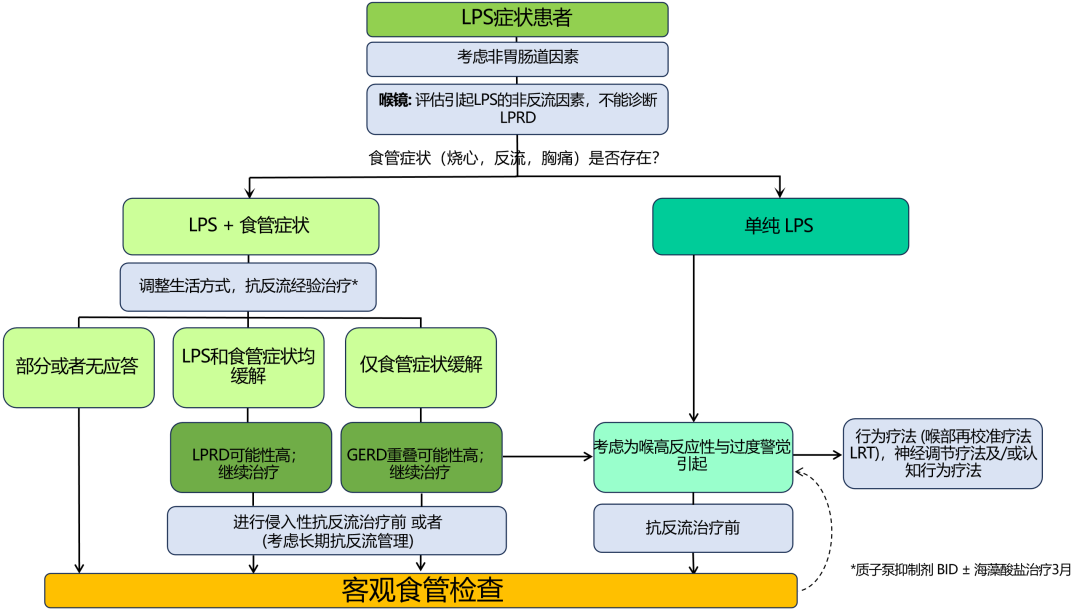
图1 喉咽症状患者诊治流程(圣地亚哥共识)
综上,以喉咽症状为主诉的 GERD 近年受到学界广泛关注,其诊治流程的规范化及治疗方案的循证医学证据正逐步完善。
此外,一些新兴的GERD亚型在2025年也备受关注。胰高糖素样肽-1受体激动剂(GLP-1 RAs) 是目前治疗 2 型糖尿病和肥胖的热门药物,其延迟胃排空的作用可能增加GERD的发病风险。一项随访时长3年的糖尿病人群队列研究显示,相比使用SGLT-2抑制剂的患者,使用GLP-1 RAs的患者发生 GERD 风险升高 27%,GERD相关并发症风险升高 55%,这提示临床医生需警惕GLP-1 RAs 相关 GERD 风险,及时制定防治策略[3]。2025年,《美国胃肠内镜学会胃食管反流病诊断与管理指南》更新,除了规范内镜下抗反流手术的指征,还特别提到袖状胃切除术后新发GERD患者的处理[4]。该指南提出,未来还需明确非典型症状为主诉的GERD、内镜下肌切开术后GERD的管理策略[4]。这说明新兴GERD的亚型可能是该领域未来的研究热点。
贲门失弛缓症(Achalasia, AC)等食管梗阻性动力障碍性疾病的诊断,需依赖多种客观检查手段的综合评估。目前临床常用检查包括高分辨率食管测压(High-resolution manometry, HRM)、上消化道内镜及钡剂造影等,其中 HRM 作为诊断金标准,可精准评估食管动力模式,但在部分临床场景下仍存在诊断局限性。
功能性管腔成像探针(Functional Luminal Imaging Probe, FLIP)成像技术是近年在国际上广泛应用的新型检查手段。该技术能够实时评估食管管腔横截面积、食管扩张性(即横截面积与扩张压力的相关性)及食管体部收缩模式,并生成直观的 3D 地形图,尤其适用于 HRM 结果不确定、测压表现与临床症状不符的患者。此外,FLIP 可特异性评估食管对扩张刺激的继发性蠕动反应,这一功能是 HRM、内镜等传统检查无法替代的。
为规范 FLIP 成像在食管动力障碍性疾病中的应用,2025 年《食管动力障碍性疾病的 FLIP 成像标准化操作与结果判读:达拉斯共识》正式发布,明确了该技术的操作流程、参数设置及数据解读标准[5]。FLIP 可在镇静内镜检查同期完成,同步评估食管胃交界处(Esophagogastric junction, EGJ)开放特性及食管体部对扩张刺激的收缩反应,成为 HRM 技术的重要补充手段。同年,《美国胃肠病学会(AGA)临床实践更新:将FLIP融入临床实践》,进一步提议将该技术纳入食管动力障碍性疾病的常规诊疗体系[6]。
基于 FLIP 的技术优势,专家在功能性吞咽困难患者中发现了一种新型致病机制:部分患者 HRM 检查表现正常,但 FLIP 成像提示气囊扩张状态下 EGJ 开放受限,据此提出 “扩张介导性梗阻(Distention-Mediated Obstruction, DMO)” 这一病理生理新类型[7]。研究者推测,DMO 可能由两种不同的病理生理学机制引起,第一是由 GERD 引起的食管感觉异常,第二是存在潜在的 EGJ 流出道梗阻,这一发现为功能性吞咽困难的精准诊治提供了新思路[7]。
综上,FLIP 成像技术在传统检查诊断困境中展现出独特价值,在食管动力障碍性疾病的诊断中发挥着日益重要的作用。
治疗方面,经口内镜下肌切开术(Peroral Endoscopic Myotomy, POEM)已成为 AC 等食管梗阻性动力障碍性疾病的一线治疗方案,但其长期疗效及安全性尚不明确。2025 年发表的一项为期 5 年的长期随访研究,比较了POEM与腹腔镜下肌切开术(Laparoscopic Heller Myotomy, LHM)联合 Dor 胃底折叠术术式在 AC 的疗效及安全性,结果显示,二者临床疗效相当,但POEM术后的反流风险相对升高[8]。另有一项回顾性研究指出,实施POEM的同时进行内镜下抗反流手术,相比单纯POEM,可更好地预防GERD的发生而不影响吞咽困难的缓解[9]。综上,POEM 作为微创治疗方式具有可靠的长期有效性,但临床实践中需加强POEM术后反流监测与针对性干预。
此外,AC 患者肌切开术后可能出现食管远端节段局灶性扩张,即 “肌切开术后食管扩张(Blown-out Myotomy, BOM)”,该并发症虽不常见,但仍是导致手术失败的重要原因之一,目前其临床管理策略尚未明确。我国学者开展的一项回顾性研究,通过对比 BOM 与非 BOM 患者的 POEM 治疗效果,发现 BOM 患者接受 POEM 治疗后仍可获得显著的症状缓解,提示补救性 POEM 可作为 BOM 的有效治疗手段,为该并发症的临床处理提供了循证医学依据[10]。
FD 是一种以餐后饱胀感、早饱感、上腹痛、上腹部烧灼感为核心症状的脑 - 肠互动异常性疾病,罗马Ⅳ标准目前将其分为餐后不适综合征(Postprandial Distress Syndrome, PDS)与上腹痛综合征(Epigastric Pain Syndrome, EPS)两个亚型,临床治疗多基于亚型分类采用促动力、抑酸等对症干预。
然而,2025 年发表的一项国际多中心大队列研究对这一分类体系提出了挑战:该研究显示,按罗马Ⅳ标准归类的 EPS 患者中,近 40% 存在 “餐后上腹痛(pEPS)” 症状,而 50% 的 PDS 患者也报告了这一表现,提示传统亚型分类无法完全涵盖部分患者的症状特征。基于此,研究提出 “餐后上腹痛综合征” 这一 FD 新亚型的构想,但其潜在病理生理学机制(如胃肠动力异常、内脏高敏感性、脑 - 肠轴调控紊乱等)及对不同治疗方案的反应性仍需进一步验证,这也预示着 FD 分类体系可能面临更新与完善[11]。
饮食干预新证据
饮食干预作为脑 - 肠互动异常疾病的重要治疗手段,其在 FD 中的疗效与应用价值一直备受关注。2025 年一项高质量随机对照试验(RCT)为 FD 的饮食治疗提供了关键循证支持:该研究显示,低 FODMAP 饮食可使 73% 的 FD 患者餐后不适症状得到显著缓解;进一步通过盲法食物激发试验结果提示,甘露醇是最常见的症状触发物(发生率 23%),且不同患者的饮食触发因素存在显著个体差异,证实了 FD 饮食管理的高度个体化特征[12]。这一结果提示,基于患者个体耐受情况制定的低 FODMAP 饮食方案,可作为 FD 个体化治疗策略的重要组成部分。
胃轻瘫是一类以胃排空延缓为核心病理生理特征的临床综合征,主要表现为早饱、餐后上腹饱胀、恶心、发作性干呕、呕吐及体重减轻等,严重影响患者生活质量。
2025 年,《美国胃肠病学会胃轻瘫管理临床实践指南》发布:
在诊断方面,指南明确建议对疑似胃轻瘫患者,采用 4 小时胃排空测试作为确诊的核心手段,相较于传统 2 小时测试,其诊断敏感性与特异性更高;
在药物治疗方面,指南有条件地推荐使用甲氧氯普胺、红霉素等促动力药物,强调需严格把控适应证与用药剂量,同时密切监测药物不良反应;在侵入性治疗方面,指南仅建议对药物治疗反应不佳的特定患者实施胃经口内镜肌切开术(G-POEM),并指出该术式作为新兴治疗手段,其临床疗效仍存在异质性,需要个体化评估[13]。
针对 G-POEM 术后疗效不稳定的临床痛点,有学者提出基于 “术后胃排空测试结果 + 临床症状缓解情况” 的难治性胃轻瘫患者分类体系,共分为 4 种临床表型:① 症状缓解且胃排空率改善;② 症状缓解但胃排空率无改善;③ 症状无缓解但胃排空率改善;④ 症状无缓解且胃排空率无改善。
研究显示,对于第①类患者,针对幽门的再治疗(如再次 G-POEM、胃电刺激)可有效解决症状复发问题;而对于第③、④类患者,再次实施 G-POEM 的疗效有限,且需重点关注此类患者大麻类药物的使用情况(可能影响症状评估与治疗反应)。该分类体系为 G-POEM 治疗失败患者的后续管理提供了精准指导,有助于优化临床决策、减少无效干预[14]。
嗳气症相关的定义、诊断标准及管理策略尚未形成统一共识。2025 年发布的《胃内、胃上嗳气、吞气和反刍综合征的诊断和管理综述》,系统规范了此类疾病的定义、分类、病理生理机制、诊断及治疗原则。
定义方面:① 胃内嗳气(GB)为胃内气体经食管下括约肌一过性松弛排出,属生理现象;② 胃上嗳气(SGB)是主动吞入空气后迅速排出的获得性行为驱动性障碍,为病理性嗳气主要类型;③ 吞气症指过量吞气入胃肠道,引发腹胀、腹痛及继发性嗳气;④ 反刍综合征是进食后无恶心、无明显用力的胃内容物反入口腔,与餐后腹壁及膈肌条件反射性收缩致腹内压升高相关。其中 SGB、吞气症及反刍综合征均属脑-肠-行为互动障碍,与焦虑、注意力聚焦、条件反射及喉-食管高警觉状态密切相关,非结构性或单纯反流性疾病。
诊断方面,该综述强调,24小时pH-阻抗监测是区分嗳气、吞气和反刍综合征的关键工具,必要时可联合高分辨率食管测压或餐后监测。单纯症状描述或问卷不足以明确疾病类型。
治疗方面,该综述指出,经验性长期抑酸治疗不应作为一线策略,强调行为治疗是核心干预手段,包括言语治疗、生物反馈、呼吸训练及认知行为治疗;药物治疗(如中枢神经调节药物)仅作为辅助[15]。
饮食干预是 IBS 综合治疗的重要手段之一。2025 年一项大型系统综述与网状荟萃分析对比了 11 种饮食疗法的疗效,结果显示:与常规饮食相比,低淀粉低糖饮食对 IBS 整体症状的改善效果排名第一,低 FODMAP 饮食排名第四。尽管低 FODMAP 饮食的相关循证证据最为充分,但低淀粉低糖饮食等新兴方案已显现潜力,值得进一步探索[16]。
另有一项针对 “自认为麸质敏感” IBS 患者的随机交叉试验发现,患者对小麦、麸质及安慰剂的症状反应无显著差异,提示心理预期在症状产生中具有重要作用,仅部分患者可能从饮食限制中真正获益,因此精准筛选须饮食干预的患者至关重要[17]。
基于血清免疫球蛋白 G(IgG)抗体检测结果的个性化排除饮食,为 IBS 饮食治疗提供了新方向。基于食物抗原特异性 IgG 检测结果,一项随机双盲对照试验发现IgG指导下的排除饮食相比假对照组可显著缓解患者腹痛的症状;便秘型 IBS 与混合型 IBS 患者的获益更为显著。该研究证实,IgG 指导的个性化排除饮食疗效优于假对照组,为 IBS 个体化饮食治疗提供了循证依据,但其长期有效性仍需更大规模研究验证[18]。
作为肠 - 脑互作异常疾病,IBS 的脑肠行为疗法应用日益广泛。一项纳入 67 项随机对照试验(RCT)的荟萃分析显示,与等候名单对照组相比,简易接触式认知行为疗法、电话通信自我疾病管理、动态心理治疗等 7 类疗法均能显著改善 IBS 症状;这些疗法对难治性 IBS 患者同样有效。然而,由于纳入研究多为低质量证据,上述结论的可靠性有限,亟需高质量 RCT 进一步验证[19]。
神经调节剂亦是 IBS 的重要治疗选择。一项纳入 28 项 RCT 的荟萃分析显示,三环类抗抑郁药(TCA)缓解 IBS 总体症状的疗效最佳,选择性 5 - 羟色胺再摄取抑制剂(SSRI)次之[20]。2025年,ATLANTIS 试验的一项事后分析进一步探索了低剂量阿米替林(TCA 类代表药物)治疗IBS的疗效预测因子:≥50 岁患者的总体疗效更优;社会经济状况较差群体的腹痛改善更为显著;男性、心理问卷评分较高者及腹泻型 IBS 患者对治疗的反应更佳,为临床精准选用阿米替林提供了参考。
普卡利肽是一种新型的鸟苷酸环化酶C受体激动剂,国外研究已证实普卡利肽有助于治疗功能性便秘(FC),但其疗效在中国人群中尚不明确。2025年一项中国多中心随机双盲安慰剂对照的Ⅲ期试验显示,普卡利肽治疗后FC患者的自发排便率显著提升,且耐受性良好。这为我国FC治疗提供了新选择。[21]
胃肠动力障碍性疾病是临床最常见的消化系统疾病类别之一,目前仍面临发病机制尚未完全阐明、诊断缺乏统一标准、治疗效果欠佳等困境。未来研究需要进一步聚焦疾病病理生理机制的深度解析,挖掘新型治疗靶点,并探索个体化精准治疗方案,以期推动胃肠动力相关疾病的临床诊疗水平持续提升。

(本文版权属于中国医学论坛报社,转载须授权)
查看更多