查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





对于HR+/HER2-晚期乳腺癌,国内外权威乳腺癌指南均推荐CDK4/6i联合内分泌治疗为一线标准治疗方案,但是对于CDK4/6i治疗进展后并无标准治疗。新型抗体药物偶联物(ADC)如德曲妥珠单抗(又称T-DXd或DS-8201)和针对滋养层细胞表面抗原2(TROP2)的戈沙妥珠单抗(SG)在HR+/HER2-(含低表达人群)晚期乳腺癌中均取得了突破性进展,为CDK4/6i耐药之后治疗策略提供了新方向。
ADC是一类抗体、连接头和细胞毒性药物组成的靶向生物药剂,以单抗为载体将小分子细胞毒性药物为靶向方式高效地运输至目标肿瘤细胞内发挥抗肿瘤的作用。ADC类药物包含三种组分(如图1):(1)高效的小分子细胞毒性药物;(2)靶向抗原的高特异性和高亲和力的抗体;(3)高稳定的连接头。
图1. ADC药物的结构
对于ER+/HER2-mBC患者的治疗,《ESMO转移性乳腺癌指南》根据患者肿瘤进展状态和内分泌治疗的敏感性进行了推荐。对于一线CDK4/6i+内分泌治疗进展后存在内脏危象或既往内分泌治疗PFS期短的HER2低表达患者,推荐应用T-DXd进行治疗,HER2 0表达患者推荐应用SG进行治疗。
T-DXd是由曲妥珠单抗、拓扑异构酶Ⅰ抑制剂有效载荷及连接子组成,具有高药物抗体比、高活性载药和强效抗肿瘤旁观者效应等优势,DB-04(DESTINY-Breast04)研究将抗HER2靶向治疗获益人群从HER2阳性拓展至HER2低表达(IHC 1+或2+/ISH-),开启HER2低表达晚期乳腺癌ADC治疗新时代,DB-06(DESTINY-Breast06)研究更将T-DXd治疗时机前移。
DB-06是一项全球性、随机、开放标签的Ⅲ期临床试验,旨在评估T-DXd与研究者选择的化疗方案(TPC,卡培他滨、紫杉醇或白蛋白结合型紫杉醇)对HR+/HER2-low(IHC 1+或IHC 2+/ISH-)或HER2-ultralow(IHC >0且<1+)晚期乳腺癌患者的疗效和安全性。
研究纳入未曾接受过晚期阶段化疗,且在开始使用内分泌联合CDK4/6i一线治疗后6个月内病情进展,或在晚期阶段接受过至少两线内分泌治疗的患者(图2)。
研究主要终点是经盲态独立中心评审委员会(BICR)评估的HER2-low人群的PFS期。关键次要终点包括经BICR评估的意向治疗人群(ITT)的PFS期以及HER2-low和ITT人群的OS期。
图2. DB-06试验设计
各组疗效和安全性数据如下:HER2-low人群中,较TPC组,T-DXd显著改善患者的PFS期13.2 个月对8.1个月,HR=0.62,95%CI:0.51~0.74,P<0.001),疾病进展或死亡风险降低38%(HR=0.62,95%CI:0.51~0.74,P<0.001)。ITT人群,T-DXd组对TPC组(13.2个月对 8.1个月,HR=0.63,95%CI:0.53~0.75,P<0.001);HER2-ultralow人群:T-DXd组对TPC组(13.2个月对8.3个月,HR=0.78,95%CI:0.50~1.21)(图3)。
T-DXd和化疗组治疗12个月OS率分别为87.0%、81.1%,死亡风险下降19%;亚组分析提示,无论患者年龄、是否CDK4/6抑制剂经治、既往内分泌治疗线数、及肝脏转移情况,PFS期均一致获益(图3)。
T-DXd的安全性特征与既往研究一致,未发现新的安全性信号。
图3. DB-06试验PFS期结果
今年ESMO大会披露了DB-06研究中ITT人群及HER2-low人群的PRO数据,PRO评估结果显示在接受T-DXd治疗期间,患者的生活质量(QoL)得以维持;在ITT人群中,与化疗相比,接受T-DXd治疗患者疼痛的至恶化时间(TTD)显著延迟(22.0个月对6.3个月;HR=0.51,95%CI:0.39~0.65),在身体功能(HR=0.72)、角色功能(HR=0.75)、情感功能(HR=0.71)、疲劳(HR=0.76)方面,T-DXd组的TTD也优于化疗组。
综上所述,DB-06研究及PRO数据均证实T-DXd用于≥1线内分泌经治的HR+、HER2-low/-ultralow晚期乳腺癌患者的疗效和安全性,进一步支持T-DXd作为此类患者的新的治疗选择。
SG是一种滋养细胞表面抗原2(Trop-2)导向的抗体-药物偶联物,是首个靶向Trop-2治疗HR+/HER2-晚期乳腺癌的ADC。根据全球III期TROPiCS-02研究,SG已在美国和其他多个国家被批准用于治疗HR+/HER2-mBC后的内分泌治疗和至少两种额外的全身化疗。
TROPiCS-02(NCT03901339)是一项多中心、随机、对照、开放标签的III期临床试验,入组人群为既往接受CDK4/6i和内分泌治疗、且2到4线化疗的HR+HER2- mBC患者,旨在评估SG用于此类经治患者的疗效与安全性。主要终点是符合RECIST v1.1标准的PFS期,关键次要终点包括OS期和安全性。
图4. TROPiCS-02试验设计
结果显示与TPC组相比,mPFS期为5.5个月(95%CI:4.2~7.0)vs 4.0个月(95%CI:3.1~4.4),HR=0.65(95%CI:0.53~0.81),疾病进展或死亡风险降低34%(P=0.0001),6个月PFS率为46.1%比30.3%,9个月PFS率为32.5%比17.3%,12个月PFS率为21.3%比7.1%。
OS期获益方面,随着随访时间的延长(中位随访时间12.75个月),SG组相比TPC组持续改善OS期(中位OS期:14.5个月对11.2个月;HR=0.79;95%CI:0.65~0.95,P=0.01)。
图5. TROPiCS-02试验OS期及PFS期结果
近期,中国医学科学院肿瘤医院徐兵河院士团队在亚洲患者中开展的III期桥接研究EVER-132-002同样取得了阳性结果。在该研究中,患者随机分为SG组(n=166)和化疗组(n=165),结果显示SG与化疗相比,PFS期得到改善(HR=0.67,95%CI:0.52~0.87;P=0.0028;mPFS期:4.3个月对4.2个月)。SG与化疗相比,OS期也得到改善(HR=0.64,95%CI:0.47~0.88;P=0.0061;mOS期:21.0个月对15.3个月)。最常见的≥3级治疗相关不良事件是中性粒细胞减少症、白细胞减少症和贫血。
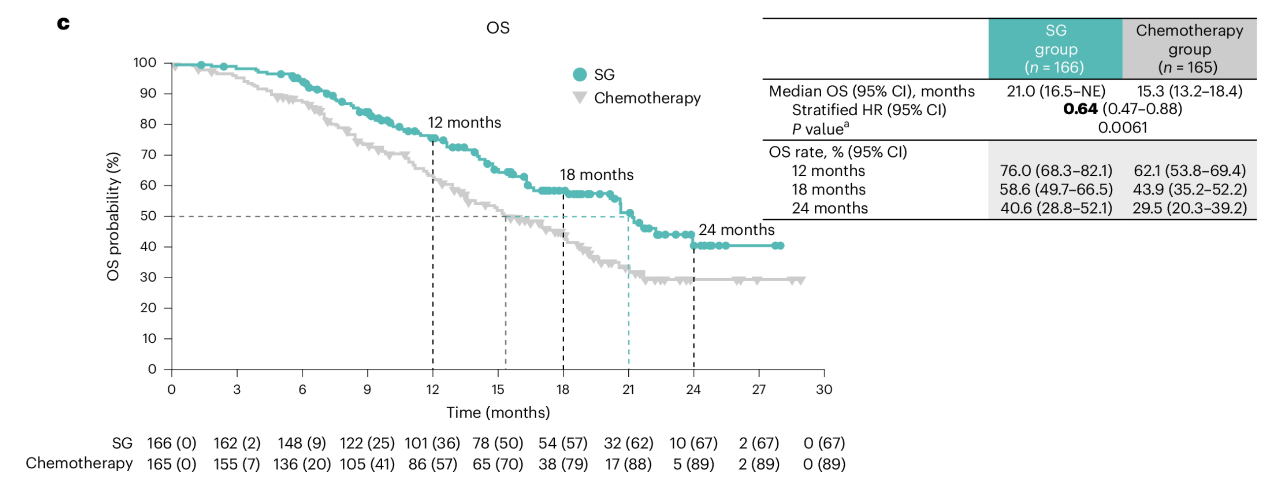
在EVER-132-002研究中,SG与化疗相比的疗效获益和可管理的安全性与全球TROPiCS-02研究的结果一致,并支持将SG作为亚洲内分泌抵抗,HR+/HER2-mBC经治患者的新治疗选择。
总之来讲,在临床中对于CDK4/6i联合内分泌一线治疗后快速进展以及两线内分泌耐药的HR+/HER2低表达乳腺癌患者,EMSO指南推荐使用T-DXd;而对于既往接受内分泌、CDK4/6i以及多线化疗的HR+/HER2阴性晚期乳腺癌患者则推荐使用SG。
目前,多项临床研究都对CDK4/6i耐药之后治疗策略提供了新方向,未来期待有更多循证医学证据的出现。目前,在缺乏直接临床证据的情况下,可以通过遵循行业内的指南和共识来指导临床实践,确保这些药物在患者中做好精准的排兵布阵。
上期链接:更换为化疗,CDK4/6i耐药后的治疗选择丨曼妙之声
上期文末互动答案:A


下列哪项研究为SG作为CDK4/6i耐药之后治疗策略提供亚洲人群证据?
A DB-04研究
B DB-06研究
C TROPiCS-02研究
D EVER-132-002研究




福利1:学习期间,我们将选取10个优质评论(50字以上且具有真情实感),入选者有机会获得价值100元的当当读书卡、伴手礼包(内含硬质帆布包、笔记本、水杯等)或64G的中国医学论坛报社Logo U盘。



福利2:累计3天签到打卡,可获得《中国医学论坛报》2024年半年数字报。
福利3:累计7天签到打卡,可获得《中国医学论坛报》2024年全年数字报。
查看更多