查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





今年的CSCO大会上,复宏汉霖以口头报告形式发布了创新抗PD-1单抗斯鲁利单抗在经治疗、不可切除或转移性高度微卫星不稳定或错配修复缺陷型(MSI-H/dMMR)实体瘤中开展的II期临床试验数据。目前斯鲁利单抗“泛癌种”治疗高度微卫星不稳定型(MSI-H)实体瘤适应症的上市注册申请于2021年4月获NMPA受理并被纳入优先审评审批程序,有望于2022年上半年获批上市。此外,斯鲁利单抗鳞状非小细胞肺癌适应症的上市注册申请也正在审评中。
围绕“Combo+Global”(联合治疗+国际化)差异化开发战略,斯鲁利单抗已获得中国、美国、欧盟等国家及地区的临床试验许可,目前共开展10项肿瘤免疫疗法临床试验,适应症广泛覆盖肺癌、肝细胞癌、食管癌、头颈癌和胃癌等高发大癌种,全球范围内累计入组约2300名受试者,也印证了国际市场对斯鲁利单抗质量的信心与认可。
以下为斯鲁利单抗针对MSI-H/dMMR实体瘤的数据发表详情:
论文题目:斯鲁利单抗(HLX10,创新型抗PD-1单抗)在经治疗、不可切除或转移性高度微卫星不稳定或错配修复缺陷(MSI-H/dMMR)实体瘤中开展的II期临床试验(ID:9951)
主要研究者:秦叔逵,中国人民解放军南京八一医院;李进,同济大学附属东方医院
展示形式:口头报告
主讲人:郭晔,同济大学附属东方医院
汇报时间:2021.09.26 17:15–17:23,分会场6,免疫治疗综合专场
试验设计
本研究是一项在标准治疗失败的、不可切除或转移性高度微卫星不稳定型或错配修复缺陷型实体瘤患者中进行的旨在评价HLX10疗效、安全性及耐受性的单臂、开放、多中心、II期临床试验。纳入的患者每两周静脉注射3 mg/kg HLX10,最多持续两年,直到疾病进展,出现不可接受的毒性或患者退出。该试验的主要终点为独立影像评估委员会(IRRC)依据RECIST v1.1标准评估的客观缓解率(ORR)。

试验结果
有效性-主要终点
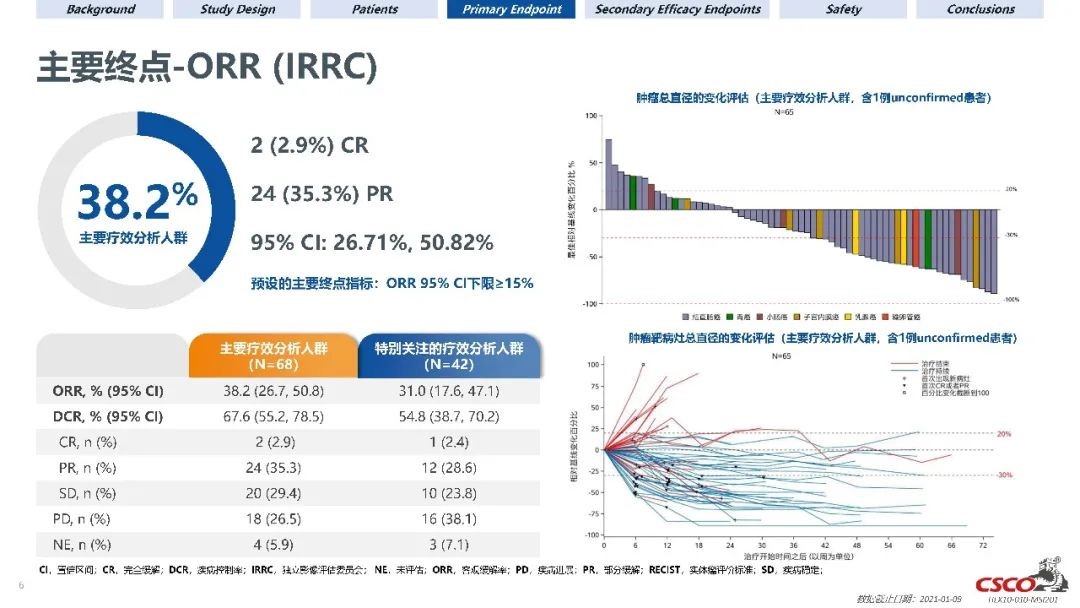
截止到2021年1月9日,本试验共入组108名患者,其中68名经中心实验室或研究中心确认MSI-H的患者被纳入主要疗效分析人群,42名被纳入特别关注疗效分析人群【包含接受过三药治疗(氟尿嘧啶类、伊立替康、奥沙利铂)的结直肠癌患者、三线及三线后胃癌患者和二线及二线后其他癌种患者】。主要疗效分析人群的中位随访时间为7.7个月(范围:1.1–16.4),特别关注疗效分析人群的中位随访时间为7.3个月(范围:1.1–16.4)。主要疗效分析人群中,经IRRC评估的ORR为38.2%(95% CI:26.7,50.8;2例完全缓解,24例部分缓解);特别关注疗效分析人群中,经IRRC评估的ORR为31.0%(95% CI:17.6%,47.1%;1例完全缓解,12例部分缓解)。
有效性-次要终点
次要疗效终点包括研究者评估的ORR、无进展生存期(PFS)、总生存期(OS)及持续缓解时间(DoR)。主要疗效分析人群的中位PFS、OS及DoR尚未达到,经IRRC评估的12个月PFS率为61.9%(95% CI:49.0,72.5),12个月OS率为81.2%(95% CI:67.8,89.4),经IRRC评估的12个月DoR率为95.7%(95% CI:72.9,99.4)。特别关注疗效分析人群中,经IRRC评估的中位PFS为4.2个月(95% CI:2.2,NR),中位DoR及OS尚未达到。
安全性
结果表明,HLX10具有良好的安全性和耐受性。
结论
HLX10在标准治疗失败的MSI-H实体瘤患者中展现了显著的抗肿瘤活性和较好的安全性。作为一种有效的组织不确定类癌症治疗候选药物,HLX10有望改善患者的临床疗效。
查看更多