查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过







近日,上海交通大学医学院附属仁济医院消化科团队研究发现产肠毒素脆弱类杆菌(ETBF)处理大肠癌细胞后产生的外泌体中miR-149-3(微小RNA miR-149-3p)减少,促进了Th17(T 辅助细胞17)分化。ETBF下调 miR-149-3p 并进一步促进 PHF5A(蛋白剪切复合体关键因子) 介导KAT2A(组蛋白乙酰化酶)的RNA(核糖核酸)的可变剪切,最终诱导大肠癌的发生。该研究成果8月6日在线发表于《胃肠病学》[Gastroenterology 2021 ,161(3):837]杂志。
ETBF感染分泌的脆弱类杆菌毒素(BFT)可引起家畜和人类腹泻, 亦可无症状地寄居于部分人群肠道内。ETBF的主要致病因素是其可以分泌BFT。近年来,ETBF与炎症性肠病、结肠炎相关大肠癌和大肠癌的发生密切相关。然而,ETBF 诱导肠道炎症和肿瘤发生的机制仍不清楚。
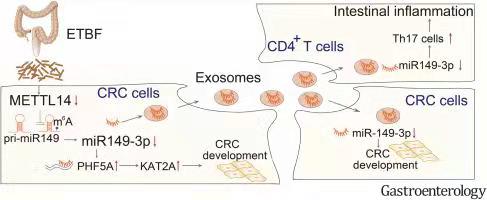
该研究中,研究人员发现ETBF处理大肠癌细胞后产生的外泌体中miR-149-3p减少,促进了Th17 细胞分化。ETBF下调 miR-149-3p 并进一步促进 PHF5A 介导KAT2A的RNA可变剪切,最终诱导大肠癌的发生。此外,研究者在临床样本验证中发现,外泌体包裹的miR-149-3p的含量在结直肠癌、活动性肠炎病患者中均显著降低。MiR-149-3p有希望成为预测肠道炎癌转化以及肠炎活动进展的生物标志物。靶向 ETBF/miR-149-3p 通路可作为一种潜在的医疗手段来治疗肠道内富含 ETBF 的肠炎和大肠癌患者。
研究人员同时发现,ETBF通过在体外和体内下调miR-149-3p来促进大肠癌细胞增殖。ETBF下调miR-149-3p依赖于METTL14(RNA甲基转移酶 14)介导的m6A甲基化。ETBF处理大肠癌细胞后,miR-149-3p的靶基因—PHF5A通过调节KAT2A mRNA的可变剪切来激活SOD2。miR-149-3p 可以被包裹在外泌体中释放并通过调节Th17细胞分化来介导细胞间交流。血浆外泌体中miR-149-3p的含量在健康对照人群、炎症性肠病以及大肠癌患者体内逐渐降低。存在于血浆外泌体中的 miR-149-3p 与炎症性肠病和大肠癌患者肠道内ETBF的丰度呈负相关。
这项基础结合临床验证的研究确定了 ETBF 促进肠炎和大肠癌变的新机制,并提供有力的证据表明 ETBF 和包裹在外泌体中的 miR-149-3p 可以作为炎症性肠病和大肠癌患者的潜在预后评估指标和治疗靶点。
论文通讯作者为仁济医院消化科洪洁研究员和陈豪燕研究员,仁济医院消化科博士研究生曹颖颖、王震华副主任医师、博士研究生严宇青、胃肠外科季林华医师、广州市第一人民医院消化科何杰教授为共同第一作者。该研究得到消化科房静远主任的大力支持以及多项国家自然科学基金的资助。
(仁济医院供稿)
查看更多