查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





人类免疫缺陷病毒(HIV)进入宿主细胞的策略是膜融合,HIV包膜糖蛋白起着融合的作用。
首先HIV包膜蛋白附着到细胞上,再与CD4受体和辅助受体(趋化因子受体CCR5或CXCR4)结合,并诱导病毒和细胞膜融合。此时,包膜蛋白会发生大的构象变化以驱动膜融合,最后病毒进入宿主细胞。
尽管包膜蛋白比那些病毒编码的酶(如逆转录酶或蛋白酶)具有更大的多样性,但包膜蛋白促进融合的构象变化暴露了一些高度保守、关键功能的区域,成为开发进入抑制剂的靶标。HIV进入抑制剂无需穿过细胞膜即可到达其靶点,因此,它是更有可能成为具有高特异性,但副作用低的一类抑制剂。
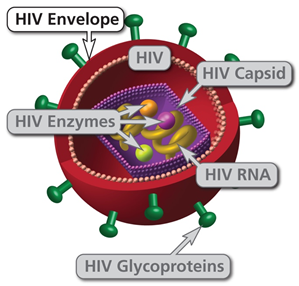
HIV的外层,由两层脂质(脂肪分子)组成
HIV使用包膜中嵌入的蛋白质“刺突”进入宿主细胞
HIV gp41六螺旋束结构的形成对病毒感染性至关重要,并且已经开发了许多基于肽的抑制剂来阻断该步骤。源自HR1或HR2的合成肽旨在结合gp41的融合中间体并防止六螺旋束的形成。T20/Enfuvirtide,一种源自gp41的36残基肽,是USFDA批准的第一个融合抑制剂。尽管取得了初步成功,但Enfuvirtide必须在低温下储存、新鲜配置并每天皮下注射两次,操作成本比较大。为了进一步提高基于HR2肽的效力,目前已经探索了不同的策略。如艾博卫泰是我国自主产权的膜融合抑制剂于2018年上市。
融合抑制剂阻止HIV胞膜与宿主CD4细胞膜融合
由于CCR5在HIV-1传播中的重要作用,已将其作为抗病毒靶标进行探索。表达CCR5D32突变的个体已被证明是健康的并且几乎完全抵抗HIV-1感染。已开发多种CCR5拮抗剂,例如Maraviroc、Aplaviroc、TAK-779、Vicriviroc,以阻断HIV-1进入。Maraviroc于2007年8月被USFDA批准的进入抑制剂。
CCR5拮抗剂阻断免疫细胞(如CD4细胞)表面的CCR5辅助受体与病毒包膜的结合
Rukobia(fostemsavir)与HIV外表面的gp120蛋白结合,干扰HIV外表面上的gp120膜蛋白与宿主细胞上的CD4受体之间的早期相互作用。从而阻止HIV进入CD4细胞。
附着后抑制剂可阻断某些免疫细胞表面的CD4受体,而HIV需要这些受体才能进入细胞。附着后抑制剂是称为进入抑制剂的一大类HIV药物的一部分。
Ibalizumab是一类CD4特异性抗体,作用部位是CD4上gp120结合位点对侧的D1-D2连接点附近的一个表位。在一项Ⅲ期临床研究中对多重耐药(Multi-drug Resistance, MDR)患者显示出明显的抗病毒效力后,Ibalizumab于2018年3月被美国食品和药物管理局(USFDA)批准,对那些MDR患者具有重要意义。
进入抑制剂具有高特异性但副作用最小的特性,有助于对艾滋病的公共措施控制,使得公共安全的危机越来越小。
马丽英 中国疾控艾防中心
本文转发自中国疾控艾防中心
往期推荐
查看更多