查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





随着人口老龄化进程加速以及肥胖、糖尿病等合并症的高发,射血分数保留型心力衰竭(HFpEF)的临床检出率呈现显著上升趋势。目前,HFpEF 至少占所有心力衰竭(简称心衰)病例的半数,被公认为是一种复杂的临床综合征。由于 HFpEF病理生理机制多样、流行病学特征各异以及诊疗策略不断更新,其诊断和管理充满挑战。本文梳理了近年来HFpEF诊疗综述中实用的临床循证建议[1-2],旨在为全科医生、基层医生和专科医生提供明确的临床指导。
心衰的定义和依据左室射血分数(LVEF)的分型
心衰的生理学定义
在生理学中,心衰被定义为:尽管充盈压是充足的,但心脏无法为代谢组织提供足够的氧气。心衰并不是一种单一的病理诊断,而是一组由心源性症状和体征组成的临床综合征。
多数心衰的定义要求患者出现主要症状,如呼吸困难、脚踝肿胀和疲劳等。这些症状可能伴有相关体征,例如颈静脉怒张、肺部啰音、外周水肿以及心功能障碍。这些定义与传统上基于LVEF百分比的收缩功能障碍的存在与否并无直接关联。
基于LVEF的心衰分类
当前的心衰命名法将LVEF≤40%的心衰定义为射血分数降低型心衰(HFrEF),LVEF ≥50%的心衰定义为HFpEF,LVEF为 41%~49%的心衰定义为射血分数轻度降低型心衰(HFmrEF)。在现行的心衰定义下,因心衰住院的成年患者中,高达50%为HFpEF患者。
HFpEF与合并症
HFpEF具有异质性,其发病机制复杂,涉及多种病理生理过程,包括心脏衰老和心脏代谢紊乱。HFpEF的患者通常年龄较大且为女性。此外,与HFrEF患者相比,HFpEF患者中肥胖、2型糖尿病、高血压、房颤、慢性肾脏病及其他非心血管疾病的发病率更高。
针对有患病风险且出现症状的HFpEF患者的诊断步骤
HFpEF的直接诊断条件
当患者出现以下临床表现时,HFpEF的诊断可能比较直接且明确:
体格检查有明显淤血体征,如腿部凹陷性水肿和肺部啰音。
利钠肽水平升高,满足欧洲心脏病学会(ESC)的标准[3]:N末端B型利钠肽前体(NT-proBNP)在窦性心律时>125 pg/ml 或心房颤动时>365 pg/ml;脑利钠肽(BNP)在窦性心律时>35 pg/ml或心房颤动时 >105 pg/ml。
有淤血的影像学证据或超声心动图提示充盈压升高。
HFpEF容易误诊和漏诊的原因
在社区中,HFpEF 的诊断要更加困难,患者可能面临误诊或漏诊的风险,原因如下,
症状汇报不充分:患者可能未充分报告症状,例如劳力性呼吸短促、端坐呼吸以及夜间阵发性呼吸困难。
对非特异性症状认知不足:疲劳、运动耐量下降和脚踝肿胀这类非特异性心衰症状,常被忽视。
未意识到肺部症状与心衰的关联:患者及部分医护人员可能未意识到肺部症状可能是由心衰引起的。
合并症干扰:存在其他疾病,这些疾病可能表现出与HFpEF相似的症状,增加了诊断的复杂性。
检查手段有限:缺乏便捷的利钠肽检测或超声心动图检查途径,限制了对HFpEF的准确诊断。
诊断不确定性:部分医护人员对如何解读利钠肽水平和超声心动图结果不够了解,导致诊断不确定性。
HFpEF的诊断路径
由于人们较少认识到心衰是一种慢性疾病,HFpEF患者可以表现为与运动相关的呼吸困难和运动耐量下降,而没有液体超负荷的体征。此外,HFpEF常见合并症的临床表现与HFpEF本身存在重叠,而且约20%的HFpEF患者利钠肽水平正常,这些因素都使得HFpEF的诊断困难。因此,对于有风险且出现症状的患者,图1展现了一个简单的诊断思路,以方便临床医生明确HFpEF诊断。
图1. HFpEF诊断流程

注:N末端B型利钠肽前体(NT-proBNP)、B型利钠肽(BNP)、二尖瓣舒张早期血流峰值速度/二尖瓣环舒张早期运动峰值速度(E/e’)、射血分数保留型心衰(HFpEF)、欧洲心衰协会HFpEF诊断评分(HFA-PEFF)、HFpEF呼吸衰竭病因诊断评分(H₂FPEF)。
HFpEF的综合管理
HFpEF管理的核心策略
HFpEF的管理方案包括识别和治疗常见的合并症。这种方案通常需要由护士、老年医学医生、药剂师和理疗师在内的多学科团队在医院中共同实施。全科医生在HFpEF管理中的参与,对于确保患者出院后护理的无缝衔接以及后续门诊监测至关重要。图2展现了HFpEF管理中的核心策略和建议。
图2. HFpEF管理的核心策略
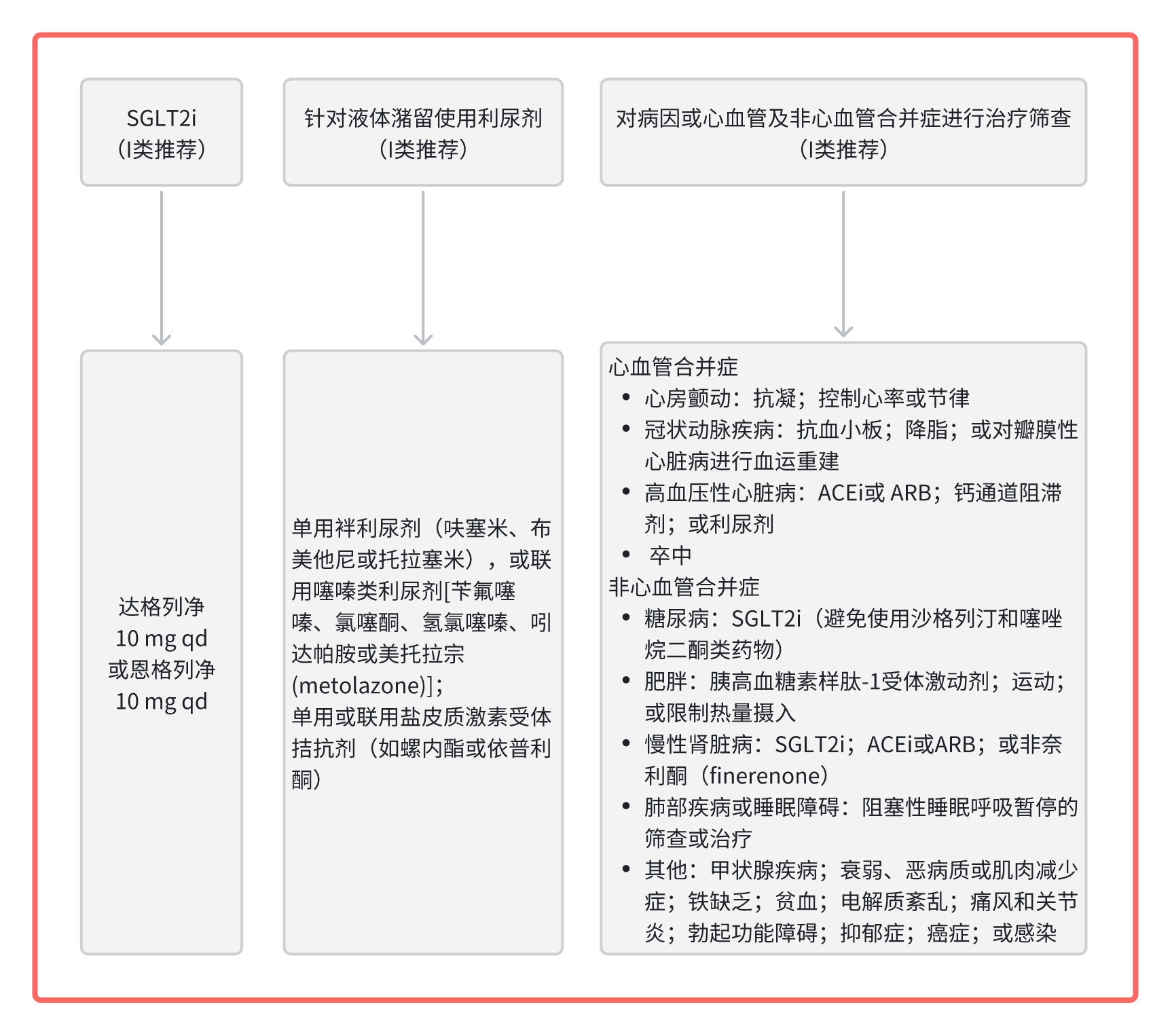
注: 血管紧张素转换酶抑制剂(ACEi)、血管紧张素受体拮抗剂(ARB)、钠 - 葡萄糖协同转运蛋白 2 抑制剂(SGLT2i)、胰高血糖素样肽-1受体激动剂(GLP-1 RA)。
合并症管理策略
针对临床中HFpEF常见合并症,下面列举了一些的管理和治疗的实用策略
高血压 按照指南推荐的血压目标进行管理,通常将血压控制在<130/80 mmHg。
冠状动脉疾病 采用抗血小板治疗;若低密度脂蛋白水平升高,则加强他汀类药物治疗;对于患有心绞痛或可诱发心肌缺血的患者,进行血运重建治疗。
肥胖症 使用胰高血糖素样肽-1 受体激动剂(GLP-1 RA)司美格鲁肽;进行有氧运动训练并限制热量摄入;开展阻塞性睡眠呼吸暂停的筛查与治疗;可考虑进行减重手术。
糖尿病 对于患有慢性肾脏病或存在蛋白尿的患者,使用血管紧张素转换酶抑制剂(ACEi)或血管紧张素受体拮抗剂(ARB);若使用ACEi或ARB治疗但仍存在蛋白尿,可使用非奈利酮(finerenone)。
慢性肾脏病 对于存在蛋白尿的情况,使用ACEi或ARB;使用钠-葡萄糖协同转运蛋白2抑制剂(SGLT2i);对于患有糖尿病且已使用ACEi或ARB治疗但仍存在蛋白尿的患者,使用非奈利酮。
心房颤动 进行抗凝治疗;若病情允许,可在房颤初始阶段考虑节律控制;心率控制的目标是每分钟约80-90次。
心脏变时功能不全 除非存在强适应证,否则避免使用β受体阻滞剂。
HFpEF的药物管理
近年来,针对HFpEF的药物治疗研究持续推进。药物治疗作为HFpEF综合管理的关键构成部分,在缓解临床症状、预防并发症以及改善临床结局等方面均发挥着基础性且至关重要的作用,以下介绍了临床上常用的治疗药物。
SGLTi 该药对HFpEF治疗的首次阳性结果发表于2021年和2022年,在EMPEROR-Preserved和DELIVER 试验中,SGLT2i将心血管死亡和因心衰住院的复合终点降低了20%[风险比(HR)0.80,95%置信区间(CI):0.73~0.87,P<0.0001]。 2023 年ESC心衰指南更新版已将SGLT2i用于HFpEF治疗列为Ia类推荐。[4]
用于治疗淤血的药物 对于容量超负荷的患者,使用利尿剂缓解淤血仍然是HFpEF治疗的基石。治疗以袢利尿剂开始,类型和剂量取决于容量超负荷的严重程度。对于使用袢利尿剂利尿效果不佳的患者,可以加用以下药物,可单选或联用:噻嗪类利尿剂、噻嗪样利尿剂、盐皮质激素受体拮抗剂(MRA)。
GLP-1 RA STEP-HFpEF试验评估了司美格鲁肽在治疗HFpEF中的有效性。司美格鲁肽显著改善了健康状况并减轻了体重。与安慰剂相比,使用司美格鲁肽时,NT-proBNP水平的降幅约高出15%,这表明左心室充盈压有所降低。司美格鲁肽还降低了C反应蛋白。
血管紧张素受体-脑啡肽酶抑制剂(ARNi)和MRA 根据 2022 年美国心脏病学会/美国心脏协会治疗指南[5],可以考虑对HFpEF患者使用额外的治疗方法,这些药物包括ARB、ARNi和 MRA。尽管这些药物在HFpEF的关键随机对照试验中均未改善主要结局,但后续分析表明这些药物可能对部分HFpEF患者有益。
回顾与总结
避雷要点一:切勿因患者症状不典型或利钠肽水平正常而直接排除HFpEF,HFpEF的诊断常因合并症干扰及表现隐匿而被漏诊或误诊。
避雷要点二:积极治疗高血压、肥胖、糖尿病及房颤等是改善HFpEF预后的核心策略。
避雷要点三:避免沿用过时的治疗方案,SGLT2i已被2023年ESC指南列为改善HFpEF预后的Ia类推荐药物。


编译:王天任
审校:邢英

互动有奖


所有参与互动答题的医生都将获得价值150元的《中国医学论坛报》数字报一年期权限和《35天医疗AI实战计划》训练营观看权限。
活动截止时间:2025年7月9日

查看更多