查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





近日,2021年的国家自然科学基金(以下简称“国自然”)公布了最新结果,相信医生朋友在短暂的休整后,紧接着就要考虑明年申请的主题了。
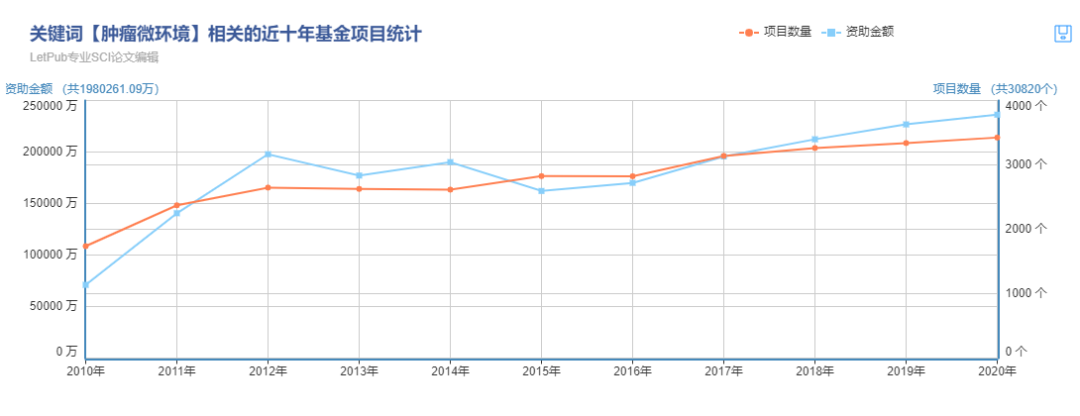
肿瘤微环境(TME)在肿瘤的发生、发展、转移以及药物敏感性方面扮演着重要角色。有关TME的研究,近几年的在Pubmed上的发文量如同中国的GDP般直冲云霄。
那么,肿瘤微环境在最近几年有多少值得深挖的研究方向呢?
小编今天就通过一篇最新发表在《环境与临床癌症研究杂志》(Journal of Experimental & Clinical Cancer Research)的综述为大家逐一探讨这些研究方向,由于原文过长,小编不得不分为三部分为您讲解。今天是第一部分:

研究方向一:肿瘤微环境中成纤维细胞(CAF)和巨噬细胞(TAM)的异质性研究
在TME中,引起异质性的主要细胞亚群是CAFs和TAMs。各种CAFs具有不同的标记物,如FAP、PDGFR、FSP1、波形蛋白、纤维连接蛋白、αSMA或CD90。事实上,实体瘤能够促进几种细胞类型转化为CAF,如间充质干细胞(MSCs),成纤维细胞,甚至周细胞,前体细胞的性质可能决定了CAF的最终分子特征。
考虑到CAF相关标记物的多样性以及这些生物标记物中的几个可能共存于单一类型的CAF中,因此,这一研究方向可以考虑研究不同类型癌症之间以及具有相同肿瘤类型的不同患者之间的可变CAF亚群。此外,也可利用蛋白质组学研究这种异质性。例如, CAFs分泌的特定LOX/LOXL酶在不同前列腺癌患者中的功能作用,患者间CAFs异质性等。可以认为CAFs异质性是肿瘤间和肿瘤内异质性的反映,这种异质性与每个肿瘤内在的DNA突变、表达模式甚至蛋白质组学特征的差异有关。
在几乎所有实体恶性肿瘤中,肿瘤细胞在功能上可分为两大类:高分化/高增殖的肿瘤细胞和低分化/低增殖的肿瘤干细胞(CSC)。重要的是,这种功能分类与周围的TME组织有关。
事实上,有几项研究建立了两组功能不同的CAF。例如,在前列腺癌中,已经证明第一亚组的CAFs通过分泌Wnt-3a促进癌细胞的增殖,而第二亚组的CAFs通过分泌SDF1增强癌细胞的转移能力和侵袭性(众所周知的CSCs特性)。Patel及其同事在口腔癌中也观察到了类似的发现,其中一组CAFs促进了肿瘤细胞的过度增殖,而另一组CAFs则增强了肿瘤的干细胞活性,从而增强了其转移潜能。这两个功能不同的CAF亚群在其他研究中被确定为促炎性CAF,对应于促进增殖的CAF和肌成纤维细胞样CAF。
值得注意的是,Pelon和他的同事们发现αSM是一种全肌成纤维细胞样CAFs相关的生物标记物。在这种情况下,纤维连接蛋白和钙调素也被认为是肌成纤维细胞样CAFs生物标记物。
TAM主要来源于循环系统中的单核细胞或组织内的巨噬细胞,这些不同的来源可能是TAM标记物特异性产生的原因。此外,起源肿瘤的特异性分子标记也可能影响TAMs的最终表达谱和生物标记物。与CAFs类似,单个TAM也可以同时表达几种生物标志物。因此,不同癌症类型和相同恶性肿瘤患者之间存在不同的TAM亚群并不奇怪。
另一方面,TAMs在功能上也可分为两大类:(Ⅰ)典型激活的肿瘤抑制性M1 TAM和(Ⅱ)交替激活的肿瘤支持性M2 TAM。此外,已经证明M1巨噬细胞与炎症和病原体的死亡密切相关,而M2巨噬细胞则与组织修复密切相关。M1相关的几种标记已经被鉴定出来,如MHC-Ⅱ、CD40、CD80或CD86;M2相关标记,包括CD163、CD204、CD206或CD20。另外,同时表达M1和M2相关标记的TAMs也有被报道,这增加了TAMs的高度异质性,使其难以被进行精确分类。
有趣的是,据报道CAFs和TAMs在TME和肿瘤肿块内都有特定的空间分布,这可能与CSCs主要位于肿瘤边缘的空间分布有关。
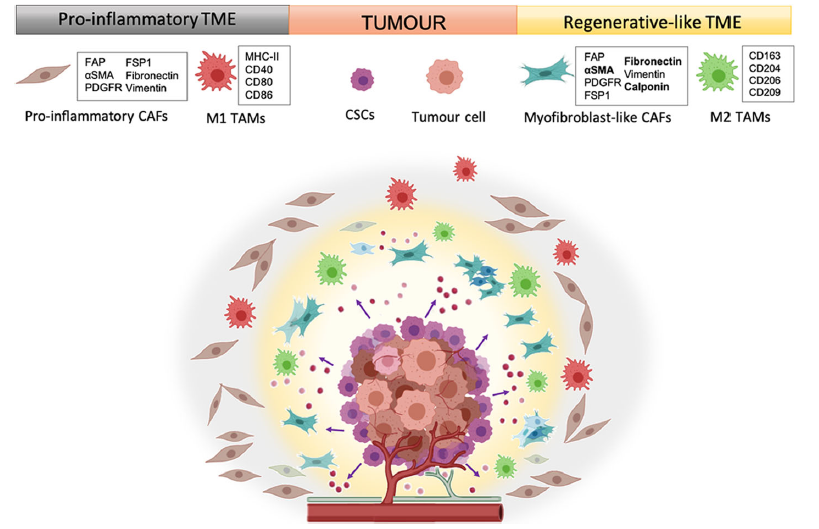
关于TAMs,已经发现表达有CD68+/CD163+的M2 TAMs可从肿瘤巢和TME中的远处向皮肤黑色素瘤的浸润前沿逐渐积聚。在另一项关于胶质母细胞瘤的研究中,作者观察到远离肿瘤的TME主要含有促炎性TAM,而靠近肿瘤的微环境主要含有抗炎性TAM。这一事件是相关的,因为M2巨噬细胞可能与抗炎表型有关,考虑到肌成纤维细胞与伤口愈合之间众所周知的关系,以及M2巨噬细胞与组织修复/再生之间的关系,实体恶性肿瘤的TME中可能存在两种亚微环境:(1)一种再生的类TME,具有高度积累性的肌成纤维细胞样CAF和M2 TAM,位于肿瘤边缘靠近CSCs的位置和(2)促炎性TME,促炎性CAFs和M1-TAMs高度聚集,在远离CSCs的位置(图1)。
有必要澄清的是,位于肿瘤边缘的CSCs可能出现在肿瘤发展的晚期。因此,这两个亚微环境的建立也可能在肿瘤发展的晚期,而不是在早期。基于TME生物标志物表达和功能异质性与实体瘤的细胞空间组织分布研究,可能是这一研究方向的热点。
科研讲坛 平台发布
查看更多