查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





已在用抗肿瘤治疗药物的患者,能否同时服用奈玛特韦/利托那韦?
推荐意见:
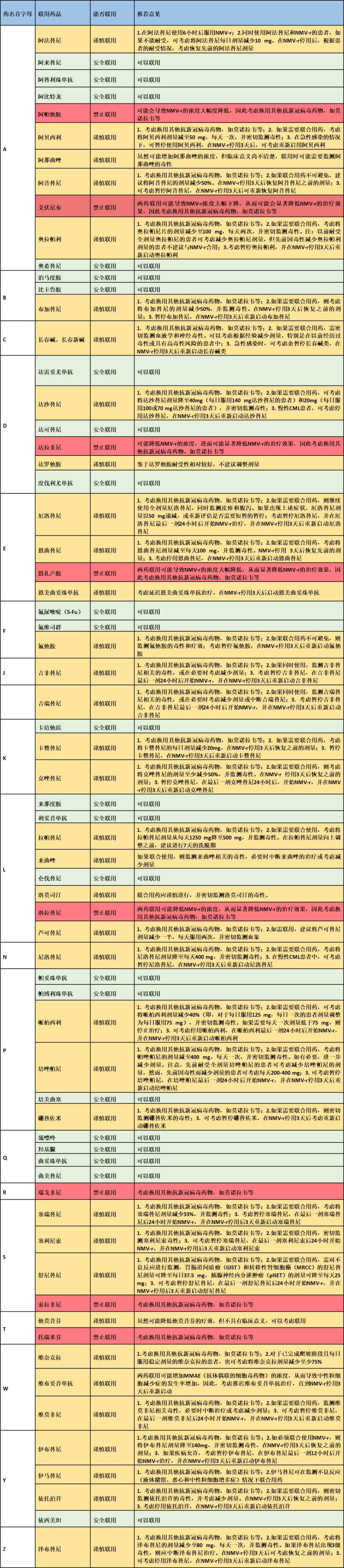
(1)目前临床常用的抗肿瘤药物多数是CYP3A4和P-糖蛋白的底物和(或)抑制剂/诱导剂,因此和奈玛特韦片/利托那韦片联用时需注意药物的相互作用。
(2)下表所示为奈玛特韦片/利托那韦片与抗肿瘤药物联用时的相关药学建议(药品按照首字母排序,便于检索)。
奈玛特韦/利托那韦和抗真菌药物合用存在药物相互作用吗?应该如何联用?
推荐意见:
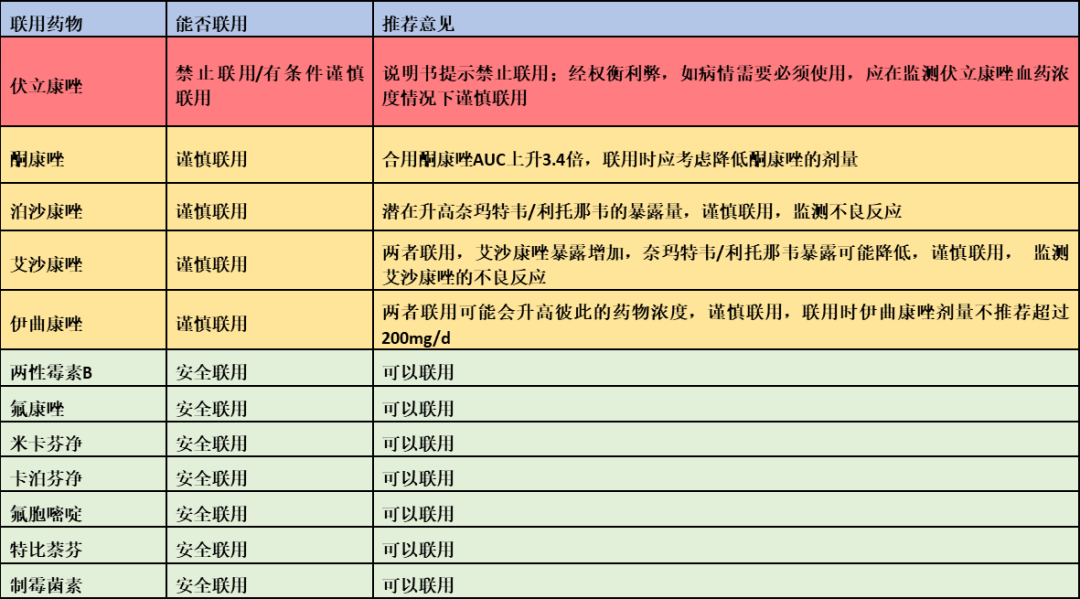
推荐依据:
奈玛特韦/利托那韦与三唑类抗真菌药物合用,可能存在复杂的药物相互作用。其中,三唑类抗真菌药物通过细胞色素P450同工酶代谢,并抑制细胞色P450同工酶的活性,包括CYP2C19,CYP2C9和CYP3A4等,这些同工酶的抑制剂或诱导剂可能分别增高和降低三唑类抗真菌药物的血药浓度,而三唑类抗真菌药物本身也会增高通过CYP450同工酶代谢药物的血药浓度。相互作用研究表明,伏立康唑与不同剂量的利托那韦合用,彼此的体内暴露均会出现下降;利托那韦可使酮康唑AUC上升3.4倍,Cmax增加34%;NMV-r与伊曲康唑或泊沙康唑合用时,可能会增加奈玛特韦体内暴露量。艾沙康唑与奈玛特韦/利托那韦联用,艾沙康唑暴露增加,奈玛特韦/利托那韦暴露可能降低。
透析患者如何使用奈玛特韦/利托那韦?eGFR<30 ml·min-1的患者能否使用奈玛特韦/利托那韦?CRRT患者如何使用奈玛特韦/利托那韦?
推荐意见:
终末期肾病或透析患者在目前仍然缺乏充分的临床数据,尽管说明书中认为不应使用,但该部分患者面临重症风险,在权衡利弊后,可考虑使用。

推荐依据:
奈玛特韦的分子量为499.5D,药动学研究表明,两种成分的消除途径分别是奈玛特韦约35%由肾脏排出,70%与血浆蛋白结合;利托那韦主要由肝脏代谢,99%与血浆蛋白结合。奈玛特韦的暴露量随着肾功能损伤严重程度的增加而增加,由于缺乏相关研究数据,药品说明书指出严重肾功能损伤患者(eGFR<30 ml·min-1,包括血液透析下的ESRD患者)不推荐使用。
目前有报道终末期肾病(ESRD)患者使用奈玛特韦片/利托那韦片的研究,研究对4名接受间歇性血液透析的ESRD患者进行药代动力学研究,结果显示奈玛特韦Cmax较非ESRD患者高4倍(4563~7898 ng/ml),但没有观察到奈玛特韦的蓄积,且治疗结束后几天内血浆水平迅速下降。这些患者的给药剂量为150 mg/100 mg,BID,血透当天在给药2~6小时后开始透析治疗。
另有研究针对8名严重肾损害患者的Ⅱ期研究中(eGFR,30 ml/min/1.73 m2,非透析),单次服用100 mg奈玛特韦后24小时的平均浓度为694.2 ng/ml(超过所需292 ng/ml的两倍),但未见有剂量依赖性的不良反应。对于血透患者,建议第一天服用300 mg/100 mg,之后每天服用150 mg/100 mg,QD,血透当天在透析后使用。体重≤40 kg的患者建议每48 h服用150 mg/100 mg。
根据药动学数据推测奈玛特韦30%的游离药物可能会被CRRT清除,其表观分布容积为109.4 L,理论上被CRRT清除的量可忽略不计;综合考虑下,推测CRRT患者可以按正常剂量用药。
12周岁以下或体重小于40 kg的儿童患者是否可以使用奈玛特韦/利托那韦?
推荐意见:

推荐依据:
2021年12月22日,FDA批准奈玛特韦/利托那韦用于12~17岁、体重≥40 kg且伴有高风险因素的新型冠状病毒感染青少年患者。目前奈玛特韦/利托那韦尚未被批准用于6~12岁的儿童,但目前有一项针对18岁以下儿童的Ⅱ/Ⅲ期临床研究正在进行,6~17岁少年儿童的用法用量根据辉瑞公司官方及Clinical Trails网站信息推荐。
另外需要注意的是,奈玛特韦片含乳糖(176 mg/片),患有乳糖不耐受、总乳糖酶缺乏或葡萄糖-半乳糖吸收不良等罕见遗传代谢疾病的患儿不应服用此药;既往有肝胆疾病、肝酶异常或者肝炎、黄疸的患儿应慎用。
育龄期、妊娠期、哺乳期患者是否可以使用奈玛特韦片/利托那韦片?
推荐意见:
(1)育龄期:建议在治疗期间以及治疗结束后7天应避免怀孕;
(2)妊娠期:建议仅在母体的潜在获益大于对胎儿的潜在风险时使用;
(3)哺乳期:建议治疗期间以及治疗结束后7天停止哺乳。
推荐依据:
目前妊娠期妇女使用奈玛特韦片/利托那韦片的临床数据有限。利托那韦可安全用于HIV感染孕妇患者,基于奈玛特韦和利托那韦的作用机制以及现有的动物研究,根据风险-获益评估,NIH指南建议符合条件使用奈玛特韦片/利托那韦片的妊娠或近期妊娠患者使用奈玛特韦片/利托那韦片。此外,1项研究显示7名接受奈玛特韦片/利托那韦片治疗的妊娠患者,除1名患者外(味觉障碍),其余患者完成疗程后,没有立即出现不良反应,也没有观察到对胎儿或新生儿的不良影响。
目前尚无哺乳期人群使用奈玛特韦片/利托那韦片的临床数据,尚不清楚奈玛特韦是否会分泌至乳汁中,及其对母乳喂养的新生儿/婴儿的影响或对乳汁分泌的影响。但动物研究显示,当大鼠暴露于8倍的奈玛特韦人体批准剂量时,后代出生17天后体重降低8%。关于人乳中存在利托那韦的报告有限。基于此,建议治疗期间以及治疗结束后7天停止哺乳。
尚缺乏妊娠期间使用本品的数据,因而不了解药物相关不良发育结局的风险,建议育龄期女性在治疗期间以及治疗结束后7天应避免怀孕。利托那韦与激素类避孕药联用时可能降低后者疗效,建议使用复方激素类避孕药患者在治疗期间及停用后的一个月经周期内使用替代避孕方法或额外的屏障避孕方法。
奈玛特韦/利托那韦能否管饲给药?应如何操作?
推荐意见:
(1)将利托那韦和奈玛特韦直接压碎并与水(约20~50 ml)混合,通过饲管给药;给药后用适量水冲洗管路。混悬液建议临用前配置。
(2)使用小孔径管路(如空肠管)管饲药物可能造成堵管,可适量增加溶媒后给药。管饲营养液或食物不影响奈玛特韦/利托那韦给药。
推荐依据:
奈玛特韦为薄膜包衣片剂,非缓释或控释制剂。奈马特韦与利托那韦均可掰开、压碎,并与苹果酱、布丁或任何普通食品或液体(包括含乳制品)混合。基于I期研究表明,混悬液与整片药物具有相似的药代动力学。由于缺乏奈玛特韦混悬液稳定性数据,建议临用前配制。奈玛特韦混悬液与利托那韦同时使用时,食物对其吸收影响不大,无需禁食后给药。
本文节选自浙江省药事管理质控中心发布《浙江省新型冠状病毒感染临床用药建议(第一期,2023年1月8日)》

查看更多