查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





基本资料
性别:女性
年龄:68岁
现病史:
2015年03月在我院查全腹部增强CT考虑直肠癌,肠镜示(距肛门8cm)直肠腺癌,后转至上海第六人民医院行腹腔镜下直肠癌根治术,术后未行放化疗。
2017年11月底患者出现大便带血,盆腔MR增强(2017-11-17):直肠癌术后改变,吻合口右旁见不规则软组织肿块影,增强后不均匀强化,其与子宫局部分界欠清,考虑直肠癌复发。
2017年12月04日在上海第六人民医院行全麻下直肠恶性肿瘤切除术,术中发现阴道转移,遂联合妇产科切除阴道。手术病理:(阴道后壁、阴道后壁切缘)纤维结缔组织内见癌浸润,(左侧阴道残端)未见肿瘤,(直肠下切缘)送检组织未见癌浸润
术后患者出现阴道瘘,予抗感染营养支持等治疗后好转。2018年03月17日开始给予FOLFOX方案化疗6周期。
2018年11月查PET/CT示直肠癌术后,术区粘膜增厚,与子宫边界不清,正中腹壁、左侧盆底见结节影,考虑直肠癌复发累及子宫伴正中腹壁、左侧盆底转移可能性大。
2018年12月03日在上海市第六人民医院行横结肠造口术+腹壁肿瘤切除术+腹腔粘连松解术,术后病理示(腹壁结节)纤维结缔组织内见腺癌浸润,符合肠腺癌转移/浸润。
2019年01月08日针对直肠吻合口复发病灶及盆腔转移病灶予姑息放疗,总剂量45GY/25F/5W,放疗过程顺利,后随访。
主诉:2019-04出现腹痛
既往史:无特殊
辅助检查
影像学检查:
2019-04-24 CT检查: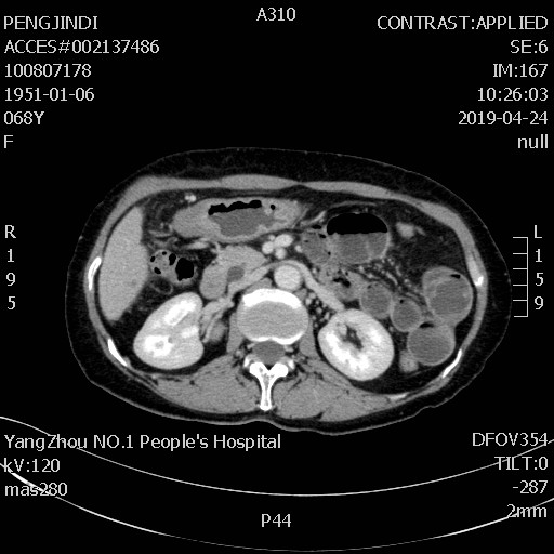
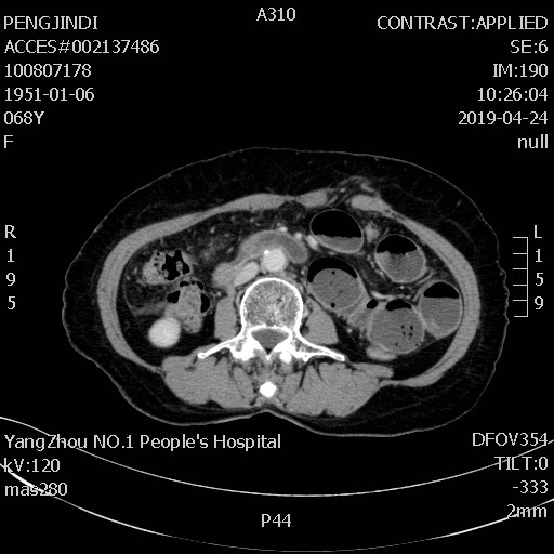
CT检查提示:左腹部部分小肠扩张积液,见气液平,两侧髂窝、局部肠间隙见少许水样密度影。腹腔及右侧结肠旁沟见多个结节状稍高密度影,最大者长径约2.5cm。与前片(20180925)相比:左下腹造瘘、小肠梗阻及腹腔多发结节为新增。考虑病情再次进展。
治疗过程:
2019年05月14日行瑞戈非尼160mg qd。
服药一周后出现全身散在红色皮疹。双手手指红肿,刀割样疼痛,
需要使用吗啡来止痛。
临床应用瑞戈非尼时出现手足皮肤反应、高血压、肝功能异常等不良反应
如何看待瑞戈非尼的不良反应?
瑞戈非尼治疗相关的AEs属可控范围
CONCUR研究:
无力/疲乏, 手足皮肤反应, 腹泻, 高血压, 发声困难等最为常见(≥30%), 大多数为1或2级
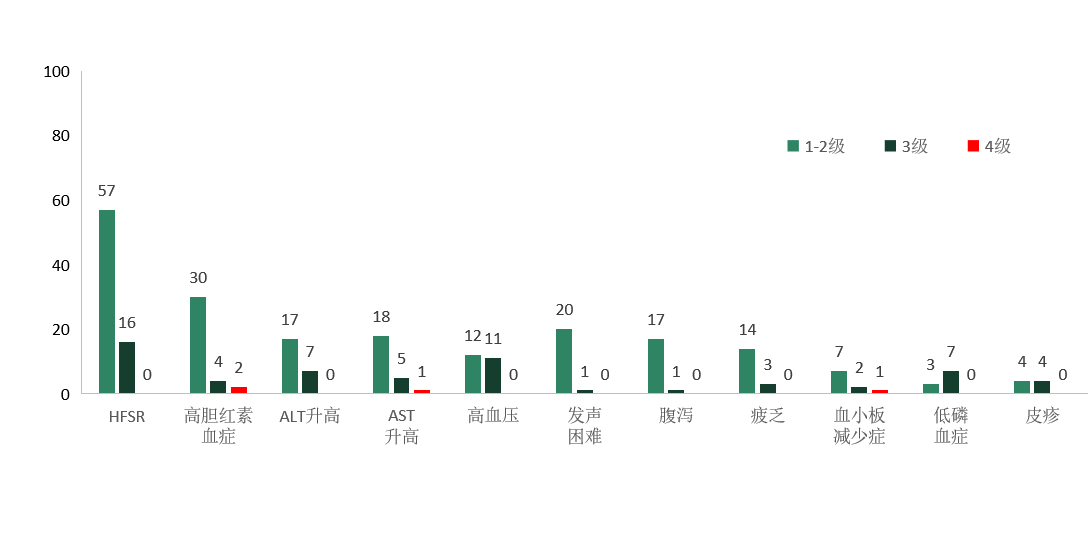
随着疗程的继续及剂量调整不良反应发生率呈降低趋势,提示耐受性增加
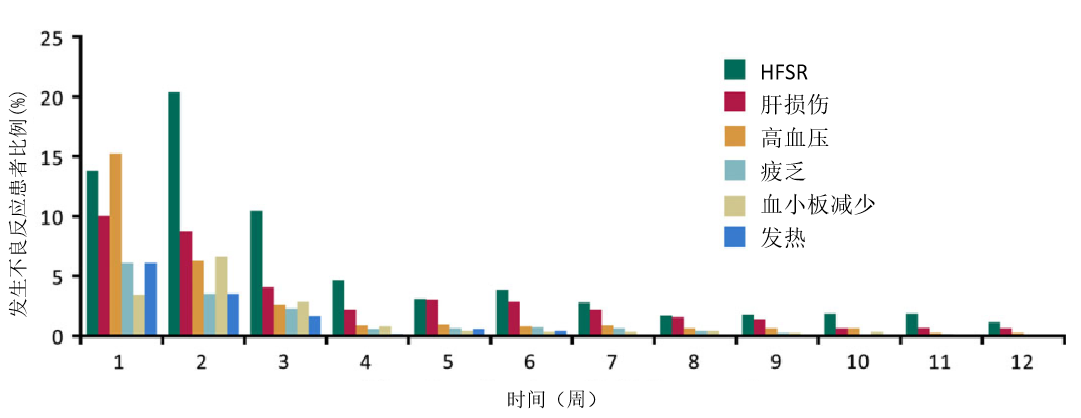
日本PMS研究:不良事件一般在治疗早期发生,且发生率随时间呈下降趋势
瑞戈非尼I期研究提示160mg为最大耐受剂量
评估瑞戈非尼口服用药21天/停药7天治疗方案在晚期实体瘤患者中的安全性、耐受性、抗肿瘤活性、药代动力学以及药效动力学特性
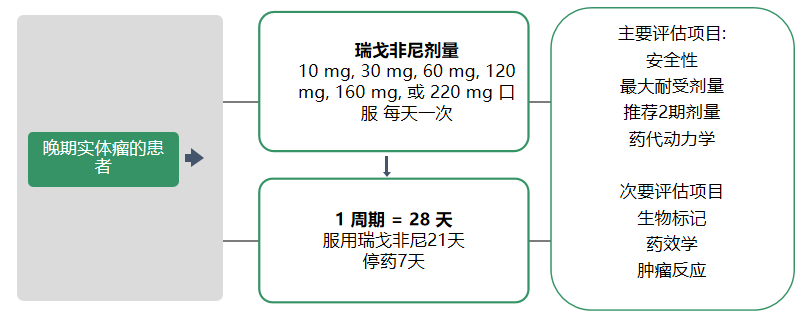
在120mg组,没有病人产生剂量限制性毒性(DLT);
在160mg组,12人中有2人产生DLT;
在220mg组,12人中有5人在第一周期产生DLT。
基于耐受性以及PK/PD评估,在每日单次口服片剂,以4周(28天)为1个周期、给药3周/停药1周的给药方案中的最大耐受剂量为160 mg
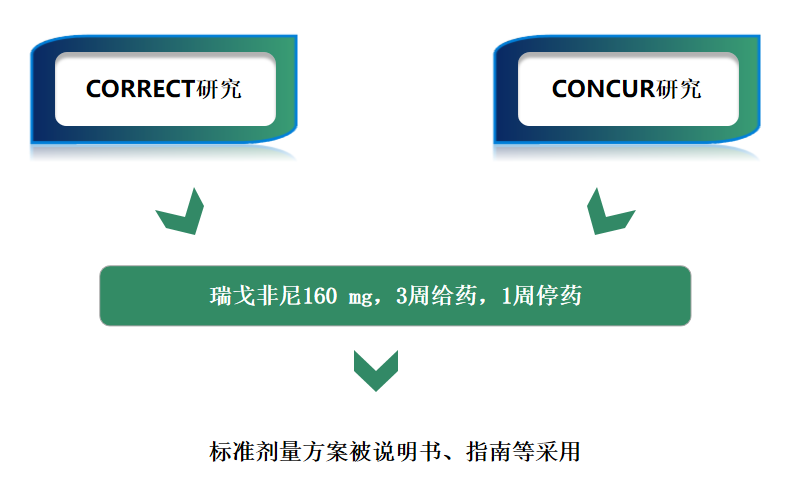
Ⅲ期研究:沿用和确立瑞戈非尼160mg 为标准剂量
ReDOS研究:瑞戈非尼剂量递增方案 可能是一种剂量选择策略
瑞戈非尼剂量优化研究(ReDOS*):在复发转移性结直肠癌患者中评估瑞戈非尼剂量递增和预防性局部使用激素策略的随机II期研究—ACCRU 网络研究

根据是否局部用激素处理,按1:1:1:1随机分成四组,A1组和B1组(组1)预防性局部使用激素12周;A2和B2组(组2)根据药物反应使用局部激素。
研究达到了主要研究终点;瑞戈非尼低剂量 vs 标准剂量,生存获益无显著差异
中位PFS 2.5月(低剂量)vs. 2月(标准剂量)
研究入组人群为欧美患者,基线时67%患者转移灶≥3个(预后不佳)
日本II期研究:瑞戈非尼剂量调整用于 标准化疗失败的不可切除转移性结直肠癌患者
背景: 160mg/d是瑞戈非尼的标准起始剂量, 但部分病例因不良事件(AE)需下调剂量至120mg/d或更低, 这在日本人群进行的研究中更常发生(84.6% vs 51.3%)
本研究旨在通过剂量滴定研究瑞戈非尼的有效性和安全性
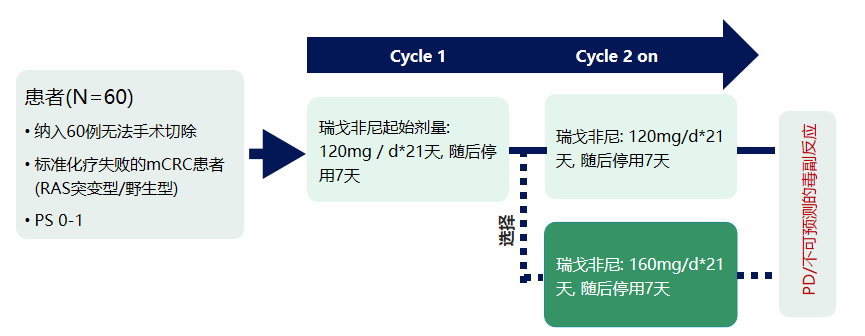
单臂多中心II期研究, 2015年9月10日至2017年3月7日期间, 共入选60例患者, 中位年龄为68.5(范围: 30-84), ECOG PS 0/1为70%/ 30%
患者每8周接受影像学评估:
主要终点: 疾病控制率(DCR: CR + PR + SD≥6周)
主要的次要终点: 无进展生存(PFS), OS和安全性
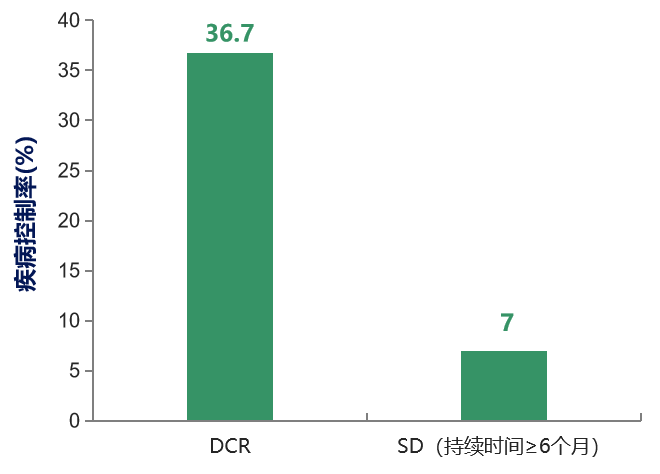
日本II期研究:提示瑞戈非尼 起始剂量120mg显示出与160mg疗效可能相当
DCR为36.7% (22/60) ; 7% (4/60)的患者, SD≥6个月
中位PFS: 2.3个月(95%CI: 1.8-2.8)
3.3% (2/60)的患者按规定剂量递增至160mg; 42% (25/60)因AE降低剂量至80mg
55% (33/60)的患者发生3-4级AE
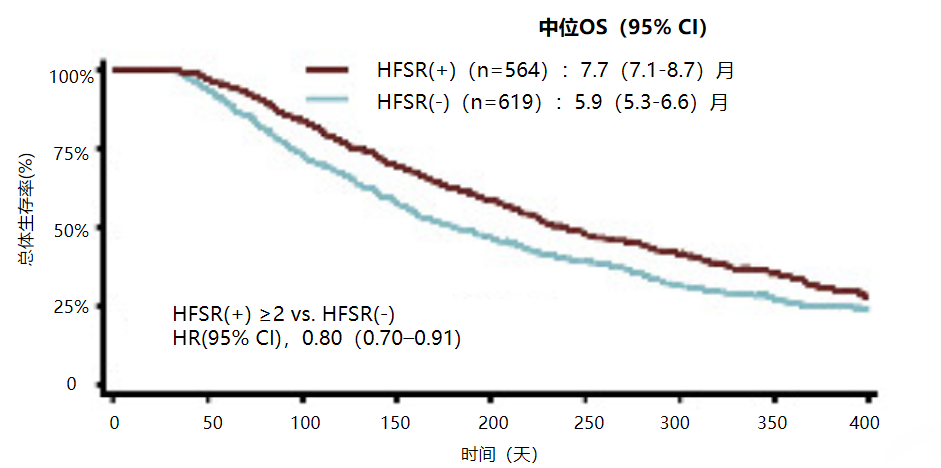
日本PMS研究:更低剂量方案可能降低HFSR和肝功能损伤的发生率
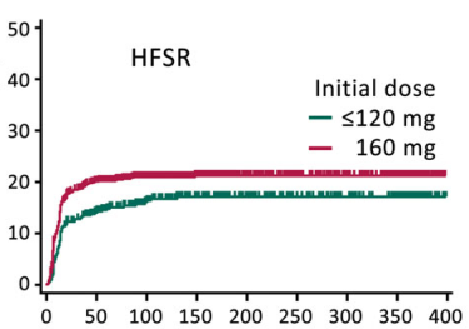
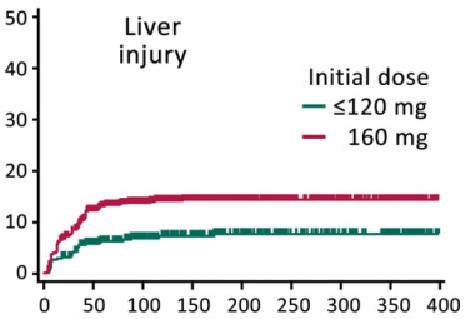
HFSR, 手足皮肤反应
HFSR是瑞戈非尼治疗的一种常见不良反应

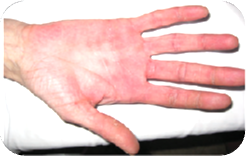
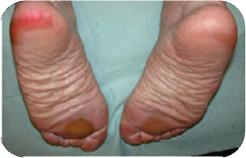
早期出现手足皮肤反应者,OS获益相对更佳
日本PMS真实世界研究
剂量调整
该患者经过停药、止痛等处理后。手指红肿、疼痛缓解,皮疹消退。继续给予瑞戈非尼,剂量调整为先服用80mg,服用一周后加量到120mg。患者未出现不良反应。
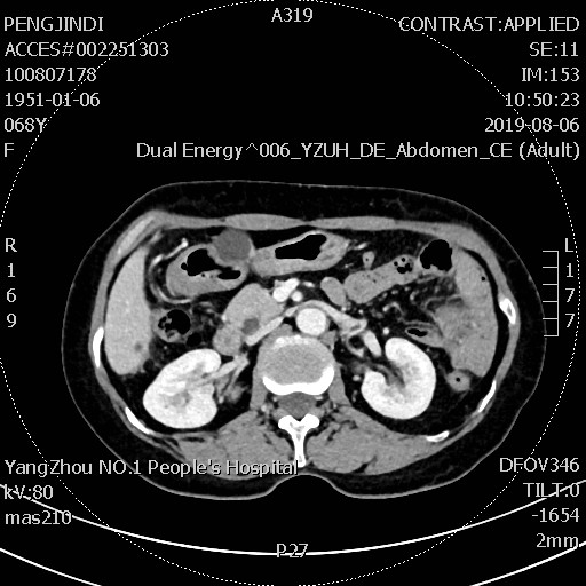
患者无明显腹痛,肠梗阻等症状。2019-08 CT检查:腹盆腔见多发不规则片絮状及结节状稍高密度影,境界欠清。右侧髂窝见少许水样密度影。与前片(20190424)相比:左腹部部分小肠扩张积液好转;盆腔积液大部分吸收。
目前继续治疗及随访中。
2019-08-06 CT检查:
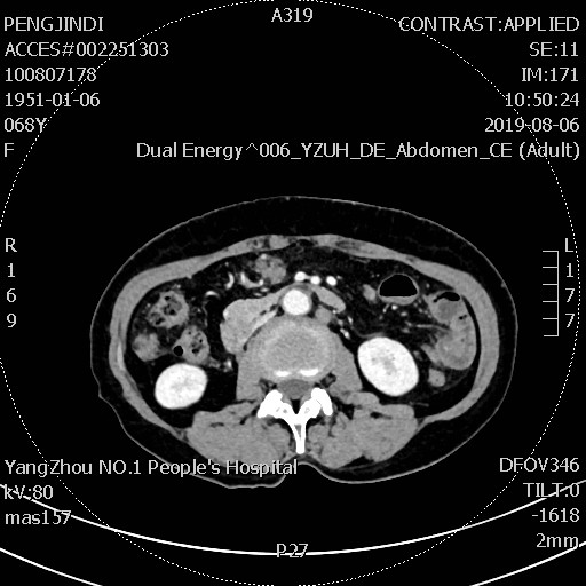
病例总结:
瑞戈非尼安全/耐受性可能随剂量管理或治疗周期而改善;
瑞戈非尼起始剂量120mg或80mg可能降低患者不良反应;
瑞戈非尼治疗过程中,早期发生HFSR与更好的OS相关。
查看更多