查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





宫颈癌是女性常见的恶性肿瘤,根据国际癌症研究机构发布的数据,2022年预计宫颈癌新发病例111,820例,死亡病例61,579例,宫颈癌发病率和死亡率均有上升[1]。当前,针对晚期宫颈癌的治疗常采取同步放化疗为主,然而对于复发和转移性晚期宫颈癌,治疗后复发率高、生存率低等问题依然存在[2]。因此,寻找新的治疗方法以提高晚期宫颈癌患者的生存率并改善预后变得尤为迫切。
在近日举行的2023年欧洲肿瘤内科学会亚洲年会(ESMO Asia)上,呋喹替尼联合信迪利单抗治疗晚期宫颈癌的II期研究入选了口头汇报。本报特邀该研究Leading PI,复旦大学附属肿瘤医院吴小华教授进行访谈,探讨呋喹替尼联合免疫治疗在妇科肿瘤领域的前沿研究进展。
吴小华 教授
复旦大学附属肿瘤医院主任医师、博士生导师
复旦大学附属肿瘤医院妇瘤科主任、妇科肿瘤多学科综合治疗团队首席专家
中国抗癌协会卵巢癌专委会主任委员
中国初级卫生保健基金会妇科专委会主任委员
上海市抗癌协会妇科肿瘤专委会前任主委
中国抗癌协会常务理事
上海市抗癌协会常务理事
中国临床肿瘤学会(CSCO)理事
IGCS国际委员会委员、亚太理事提名人
SGO教育委员会委员、执行委员
西北大学Feinberg医学院妇产科系客座教授
NCCN国际审阅专家;Int. J. Gynecol Cancer, Cancer Medicine, J. Gynecol Cancer, 中华妇产科学,中华临床解剖学等杂志编委
吴小华教授访谈视频
未尽之需:复发转移率高、预后差,宫颈癌新治疗方案亟待探索
宫颈癌是我国女性常见的恶性肿瘤之一,根据您的临床经验,请您为我们讲解一下宫颈癌的治疗现状和预后如何?目前临床上还存在怎样的治疗需求?
宫颈癌作为我国女性第二大常见的生殖系统恶性肿瘤,其早期治疗目前主要采用根治性手术和放疗[3]。然而,大多数患者在治疗后2年内都会面临复发或转移的风险,且预后相当不乐观,其5年生存率仅为17%[4]。目前,针对复发转移性宫颈癌患者的一线标准治疗方法是联合应用含铂化疗和抗血管生成治疗[5]。这种治疗方案已经被广泛采用,并取得了一定的疗效。然而,该方案所带来的不耐受性和最终产生的耐药性限制了其在复发转移性宫颈癌患者中的应用,导致疾病最终出现进展。而对于那些经历了一线及以上系统治疗失败的复发转移性宫颈癌患者来说,目前还没有既定的二线治疗标准,后线治疗的选择较少、效果有限[6],这就造成了一个重要的未被满足的需求。
因此,我们希望加大对复发转移性宫颈癌的研究力度,寻找新的药物和治疗策略,探索新的有效治疗方案,以提高这些患者的生存率和生活质量,满足患者需求并改善预后。
一展宏图:呋喹替尼联合免疫治疗探索妇科肿瘤治疗新纪元
呋喹替尼联合信迪利单抗的“幸福组合”方案的疗效,已经在消化道肿瘤及多项实体瘤研究中进行验证。本次您牵头的这项研究正式该方案在宫颈癌中的探索,并在近期举行的ESMO Asia年会上以口头报告形式重磅发布,请问您的团队在方案选取和研究设计上经历了怎样的考量?
抗血管生成药物联合免疫治疗是肿瘤领域研究的热点,两者在治疗中可以产生协同作用,在多个瘤肿研究中已得到验证。
选择抗血管生成药物时,呋喹替尼作为我国自主研发、主要靶向血管内皮生长因子受体(VEGFR-1/2/3)激酶,其具有激酶选择性高、对其他激酶脱靶活性低的特点,因此在联合用药中具有较好的适配性。呋喹替尼的疗效及安全性也已经在结直肠癌2项大型III期研究中得到证实[7,8]。2018年9月,国家药品监督管理局批准呋喹替尼用于三线晚期转移性结直肠癌的治疗;2023年11月,呋喹替尼在美国获批上市,并于2023年6月和9月分别在欧洲及日本提交了上市申请。
临床前研究表明[9],呋喹替尼联合免疫治疗具有一定的抗肿瘤增效作用,在抑制肿瘤新生血管形成的同时,亦能促进血管正常化、增强杀伤性T细胞浸润,降低PD-1阳性的CD8+T细胞,促进杀伤功能,同时调节TAM和促进M1型巨噬细胞极化,增强吞噬功能。在呋喹替尼联合信迪利单抗治疗晚期实体瘤的Ib/II期研究中,我们选择子宫内膜癌和宫颈癌两个队列同时开展研究探索。
子宫内膜癌队列的结果已于2021年CSCO年会公布[10]。研究结果表明,在二线及以上pMMR晚期子宫内膜癌患者中,呋喹替尼联合免疫治疗的ORR和DCR分别为36.8%和94.7%,中位无进展生存期(mPFS)为6.9个月,中位总生存期(mOS)未达到。该研究的安全性与同类抗血管生成药物联合免疫治疗报道的安全性基本一致,未观察到新的异常安全性信号。基于该研究结果,我们继续扩大样本量并进行了子宫内膜癌注册研究。
在本次ESMO Asia年会上,我们对宫颈癌队列研究进行了报告。该研究纳入了34例晚期宫颈癌患者,这些患者经历了至少一线含铂化疗失败、或治疗中出现无法耐受的毒性、或无法接受标准治疗。研究的主要终点为ORR,次要终点包括DCR、缓解持续时间(DoR)、mPFS、mOS、安全性等。其中,我们根据患者PD-L1表达情况的不同进行了分层,24例CPS≥1,8例CPS<1。
大显身手:“幸福组合”有望开启宫颈癌靶免联合新篇章
作为一项多中心、单臂、II期临床研究,请问目前本研究取得了怎样的阶段性成果?“幸福组合”在晚期宫颈癌治疗中的表现如何?
目前,宫颈癌免疫治疗的深入探索和研究为晚期患者的治疗开辟了新天地。然而,现有研究表明免疫治疗的单药疗效并不理想。以KEYNOTE-158研究[11]为例,对于化疗后进展、PD-L1表达阳性(CPS≥1)的复发或转移性宫颈癌患者,免疫单药治疗ORR仅为14.3%,中位PFS仅为2.1个月。虽然国内也批准上市了其他免疫单药治疗,但它们的疗效仍然有限。
在宫颈癌队列研究中,我们探索了呋喹替尼联合信迪利单抗在初治和经治宫颈癌患者中的应用。结果显示,在初治患者中,呋喹替尼联合信迪利单抗的ORR为50%,DCR为100%,mPFS为10.3个月,15个月的总生存率为83.3%;在经治患者中,ORR为29.6%,DCR为100%,mPFS为8.2个月,15个月OS率为70.0%,尤其在PD-L1 CPS>1的患者获益显著,ORR达到41.2%,mPFS为19.4个月,15个月的总生存率为76.0%。
表1 宫颈癌队列研究疗效结果
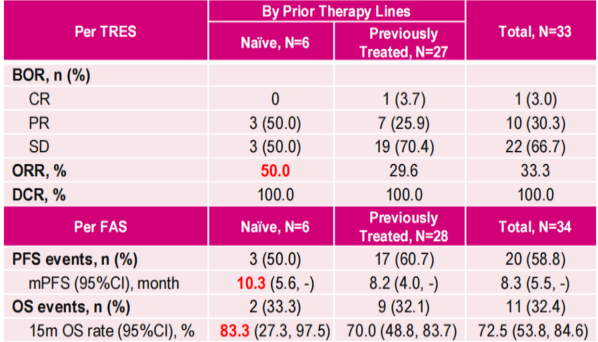
表2 经治患者疗效结果
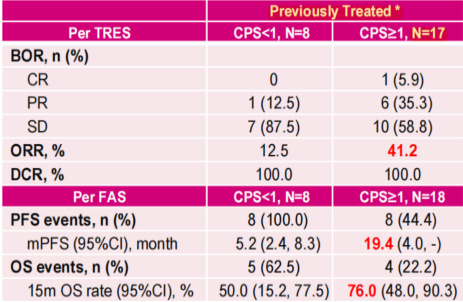
此外,我们发现该方案治疗后患者肿瘤的缩小程度显著:93.9%的患者肿瘤有所缩小,超过51.5%的患者肿瘤缩小超过30%,甚至有30%以上的患者的肿瘤缩小了一倍以上,为晚期宫颈癌患者带来了更长的生存获益。
图1 肿瘤应答评估瀑布图
图2 肿瘤应答评估泳道图
总的来说,我们的研究结果显示呋喹替尼联合信迪利单抗在晚期宫颈癌治疗中表现出良好的疗效,特别是在经治的PD-L1 CPS≥1的患者中,显示出了亮眼的中位PFS。此外,该联合治疗方案的安全性也整体可控。
未来可期:妇瘤领域本土原研药物前景广阔
论坛报
呋喹替尼同时在子宫内膜癌、宫颈癌进行了相关研究探索。您作为妇瘤领域研究的领军人物,能否谈谈您对呋喹替尼在妇瘤领域的潜力和应用前景有哪些期待?
呋喹替尼作为我国本土原研创新药,近期获得FDA批准用于治疗晚期结直肠癌,这证明了我国原研创新药物处于全球领先水平。本研究是呋喹替尼在妇科肿瘤领域的又一突破。
呋喹替尼联合免疫治疗有望为晚期复发转移性的宫颈癌患者,尤其对于PD-L1表达阳性的患者提供一种有潜力的治疗选择。通过其抗血管生成作用,呋喹替尼能够激活患者的免疫应答,从而有望为患者带来治疗获益。我们对呋喹替尼在妇瘤领域的潜力充满期待,期望它能够在宫颈癌治疗中发挥重要作用。
此外,呋喹替尼在既往的大型临床研究中显示出良好的安全性,这对于联合治疗方案来说非常重要。基于这些有效性和安全性的数据,提示呋喹替尼具备较好的应用潜力,我们期待它在妇瘤领域的应用能够为患者带来更好的疗效和生存优势。
同时作为呋喹替尼和信迪利单抗用于子宫内膜癌研究的主要研究者,我亲眼见证了该方案在子宫内膜癌治疗中具有明显的临床优势。这一方案已经在今年7月被药品审评中心纳入突破性治疗品种。我们期待它能尽早获得批准上市,为晚期子宫内膜癌患者带来新的选择。
[1] Xia C, Dong X, Li H, et al. Cancer statistics in China and United States, 2022: profiles, trends, and determinants. Chin Med J (Engl). 2022;135(5):584-590. Published 2022 Feb 9.
[2] Naga Ch P , Gurram L , Chopra S , et al. The management of locally advanced cervical cancer[J]. Curr Opin Oncol, 2018, 30(5):323-329.
[3] 中国抗癌协会肿瘤内分泌专业委员会.子宫颈癌手术分期中国专家共识(2023年版)[J].中国实用妇科与产科杂志,2023,39(10):996-1002.
[4] Marret G, Borcoman E, Le Tourneau C. Pembrolizumab for the treatment of cervical cancer. Expert Opin Biol Ther. 2019;19:871-877. 3
[5] Koh WJ, Abu-Rustum NR, Bean S, et al. Cervical Cancer, Version 3.2019, NCCN Clinical Practice Guidelines in Oncology. J Natl Compr Canc Netw. 2019;17(1):64-84.
[6] Boussios S, Seraj E, Zarkavelis G, et al. Management of patients with recurrent/advanced cervical cancer beyond first line platinum regimens: Where do we stand? A literature review. Crit Rev Oncol Hematol. 2016;108:164-174.
[7] ] Li J, Qin S, Xu RH, Shen L, Xu J, Bai Y, et al. Effect of Fruquintinib vs Placebo on Overall Survival in Patients With Previously Treated Metastatic Colorectal Cancer: The FRESCO Randomized Clinical Trial. Jama. 2018;319(24):2486-96.
[8] Dasari A, Lonardi S, Garcia-Carbonero R, et al. Fruquintinib versus placebo in patients with refractory metastatic colorectal cancer (FRESCO-2): an international, multicentre, randomised, double-blind, phase 3 study. Lancet. 2023;402(10395):41-53.
[9] Li Q, Cheng X, Zhou C, et al. Fruquintinib Enhances the Antitumor Immune Responses of Anti-Programmed Death Receptor-1 in Colorectal Cancer. Front Oncol. 2022;12:841977.
[10] Qin SK, et al. 2019 CSCO Oral presentation.
[11] Chung HC, Ros W, Delord JP, et al. Efficacy and Safety of Pembrolizumab in Previously Treated Advanced Cervical Cancer: Results From the Phase II KEYNOTE-158 Study. J Clin Oncol. 2019;37(17):1470-1478.
本资料由和黄医药提供支持。
本资料旨在促进医药信息的沟通和交流,而非广告宣传。
查看更多