查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





作者:福建省立医院 胡嘉庆 郑金辉
食管早癌的内镜下治疗开展已日趋成熟,但是由于早期病变难以发现和手术空间小,存在复发和残留的风险,如何降低风险和处理复发残余的病例,是目前困扰消化内镜医生的一个难题。
食管癌是我国常见恶性肿瘤,我国以鳞癌为主,欧美国家以腺癌为主,早期食管癌治疗后5年生存率可达到90%以上,早发现和早治疗对改善患者预后有着重要意义。尤其是ESD治疗备受关注,优势在于能够一次性完整切除病灶及提供病理诊断,且能保留食管解剖和功能,较之传统手术创伤小、并发症少,可改善患者生活质量。然而值得注意的是,由于早期食管癌及癌前病变较难发现,加之内镜治疗的手术范围小,可能导致病灶复发,影响患者预后。因此,如何降低内镜术后残留和复发,是目前治疗早期食管癌及癌前病变的研究热点。
食管早期癌治疗后残余复发的定义
根据《中国早期食管癌筛查及内镜诊治专家共识意见》所提出,残留及复发的定义如下:
残留(residual):术后6个月以内在原切除部位及周围1 cm内黏膜发现肿瘤病灶。
局部复发(local recurrence):手术6个月以后在原切除部位及周围1 cm内黏膜发现肿瘤病灶。
食管早期癌治疗复发及残留的危险因素及预防
食管早期癌常用的内镜切除技术主要包括内镜黏膜切除术(endoscopic mucosal resection,EMR)、内镜黏膜下剥离术(endoscopic submucosal dissection,ESD)等。指南中推荐对于可一次性完全切除的食管HGIN、M1期癌、M2期癌以及术前评估无可疑淋巴结转移的M3期癌可使用EMR治疗。目前EMR技术日趋多样化,EPMR(分片EMR)用于传统EMR不能一次完整切除的较大病灶,将病灶分块切除,但难以评估根治效果,且易导致病变局部残留或复发。分片切除是局部复发的危险因素。另外,分5片以上切除的病例局部复发率显著升高。
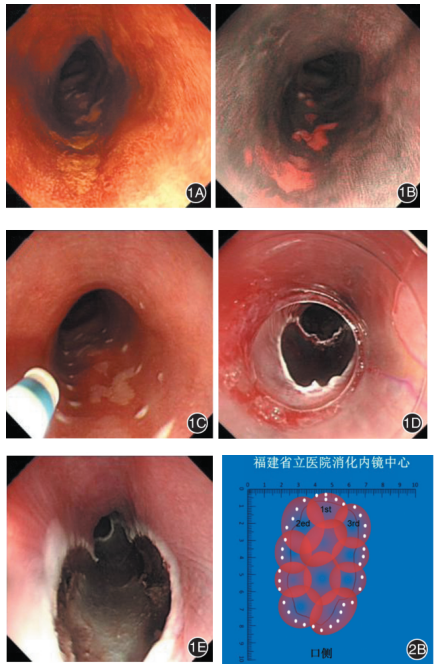
图1 内镜分片黏膜切除术操作过程
从完整切除及减少局部复发的观点来看,15 mm以上的病变应该用ESD行整块切除。指南中也提到对于食管HGIN、M1期癌、M2期癌以及术前评估无可疑淋巴结转移的M3期癌首选ESD治疗。既往Meta分析中发现ESD局部复发率明显低于EMR。国内EMR术后局部复发率为0~15.3%,ESD术后则为0~9.4%。复发可能与EMR方式、EMR分片数、病变部位、浸润深度、操作是否规范及食管癌家族史有关。过去的研究中,ESD后的局部复发率为0.0~2.6%,ESGE的指南中报告的局部复发率为0.35%(3/850)。
在术前明确肿瘤的侧方进展范围对于减少术后残留及复发尤为重要,在ESD整块切除的情况下,很少见到局部复发。目前用于诊断早期食管癌和癌前病变边界的内镜方法主要有色素内镜(碘液染色)、超声内镜、放大内镜及内镜窄带成像技术。相对于早期胃癌而言,早期食管癌及癌前病变的边界确定更为准确和清晰。
同时进行肿瘤浸润深度的评估也必不可少,通过观察肿瘤的大体观(包括巴黎分型、饱满程度、有无溃疡、有无结节)、碘染情况(有无榻榻米征)、放大内镜(包括IPCL形态、AVA大小)、超声内镜来综合评估肿瘤浸润深度,局限于M2或M3层的早期食管癌病例发生基底切缘残留的主要原因可能为ESD手术深度不够,因此原则上为避免基底切缘残留,剥离深度应该紧贴并暴露固有肌层。
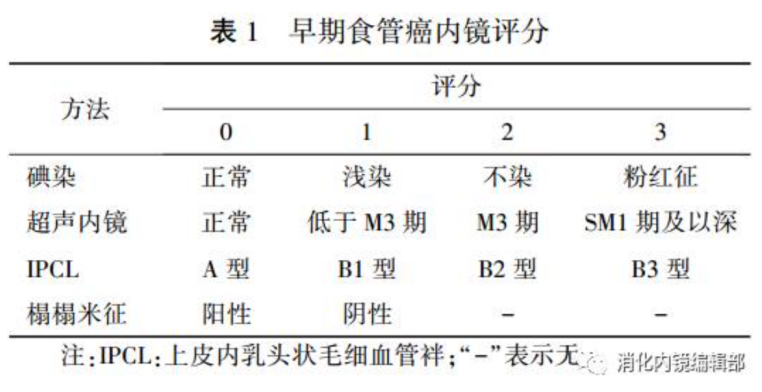
“福建省食管癌早诊早治促进联盟”在福建地区提出利用通过碘染、EUS、IPCL的AB分型及榻榻米征进行评分,碘染正常0分,浅染1分,不染2分,粉红征阳性3分;EUS正常0分,低于M3期1分,M3期2分,SM1期及以深3分;IPCL的AB分型中A型0分,B1型1分,B2型2分,B3型3分;榻榻米征阳性0分,阴性1分。建议对评分>5分的高危人群接受进一步治疗。通过该系统的推广应用,联盟内各单位首诊医师可较准确地评估确诊病例的严重程度,选择最适合的治疗措施。
在预防残留及复发方面,ESD术前对病灶边界及深度的准确评估是避免术后标本切缘残留的关键。既往研究显示,绝大多数侧切缘残余组织为低级别瘤变,且病灶累及食管环周3/4以上者更易发生侧切缘残留,可能和操作者为缓解术后食管狭窄程度在剥离范围上相对保守有关。需警惕的是,在充分评估食管病灶范围及深度的前提下,操作者应该避免对病变的过度切除,以免增加ESD术后食管狭窄的发生率,从而对患者的生活质量产生不同程度影响。病变切除后应仔细检查创面,可结合染色内镜观察。发现残留应及时进行处理。
在术后我们需要对标本进行评估,以明确是否进行治愈性切除,包括大体形态、部位、组织学类型、脉管浸润、水平切缘及垂直切缘情况。ESD术后标本切缘阳性会极大增加肿瘤残留和复发的风险,研究中发现多因素分析显示病变长度(≥5 cm)、病变浸润深度(M3以深)是早期食管癌及癌前病变ESD术后标本切缘阳性的独立危险因素。
肿瘤距离标本边缘1mm以上时局部复发率为0%。标本边缘可见肿瘤时,局部复发率为40%。在日本一项研究中随访27例(包括侧切缘阳性HM1/侧切缘不明HMx),中位随访时间3.8年内,局部复发一例也没有发现。所以即使ESD后的病理诊断中是HM1/HMx,也很少出现局部复发,但其风险仍不容忽视。既往其他文献中食道ESD中HM1或HMX的局部复发率病例占5.0%(39/767),其危险因素为肿瘤直径20mm以上及位于颈部食道。
食管早癌病灶治疗后残余复发的处理方式
目前对早期食管癌及癌前病变ESD术后标本切缘残留的最佳处理方式尚无统一意见。我们的经验是:此类患者需结合术后病理、标本切缘病理、患者基础状况、费用问题及个人及家庭意愿等多种因素进行综合判断选择个体化治疗方案。
指南中提到对于随访过程中发现病变残留或局部复发以及新发病灶,可再次予以内镜下治疗,内镜下治疗失败者可追加外科手术治疗或放化疗。有些直径略大的病变也可以通过EPMR、MBM等方式治疗,但不作为首选,因为EPMR、MBM为分片切除病灶,切下的小片组织由于受电凝等作用常影响进一步的病理评估。若术后残留部分较大,应再次追加内镜下局部治疗,对于小的残余病灶可用热活检钳或氩离子凝固术(argon plasma coagulation,APC)处理。切除的标本要回收,进行病理组织学检查。
根据既往研究,局部复发多在初次治疗后1年内发生,但也有几年后发生的情况,需要长期随访。有关非治愈性切除病例的内镜随访间隔,虽然没有明确的标准,但很多研究认为切除后1年内3~6个月复查是合适的。如果为HM1或肿瘤距切缘1 mm以内,则推荐更为慎重的随访。另外,复发的时间为7~35个月,因此至少需要3年的慎重随访。如上所述,因为对非治愈性切除病例更为严密的随访观察,即使有局部复发,分期也大多在cT1a-EP/LPM,大多能够用内镜切除。局部复发病例也和初发癌、异时性多发癌一样进行内镜诊断。如果判断为可以进行内镜切除的话,大多选择ESD。
针对局部注射时抬举不良和高度纤维化等原因内镜切除困难的病例,内镜下毁损治疗消融技术主要包括射频消融(radiofrequency ablation,RFA)、光动力疗法(photodynamic therapy,PDT)、冰冻疗法(cryotherapy)、氩离子束凝固术(argon plasma coagulation,APC)。虽然以上方法有无法进行组织病理学评价的缺点,但既往研究中报告了良好的局部控制。值得注意的是,既往研究中分析了6例早期食管癌完全消融术后局部复发病例,复发病灶内镜切除病理学显示肿瘤病灶均存在黏膜下腺体累及。因此,目前对于早期食管鳞癌及HGD,推荐首选ESD或EMR尝试将病灶整块切除,获得准确病理学分期并指导进一步治疗和随访。另外,由于瘢痕的原因,局部复发病例的内镜切除技术上比较困难,最好是在设备齐全的中心,由操作熟练的医师进行。此类病例多可通过内镜下治疗清除,内镜下治疗失败者可追加手术或放射、化学疗法。
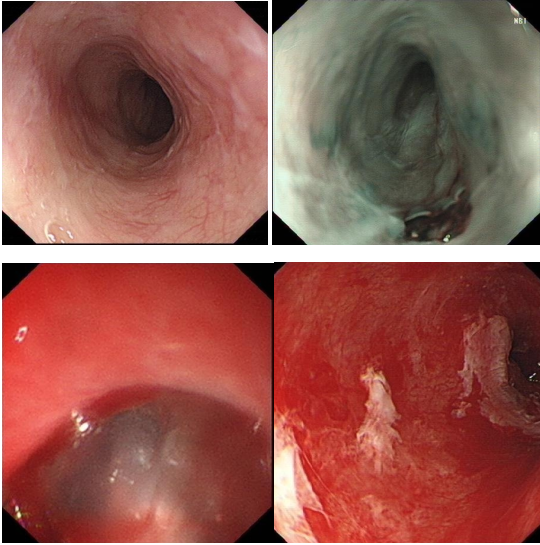
图2 ESD术后复发行射频消融术
食道腺癌内镜切除术后的局部复发
西方国家巴雷特腺癌在食管癌中发病率最高,且预后较差。高度异常增生和巴雷特黏膜腺癌的长期预后较好。前期的研究表明,对于局限于黏膜内的肿瘤,内镜切除(ER)和外科切除(SR)对患者的长期生存没有明显差异。
日本的多中心共同研究中,食管胃结合部腺癌的ESD/EMR整块切除率为99.1/60.8%,切缘阴性整块切除率为87.9/49.0%,5年累积局部复发率0.5/13.0%,ESD数据更好。另外,内镜切除后局部复发病例中没有切缘阴性的整块切除的病例。
国外食道腺癌局部复发的危险因子有分片切除、长段巴雷特食管(LSBE),同时性多发癌。值得注意的一点是——局部复发的定义在欧美和日本是不同的。在欧美,很多报告都将异时性多发与局部复发病变一起定义为异时性癌。另一方面,日本将异时多发癌与局部复发病变分开考虑。其理由是,欧美的食道腺癌多以LSBE(长段巴雷特食管)为背景,以LSBE为背景的巴雷特腺癌难以进行内镜下的范围诊断,内镜切除后异时性多发癌发生率高被认为是受此影响。另一方面,日本的巴雷特腺癌多以短段巴雷特食管(SSBE)为背景,欧美与日本的异时性多发癌的风险因而不同。
在食道腺癌内镜切除术后的局部复发的治疗方面,在欧美国家,标准的方法是对内镜检查中能够识别的病变实行EMR,将残留的巴雷特黏膜用射频治疗(RFA)烧灼。但是,在日本及中国,食道腺癌大多以SSBE为背景,且RFA没有获得上市许可,对于EMR/ESD后的局部复发病例,与食道鳞癌一样,常常再度选择内镜切除。
小结
通过规范的诊断及治疗,目前食管内镜术后残留及复发病例相对较少,但也有发生。通过放大内镜及喷洒碘液行确切的肿瘤侧方范围诊断,通过超声内镜及放大内镜观察IPCL形态进行肿瘤浸润深度的判断,在精准标记下切开剥离以保证边切缘阴性,同时通过术中保持合适剥离层面以尽量保证底切缘的阴性的整块切除,有助于减少残留及复发的风险。通过遵循标准的内镜随访,早期发现残留或复发病灶,绝大多数都可再次内镜切除,必要时可追加射频消融进行补充术后。而食管腺癌内镜治疗后复发病例较少,切缘阴性的整块切除的病例基本不会出现复发。欧美与中日相比,在复发的定义上有所差别,治疗方式上欧美主要采用RFA进行残余及复发病变的治疗,而中日多采用内镜下的治疗方法(EMR及ESD)进行处理。
原创内容,转载须授权

胡嘉庆
福建省消化内镜中心
医师 医学硕士
福建省医学会消化内镜学分会静脉曲张学组委员
福建省医学会消化内镜学分会食管学组委员
熟练掌握胃、肠镜操作,参与开展内镜治疗如(EUS、ESD、ERCP)。
发表中华系列期刊2篇,国内期刊论文4篇,主持福建医科大学启航基金1项,参与省级课题多项,参编著作1部。
2021年获“镜武门”ERCP病例大赛华南区第一名,获第一届全国ERCP规范化诊治华东区优秀病例。

郑金辉
福建省立医院消化内镜中心 副主任医师
中华医学会消化内镜学分会ERCP学组委员
福建省医学会消化内镜学分会静脉曲张学组成员
福建省医学会消化内镜学ERCP学组成员
本文版权属于中国医学论坛报社
查看更多