查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





作者:华中科技大学同济医学院附属协和医院 聂文闻 刘坤维
2023年5月26日,华中科技大学同济医学院附属协和医院(以下简称“武汉协和医院”)心脏大血管外科夏家红、吴杰教授团队在心血管期刊《循环》杂志(影响因子: 39.9分)上发表了题为“肝脏通过PCSK9/CD36通路对心脏移植排斥反应进行免疫调控”的研究论文,报道了心脏移植排斥反应(Heart Transplant Rejection,HTR)中肝脏通过PCSK9/CD36通路进行免疫调节的新机制,提示该通路的调节可能是HTR的潜在治疗靶点。武汉协和医院心脏大血管外科夏家红教授和吴杰教授为共同通讯作者,我院心脏大血管外科张曦博士和许恒博士为本文的共同第一作者。
心脏移植是治疗难治性终末期心脏病有效的方法,心脏移植排斥反应是导致心脏移植预后不佳的主要原因。以往的研究主要集中在移植物和免疫器官中的免疫细胞上,而忽略了非免疫器官和相关分子在心脏移植排斥反应中的作用。
夏家红教授团队通过收集临床心脏移植患者和心脏移植小鼠受体血清进行ELISA检测,发现在HTR期间受体内的PCSK9水平显著升高,并且通过基因敲除和抗体中和的方式抑制受体小鼠的PCSK9,能够明显减轻HTR。通过多器官筛选,证实HTR期间PCSK9主要来源于受体的肝脏。通过肝脏多组学和体外实验研究,发现HTR过程中受体小鼠的肝脏的炎症和代谢通路发生了显著改变,并阐明了TNF-α和IFN-γ通过SREBP2协同促进肝细胞PCSK9的表达。机制研究证明PCSK9能够通过CD36途径促进巨噬细胞的炎性功能,从而介导效应T细胞的分化和IFN-γ的产生。这些结果揭示了HTR期间受体肝脏通过PCSK9/CD36通路进行免疫调节的新机制,并提示该调节通路可能是HTR的潜在治疗靶点。
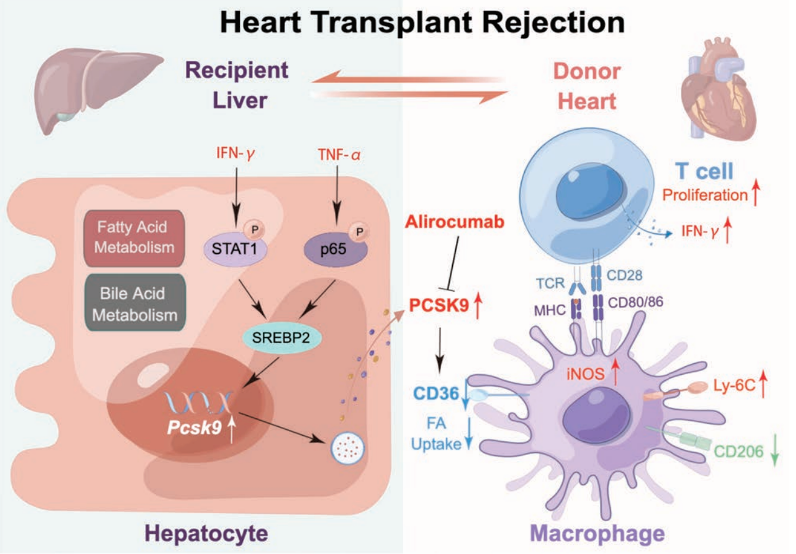
肝脏调节移植心脏免疫反应的机理示意图(源自Circulation)
该研究首次揭示了HTR期间受体肝脏通过PCSK9/CD36通路进行免疫调节的新机制,不仅发现了HTR的临床诊疗新靶点,而且为移植免疫学的研究打开了新大门——“非免疫器官调控机制”。该研究成果也受邀在美国圣地亚哥(San Diego)举办的2023年美国器官移植大会(American Transplant Congress)上作口头发言。
查看更多