200
评论
查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





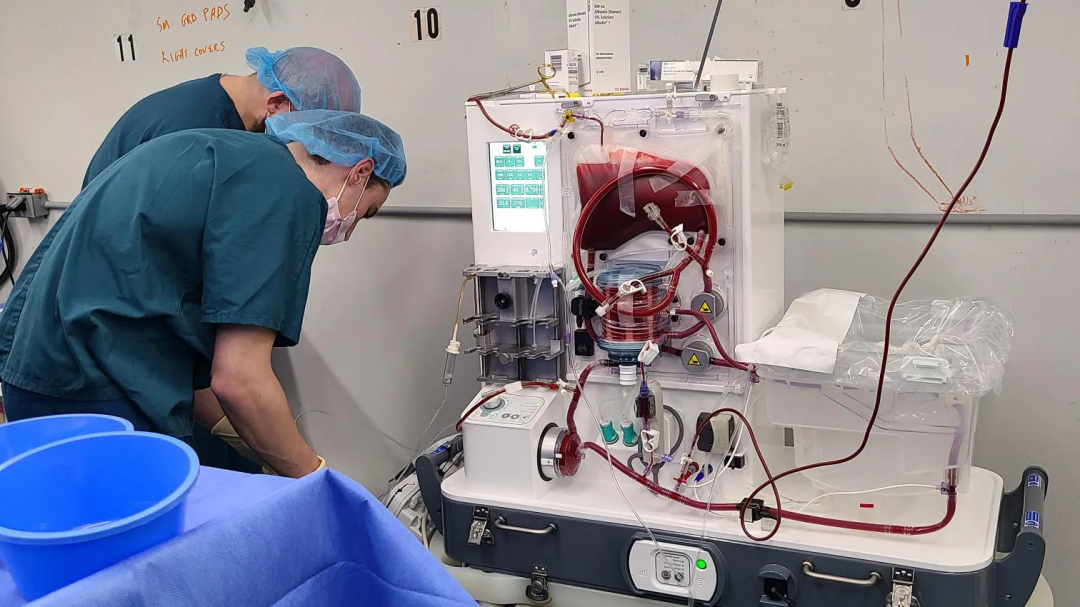
物种间免疫介导的不相容性导致器官排斥

该研究报道了将基因编辑猪肾脏移植到非人灵长类动物(NHP)体内的手术设计和成功过程。该研究使用尤卡坦迷你猪作为供体猪,对其进行了创纪录的多达69处基因编辑,敲除了会引起排斥反应的表达聚糖抗原的3个基因(GGTA1、CMAH和B4GALNT2L),敲入了7个人类基因以减少灵长类免疫系统的对抗,这7个人类基因包括补体相关的CD46和CD55、凝血相关的THBD和PROCR、先天免疫相关的CD47,抑制缺血再灌注损伤、细胞凋亡和炎症的TNFAIP3和HMOX1。另外59处基因编辑则是让猪逆转录病毒基因的所有拷贝失活。
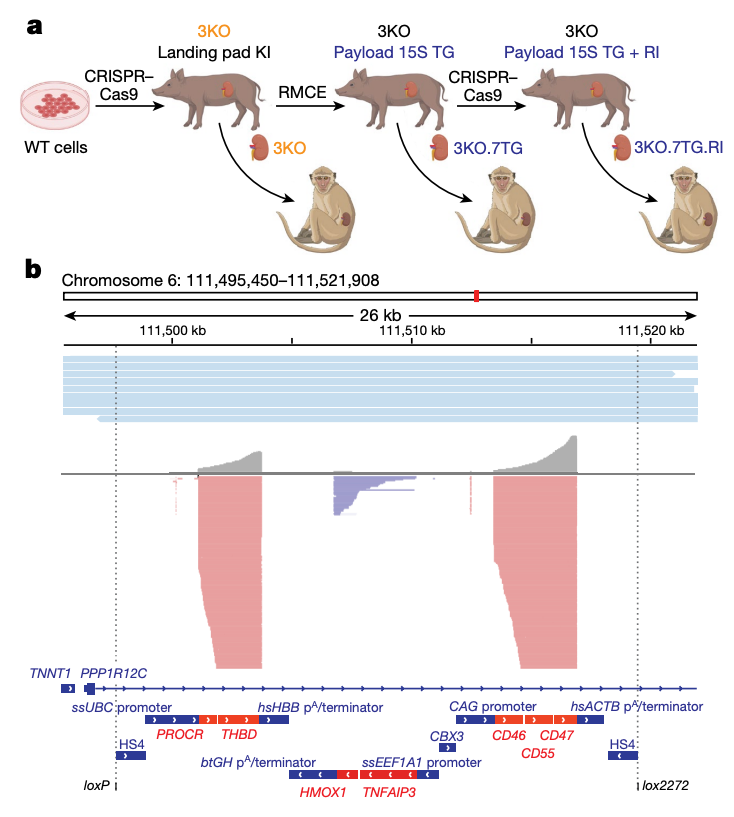
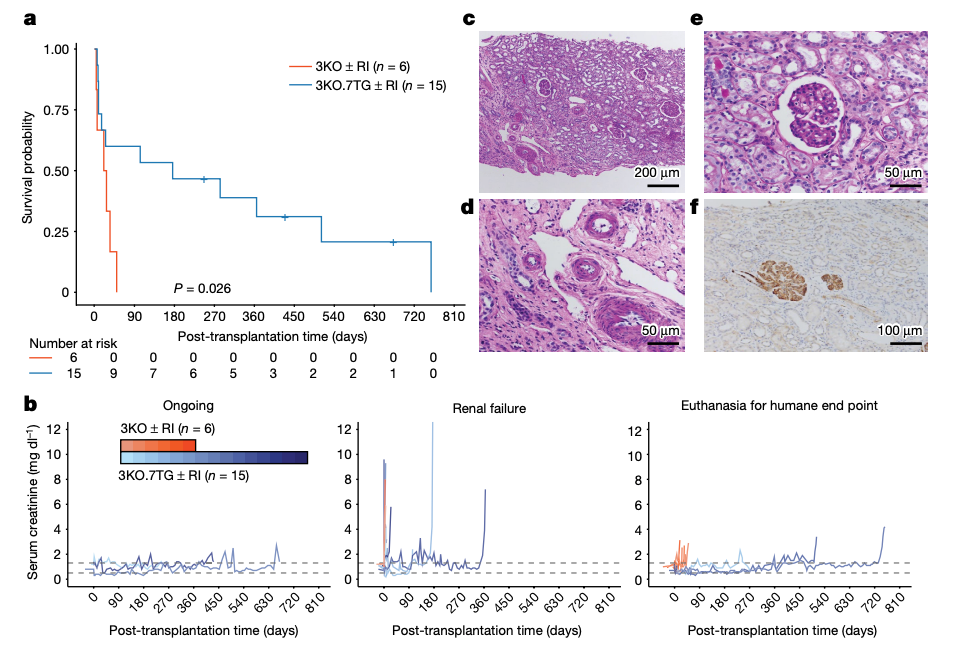
这项异种器官移植的里程碑式临床前数据,证明了基因编辑的猪肾脏可以在异种移植后长期存活,在移植到非人灵长类动物(NHP)后能够维持器官功能并存活超过两年时间。这些结果显示出今后猪器官移植到人体的前景,并推动该技术向临床测试更进一步。
作者:王聪
来源:生物世界
查看更多